熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Induction of photosynthesis under anoxic condition in Thalassiosira pseudonana and Euglena gracilis: interactions between fermentation and photosynthesis
假海鏈藻和纖細裸藻在缺氧條件下誘導(dǎo)光合作用:發(fā)酵與光合作用之間的相互作用
來源:Front. Plant Sci. 14:1186926.
1. 摘要核心內(nèi)容
研究對象:兩種次級內(nèi)共生微藻——海洋硅藻 假微型海鏈藻(Thalassiosira pseudonana) 和原生生物 纖細裸藻(Euglena gracilis)。
核心發(fā)現(xiàn):
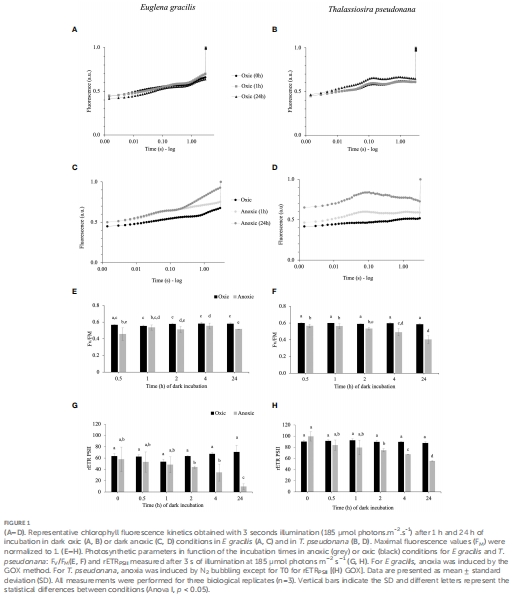
在黑暗缺氧條件下培養(yǎng)后,兩種藻類均能恢復(fù)光合線性電子傳遞(LEF),并表現(xiàn)出短暫的 PSI環(huán)式電子流(CEF) 激活(圖1, 圖7)。
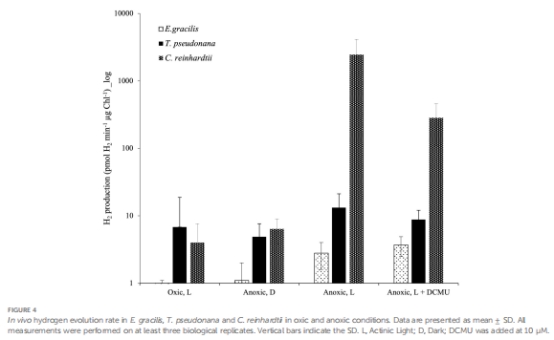
與綠藻模型 萊茵衣藻(Chlamydomonas reinhardtii) 不同,二者在缺氧條件下 未檢測到持續(xù)的氫酶活性(圖4),表明其光合恢復(fù)依賴其他電子傳遞途徑。
提出可能的替代電子傳遞機制:硅藻通過 異化硝酸鹽還原為銨(DNRA),裸藻通過 蠟酯發(fā)酵 維持光合電子傳遞(討論4.3節(jié))。
2. 研究目的
探究非綠藻微藻(硅藻和裸藻)在缺氧條件下如何協(xié)調(diào) 發(fā)酵代謝 與 光合作用。
驗證二者是否依賴類似萊茵衣藻的 氫酶介導(dǎo)的電子傳遞 途徑。
揭示缺氧環(huán)境中微藻光合作用的進化適應(yīng)性策略。
3. 研究思路
graph TD
A[缺氧誘導(dǎo)] --> B[光合參數(shù)檢測]
B --> C[氫酶活性驗證]
C --> D[電子傳遞機制解析]
D --> E[替代途徑假設(shè)]
實驗設(shè)計:
缺氧條件:黑暗缺氧培養(yǎng)(24小時),通過氮氣鼓泡或葡萄糖氧化酶(GOX)系統(tǒng)實現(xiàn)(方法2.2)。
光合參數(shù)檢測:
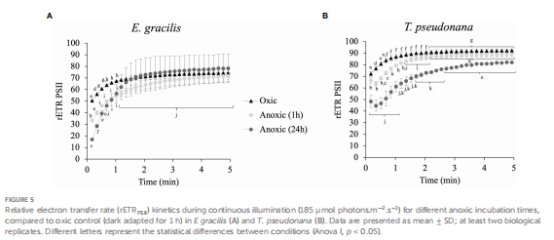
葉綠素熒光動力學(xué):測量PSII量子效率(Fv/Fm)和相對電子傳遞速率(rETRPSII)(圖1, 圖5)。
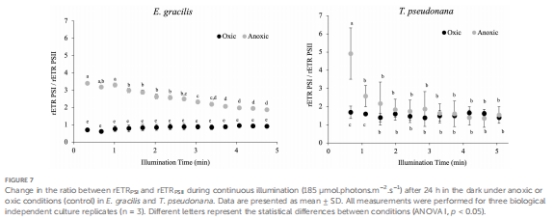
PSI氧化還原狀態(tài):通過P700信號計算rETRPSI(圖7)。
氫酶活性:使用 Unisense氫微電極 實時監(jiān)測H?釋放(圖4)。
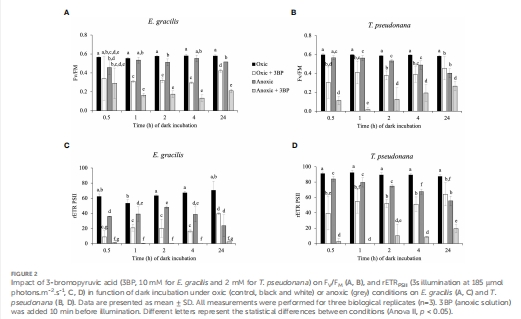
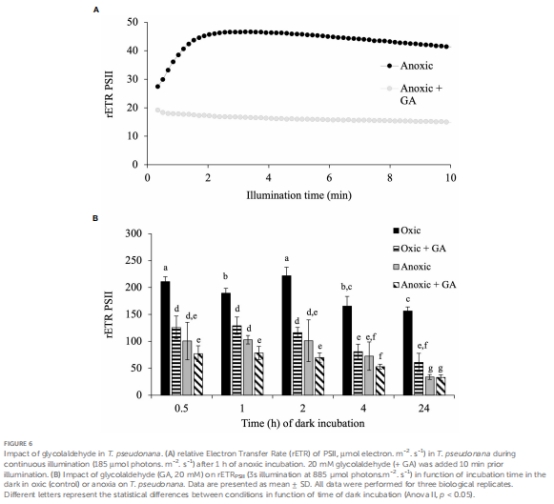
抑制劑實驗:3-溴丙酮酸(3BP)抑制發(fā)酵途徑,乙醛酸(GA)抑制卡爾文循環(huán)(圖2, 圖6)。
4. 關(guān)鍵數(shù)據(jù)及研究意義
數(shù)據(jù)來源與意義
檢測指標 數(shù)據(jù)來源 研究意義 圖表位置
rETRPSII/rETRPSI比值 葉綠素熒光動力學(xué) 揭示PSI環(huán)式電子流(CEF)的激活程度:缺氧條件下比值升高表明CEF增強(圖7) 圖7
H?釋放速率 Unisense氫微電極 核心發(fā)現(xiàn):兩種藻類缺氧時光照下H?釋放未增加,否定氫酶主導(dǎo)的電子傳遞(圖4) 圖4
3BP抑制效應(yīng) 發(fā)酵途徑抑制劑 缺氧光合恢復(fù)依賴發(fā)酵途徑(圖2),證明發(fā)酵與光合的耦合 圖2
GA抑制效應(yīng) 卡爾文循環(huán)抑制劑 硅藻中GA抑制光合恢復(fù)(圖6),表明卡爾文循環(huán)是電子最終受體 圖6
5. 結(jié)論
光合恢復(fù)機制:
缺氧條件下,兩種藻類通過 短暫激活PSI環(huán)式電子流(CEF) 維持光合電子傳遞(圖7),避免光系統(tǒng)過度還原。
無氫酶參與:Unisense電極數(shù)據(jù)證實二者無光照依賴的H?釋放(圖4),與萊茵衣藻截然不同。
替代電子傳遞途徑:
硅藻(T. pseudonana):可能通過 DNRA途徑(硝酸鹽→銨)消耗電子,支持卡爾文循環(huán)再激活(討論4.3)。
裸藻(E. gracilis):依賴 蠟酯發(fā)酵,將電子傳遞至線粒體,維持胞內(nèi)氧化還原平衡(討論4.3)。
進化意義:微藻在缺氧環(huán)境中演化出多樣化的電子傳遞策略,減少對氧敏感酶(如氫酶)的依賴。
6. Unisense氫微電極數(shù)據(jù)的科研意義詳解
檢測原理與參數(shù)
電極型號:Unisense H?微傳感器(方法2.6)。
檢測指標:實時監(jiān)測光照/黑暗條件下H?釋放速率(pmol·min?1·μg chl?1)。
關(guān)鍵參數(shù):
靈敏度:可檢測低至5 pmol·min?1·μg chl?1的H?釋放。
實時性:動態(tài)追蹤光照刺激后的H?釋放變化。
研究意義
證偽氫酶主導(dǎo)假說:
在萊茵衣藻中,缺氧光照下H?釋放速率可達 2 nmol·min?1·μg chl?1(圖4),而兩種目標藻類僅 5 pmol·min?1·μg chl?1(背景水平)。這一數(shù)據(jù)直接否定了氫酶在二者光合恢復(fù)中的核心作用。
推動新機制發(fā)現(xiàn):
陰性結(jié)果(無H?釋放)促使研究者轉(zhuǎn)向其他電子傳遞途徑(如DNRA、蠟酯發(fā)酵),深化對微藻代謝多樣性的認知。
技術(shù)優(yōu)勢:
微尺度檢測:適用于小體積樣品(如4 mL比色皿),避免傳統(tǒng)氣相色譜對樣品量的限制。
缺氧環(huán)境兼容:整合氮氣帳篷(圖4插圖),確保檢測全程嚴格缺氧。
對領(lǐng)域的影響
為研究非模式藻類的缺氧代謝提供可靠工具,避免因依賴綠藻模型而產(chǎn)生認知偏差。
推動針對硅藻/裸藻獨特代謝途徑的工程改造(如利用DNRA途徑優(yōu)化廢水脫氮)。
總結(jié)
本研究通過整合Unisense微電極技術(shù)與光合生理學(xué)方法,揭示了硅藻和裸藻在缺氧環(huán)境中不依賴氫酶的光合作用恢復(fù)機制。Unisense電極的關(guān)鍵作用在于 精準量化H?釋放,為否定傳統(tǒng)假說提供直接證據(jù),進而推動對新型電子傳遞途徑(DNRA、蠟酯發(fā)酵)的探索。這一發(fā)現(xiàn)不僅拓展了對微藻逆境生理的理解,也為生物能源和環(huán)境污染修復(fù)提供了新思路。