熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Evaluation of H2S gas removal by a biotrickling filter: Effect of oxygen dose on the performance and microbial communities
生物滴濾器去除 H 2 S 氣體的評估:氧氣劑量對性能和微生物群落的影響
來源:Process Safety and Environmental Protection 166 (2022) 30–40
摘要核心內(nèi)容
研究通過生物滴濾塔(BTF) 探究氧氣劑量(1%-10%)對H?S生物去除的影響機制。核心發(fā)現(xiàn):
氧氣劑量調(diào)控產(chǎn)物分布:低氧(1%)時單質(zhì)硫(S?)產(chǎn)率達78.13%,高氧(10%)時硫酸鹽(SO?2?)占80.39%;
微生物群落響應(yīng):低氧主導(dǎo)菌屬為硫氧化菌(如Terrimicrobium),高氧時嗜酸菌Acidithiobacillus占比72.87%;
高效去除性能:H?S去除率≥94.1%,最大去除能力達6.00±0.35 gH?S·m?3·h?1;
技術(shù)亮點:使用丹麥Unisense微電極精準監(jiān)測溶解態(tài)H?S(D_{H?S}),證實微生物轉(zhuǎn)化速率快于氣液傳質(zhì)速率。
研究目的
揭示氧氣劑量對BTF脫硫性能的影響規(guī)律;
解析硫產(chǎn)物(S?、SO?2?)分配的氧控機制;
探究微生物群落結(jié)構(gòu)與功能的氧適應(yīng)性;
建立H?S生物氧化路徑模型,指導(dǎo)工業(yè)應(yīng)用優(yōu)化。
研究思路
實驗設(shè)計:
構(gòu)建BTF系統(tǒng)(圖1),聚氨酯填料負載微生物;
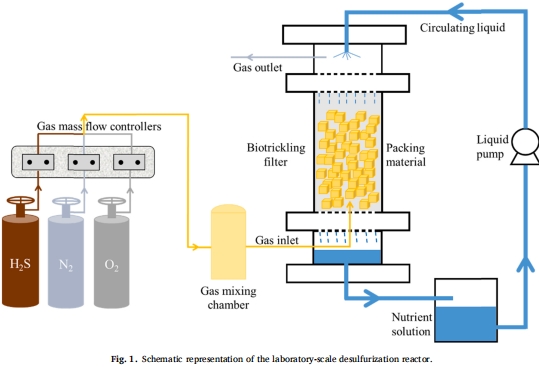
分4階段調(diào)控氧氣劑量(1%、3%、5%、10%),每階段10天;
恒定H?S進氣濃度(0.30 g·m?3),空床停留時間3分鐘。
數(shù)據(jù)采集:
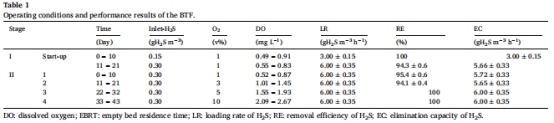
性能參數(shù):H?S去除率(RE)、去除能力(EC)(表1);
硫產(chǎn)物:SO?2?、SO?2?、S2?濃度(離子色譜)及S?(質(zhì)量平衡法計算);
微生物群落:16S rRNA高通量測序(門/屬水平);
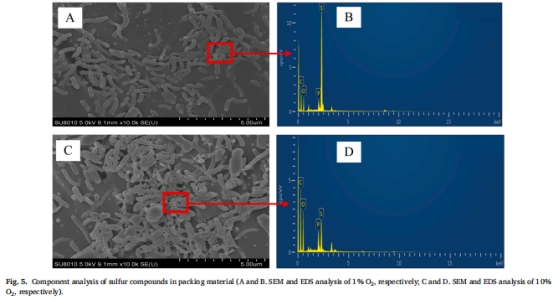
填料表征:SEM-EDS分析元素分布(圖5)。
檢測技術(shù):
溶解H?S:Unisense H?S微電極(D_{H?S})實時監(jiān)測;
溶解氧(DO):電極法跟蹤液相氧動態(tài)。
關(guān)鍵數(shù)據(jù)及研究意義
1. H?S去除性能(圖2 & 表1)
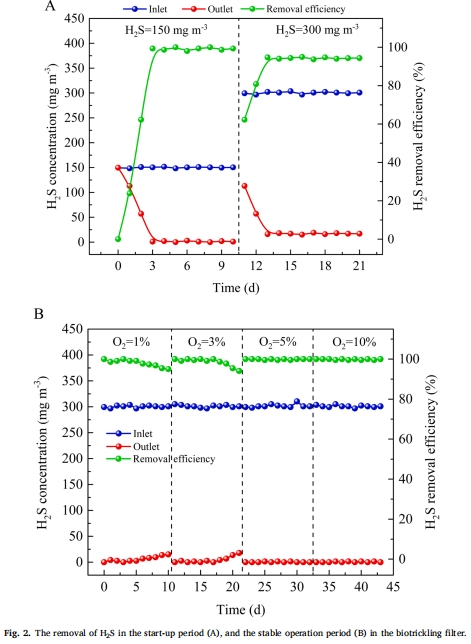
數(shù)據(jù)來源:進氣/出氣H?S濃度監(jiān)測(表1),去除率計算。
核心發(fā)現(xiàn):
氧濃度↑1%→10%,RE從95.4%升至100%(圖2B);
EC最大值6.00 gH?S·m?3·h?1(10% O?)。
研究意義:證實高氧提升微生物氧化活性,為工程化氧控策略提供依據(jù)。
2. 硫產(chǎn)物分布(圖3 & 圖4)
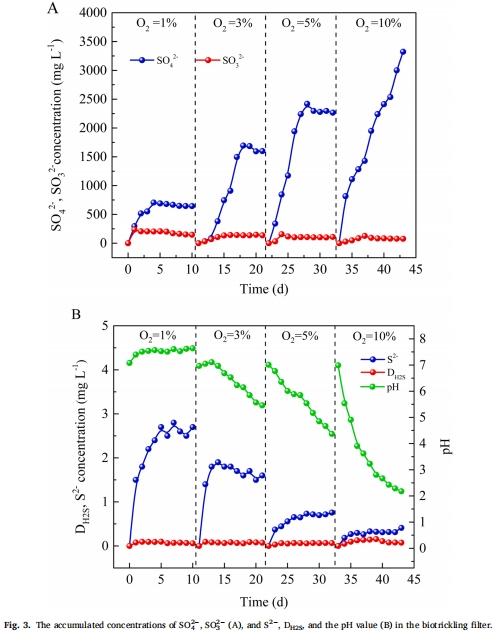
數(shù)據(jù)來源:液相離子色譜(SO?2?、SO?2?)、S2?電極、S?質(zhì)量平衡(式8)。
核心發(fā)現(xiàn)(圖4):
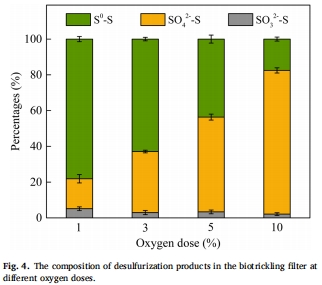
1% O?:S?占比78.13%(主產(chǎn)物);
10% O?:SO?2?占比80.39%(主產(chǎn)物)。
研究意義:揭示氧劑量定向調(diào)控硫形態(tài),支持S?資源化回收(低氧)或硫酸鹽生成(高氧)。
3. 微生物群落(圖6)
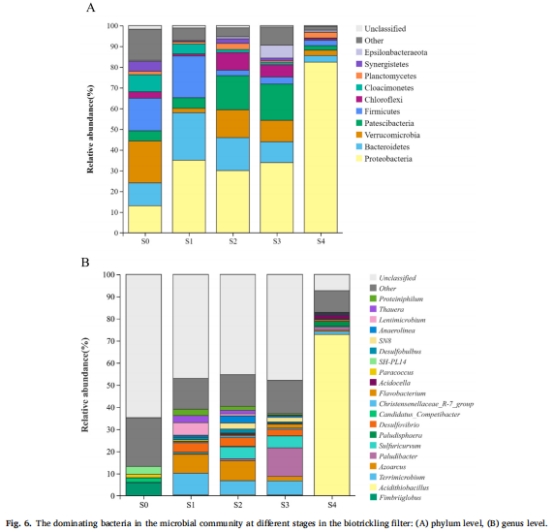
數(shù)據(jù)來源:16S測序(樣品S1-S4)。
核心發(fā)現(xiàn)(圖6B):
1% O?:Terrimicrobium(9.81%)、Azoarcus(8.53%)主導(dǎo)S?生成;
10% O?:Acidithiobacillus(72.87%)主導(dǎo)SO?2?生成。
研究意義:闡明功能菌群的氧適應(yīng)性,為菌劑強化提供靶標。
4. 填料表征(圖5)
數(shù)據(jù)來源:SEM-EDS元素分析。
核心發(fā)現(xiàn):
1% O?:硫元素占比76.08%(證實S?沉積);
10% O?:硫元素降至16.69%(SO?2?溶解流失)。
研究意義:驗證質(zhì)量平衡計算結(jié)果,直觀展示硫形態(tài)轉(zhuǎn)變。
丹麥Unisense電極的研究意義
技術(shù)原理
選擇性監(jiān)測溶解H?S(D_{H?S}):微電極尖端(<0.1 mm)直接穿透液膜,實時響應(yīng)溶解態(tài)H?S濃度變化(非氣態(tài)H?S)。
高時空分辨率:秒級響應(yīng)捕捉氣液傳質(zhì)與微生物代謝動態(tài)。
關(guān)鍵數(shù)據(jù)(圖3B)
D_{H?S}始終低于0.1 mg·L?1(遠低于進氣H?S濃度),證明微生物轉(zhuǎn)化速率>氣液傳質(zhì)速率。
pH驟降時(10% O?→pH=2.18)D_{H?S}仍穩(wěn)定,表明嗜酸菌保持高效代謝。
研究價值
揭示限速步驟:D_{H?S}極低說明系統(tǒng)性能受氣液傳質(zhì)限制而非生物活性;
驗證代謝路徑:低D_{H?S}佐證H?S→S?/SO?2?的快速轉(zhuǎn)化(圖7路徑);
指導(dǎo)工程優(yōu)化:需強化傳質(zhì)(如增加比表面積)而非僅提高氧量。
結(jié)論
氧控產(chǎn)物分配:低氧(≤3%)富集S?(>62.9%),高氧(≥5%)傾向SO?2?(>53.1%);
微生物定向馴化:Acidithiobacillus在酸性高氧環(huán)境占比>72%,支撐系統(tǒng)穩(wěn)定性;
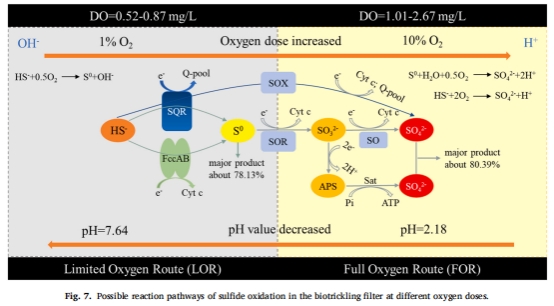
反應(yīng)路徑模型(圖7):
限氧路徑(LOR):H?S → S?(依賴SQR酶);
富氧路徑(FOR):S? → SO?2?(依賴SOR酶);
工程啟示:通過氧劑量調(diào)控可實現(xiàn)硫資源定向回收(S?)或硫酸鹽生成(SO?2?)。
Unisense電極的行業(yè)價值
對比傳統(tǒng)溶解H?S檢測方法(如甲基藍比色法):
參數(shù) Unisense微電極 傳統(tǒng)方法
響應(yīng)時間 秒級 分鐘級
空間分辨率 亞毫米級 整液平均
抗干擾性 不受色度/濁度影響 需預(yù)處理
實時性 在線連續(xù)監(jiān)測 離線采樣
該技術(shù)為生物脫硫系統(tǒng)的動態(tài)調(diào)控和機制解析提供不可替代的工具支撐。