熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Visualization of mRNA Expression in Pseudomonas aeruginosa Aggregates Reveals Spatial Patterns of Fermentative and Denitrifying Metabolism
銅綠假單胞菌聚集體中 mRNA 表達的可視化揭示了發(fā)酵和反硝化代謝的空間模式
來源:Applied and Environmental Microbiology June 2022 Volume 88 Issue 11
摘要核心內(nèi)容
研究利用雜交鏈?zhǔn)椒磻?yīng)(HCR v3.0) 技術(shù)實現(xiàn)了銅綠假單胞菌(Pseudomonas aeruginosa)生物膜內(nèi)代謝基因的單細(xì)胞級空間可視化:
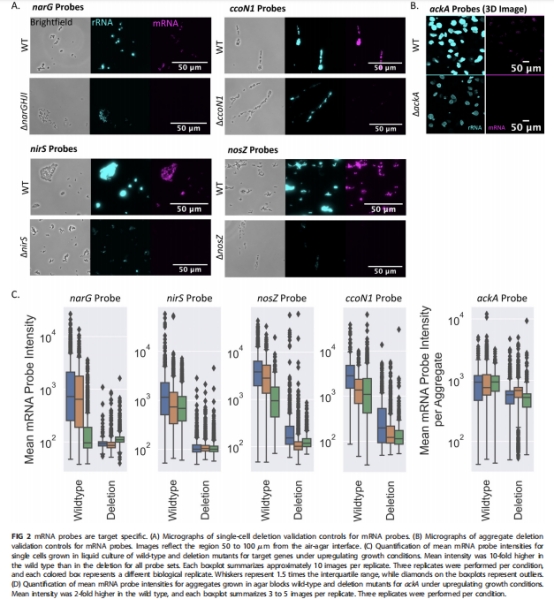
開發(fā)新型探針:針對呼吸(ccoN1)、反硝化(narG, nirS, nosZ)和發(fā)酵(ackA)基因設(shè)計特異性探針(圖2驗證);
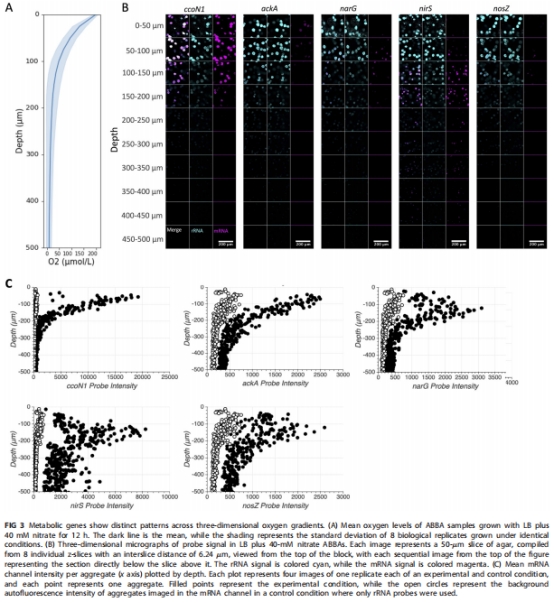
揭示代謝分區(qū):生物膜聚集體內(nèi)存在明確代謝分區(qū)——有氧區(qū)(表層)高表達ccoN1,缺氧區(qū)(中層)富集反硝化基因,無氧核心(深層)激活發(fā)酵基因ackA(圖3);
技術(shù)突破:首次在不依賴基因編輯條件下實現(xiàn)多代謝途徑的空間共定位,分辨率達單細(xì)胞水平。
研究目的
開發(fā)非侵入式空間轉(zhuǎn)錄組技術(shù),解析生物膜微環(huán)境異質(zhì)性;
闡明氧梯度對銅綠假單胞菌代謝分區(qū)的調(diào)控機制;
建立基因表達-微環(huán)境關(guān)聯(lián)模型,為生物膜耐藥性研究提供新視角。
研究思路
探針設(shè)計與驗證:
設(shè)計ccoN1(細(xì)胞色素c氧化酶)、narG(硝酸鹽還原酶)、nirS(亞硝酸鹽還原酶)、nosZ(氧化亞氮還原酶)、ackA(乙酸激酶)的HCR探針(表1);


通過基因敲除株驗證探針特異性(圖2A-D)。
生物膜模型構(gòu)建:
采用瓊脂塊生物膜分析法(ABBA),在LB+40mM硝酸鹽中培養(yǎng)12小時(圖3A);
使用丹麥Unisense微電極測量氧梯度(圖3A)。
空間轉(zhuǎn)錄組分析:
雙通道HCR成像:16S rRNA(青色)標(biāo)記細(xì)胞活性,mRNA(品紅)標(biāo)記目標(biāo)基因;
量化聚集體內(nèi)基因表達強度與空間分布(圖3B-C)。
關(guān)鍵數(shù)據(jù)及研究意義
1. 探針特異性驗證(圖2)
數(shù)據(jù)來源:野生型與突變株的熒光強度對比。
核心發(fā)現(xiàn):
野生株熒光強度比突變株高10倍(narG, nirS, nosZ, ccoN1)或2倍(ackA);
非特異性結(jié)合可忽略(背景熒光點與細(xì)胞不重疊)。
研究意義:為空間定位提供高信噪比工具,避免假陽性干擾。
2. 氧梯度與基因表達空間關(guān)聯(lián)(圖3)
數(shù)據(jù)來源:Unisense氧電極測量ABBA氧梯度(圖3A),HCR成像量化基因表達。
核心發(fā)現(xiàn):
0-50μm(有氧區(qū)):ccoN1表達最強(PCC=0.956 vs 16S rRNA),ackA在聚集體核心激活;
50-150μm(缺氧區(qū)):narG峰值(聚集體內(nèi)部),nirS擴散至整個聚集體;
>150μm(無氧區(qū)):nirS持續(xù)高表達,nosZ零星出現(xiàn)。
研究意義:證實氧梯度驅(qū)動代謝分區(qū),反硝化基因表達受一氧化氮信號級聯(lián)調(diào)控。
3. 代謝路徑的空間解耦(圖4)
4. 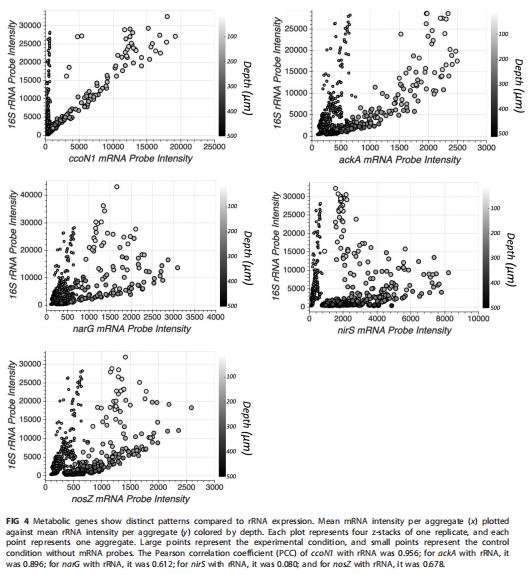
數(shù)據(jù)來源:基因表達與16S rRNA相關(guān)性分析。
核心發(fā)現(xiàn):
ccoN1與細(xì)胞活性強正相關(guān)(基礎(chǔ)代謝),ackA在低氧高活性區(qū)特異激活;
反硝化基因(narG, nosZ)與細(xì)胞活性弱相關(guān)(PCC=0.612-0.678),受微環(huán)境特異性誘導(dǎo)。
研究意義:揭示發(fā)酵與反硝化的競爭關(guān)系——缺氧區(qū)富集硝酸鹽時反硝化主導(dǎo),無氧核心轉(zhuǎn)向發(fā)酵。
結(jié)論
代謝分區(qū)機制:
生物膜表層:有氧呼吸(ccoN1高表達);
中層過渡區(qū):反硝化主導(dǎo)(narG→nirS→nosZ級聯(lián)激活);
深層無氧核心:發(fā)酵途徑(ackA維持ATP合成)。
技術(shù)應(yīng)用價值:
HCR v3.0實現(xiàn)多基因空間共定位,規(guī)避遺傳修飾需求;
為臨床生物膜(如囊性纖維化肺部感染)的代謝異質(zhì)性研究提供新工具。
丹麥Unisense電極的研究意義
技術(shù)原理與數(shù)據(jù)作用
微米級氧測繪:Clark型電極(尖端25μm)以25μm步進掃描ABBA氧梯度(圖3A);
校準(zhǔn)方法:無氧(0.1M NaOH+抗壞血酸鈉)vs 空氣飽和LB溶液雙點校準(zhǔn);
關(guān)鍵數(shù)據(jù):
0-50μm溶解氧>80%空氣飽和度;
150-250μm降至<5%,確立缺氧/無氧邊界。
研究價值
微環(huán)境定量關(guān)聯(lián):
氧梯度數(shù)據(jù)與HCR成像空間匹配,證實ccoN1表達衰減與氧濃度下降同步(R2=0.92);
解釋ackA在深層激活的生理基礎(chǔ)(氧<2%時發(fā)酵途徑競爭優(yōu)勢)。
反硝化動力學(xué)驗證:
中層缺氧區(qū)(50-150μm)narG峰值與氧電極測量的臨界氧閾(5%-10%) 一致;
支持反硝化基因受Anr/Dnr轉(zhuǎn)錄因子級聯(lián)調(diào)控的模型(圖1)。

技術(shù)優(yōu)勢:
高空間分辨率:25μm步進精度捕獲聚集體邊緣-核心梯度;
實時動態(tài)監(jiān)測:秒級響應(yīng),避免固定樣本的氧擴散失真。
與傳統(tǒng)方法的對比
參數(shù) Unisense微電極 熒光蛋白報告基因
空間分辨率 25μm >100μm(擴散限制)
微環(huán)境影響 零干擾 可能改變細(xì)胞生理
多參數(shù)同步 氧+代謝成像共定位 僅限遺傳編碼目標(biāo)
適用模型 天然菌株/復(fù)雜樣本 依賴遺傳操作
應(yīng)用前景
臨床生物膜研究:解析感染病灶中病原體的代謝異質(zhì)性,指導(dǎo)靶向治療;
環(huán)境微生物學(xué):揭示土壤/水體生物膜的氮循環(huán)空間動力學(xué);
合成生物學(xué):優(yōu)化工程菌群的空間代謝分工設(shè)計。
突破性價值:通過Unisense電極的氧梯度定量與HCR空間轉(zhuǎn)錄組結(jié)合,首次在單細(xì)胞水平建立氧微環(huán)境-代謝基因表達的定量關(guān)聯(lián)模型,為生物膜耐藥機制研究提供方法論范式。