熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
Pharmacological Inhibition of Class III Alcohol Dehydrogenase 5: Turning Remote Ischemic Conditioning Effective in a Diabetic Stroke Model
III 類醇脫氫酶 5 的藥理學(xué)抑制:使遠(yuǎn)程缺血調(diào)理在糖尿病中風(fēng)模型中有效
來(lái)源:Antioxidants 2022, 11, 2051
摘要核心內(nèi)容
本研究針對(duì)糖尿病合并腦卒中患者中 遠(yuǎn)程缺血調(diào)節(jié)(RIC)療法失效 的臨床難題,提出 GSNOR抑制劑(GRI)聯(lián)合RIC 的創(chuàng)新策略:
核心發(fā)現(xiàn):
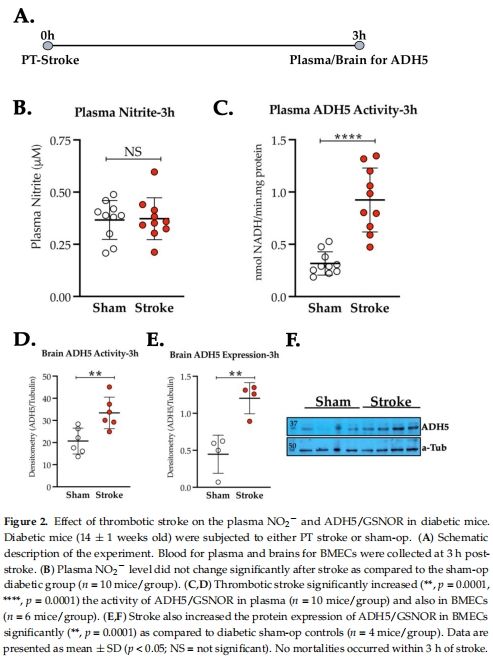
糖尿病卒中早期 GSNOR活性顯著升高(圖2B-E),加速S-亞硝基化(SNO)儲(chǔ)庫(kù)降解,導(dǎo)致RIC失效。
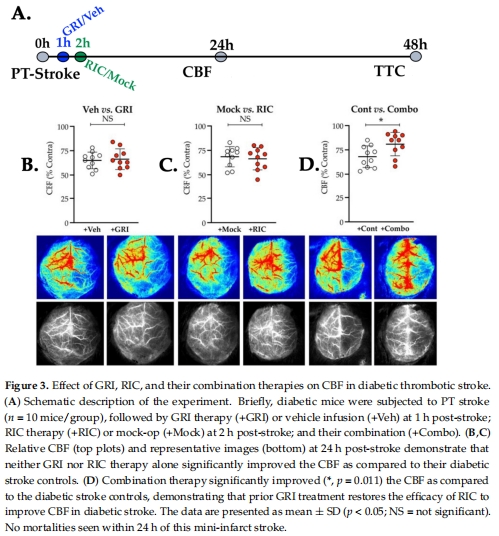
單獨(dú)使用RIC或GRI在糖尿病卒中模型中均無(wú)效(圖3-4),但 GRI預(yù)處理后聯(lián)合RIC 顯著提升腦血流(CBF)(圖3C)、減少梗死體積(圖4C)并改善神經(jīng)功能(圖5)。
機(jī)制解析:
RIC通過(guò)激活內(nèi)皮型一氧化氮合酶(eNOS/NOS3)增強(qiáng)SNO生成,但糖尿病導(dǎo)致 NOS3功能障礙 和 GSNOR活性上調(diào),中和RIC效應(yīng)。
GRI抑制GSNOR活性,保護(hù)SNO儲(chǔ)庫(kù)(如GSNO),恢復(fù)RIC的血管保護(hù)作用(圖7)。

臨床意義:
首次提出 "GRI-RIC聯(lián)合療法" 可克服糖尿病卒中患者的治療抵抗,為個(gè)體化卒中治療提供新方向。
研究目的
驗(yàn)證假說(shuō):
糖尿病合并卒中是否通過(guò)上調(diào)GSNOR活性導(dǎo)致RIC失效(圖2)。
GSNOR抑制劑(GRI)能否恢復(fù)RIC在糖尿病卒中中的保護(hù)作用(圖3-8)。
轉(zhuǎn)化目標(biāo):
解決RIC臨床中性結(jié)果的困境,為合并癥卒中患者提供有效治療方案。
研究思路與技術(shù)路線
采用 多模型驗(yàn)證+組合干預(yù) 策略:
動(dòng)物模型:
遺傳模型:NOS3+/-小鼠(模擬內(nèi)皮功能障礙,圖1)。
疾病模型:鏈脲佐菌素(STZ)誘導(dǎo)的糖尿病小鼠(圖2)。
卒中模型:
血栓性卒中:光化學(xué)血栓(PT)模型(圖1-5)。
再灌注卒中:短暫大腦中動(dòng)脈閉塞(tMCAO)模型(圖6-8)。
干預(yù)方案:
單藥治療:RIC(遠(yuǎn)程肢體缺血)或GRI(N6022,2.5 mg/kg)。
聯(lián)合治療:GRI預(yù)處理(卒中后1h)后行RIC(卒中后2h)。
檢測(cè)終點(diǎn):
急性期:CBF(激光散斑成像)、GSNOR活性(酶學(xué)法)、炎癥基因(qPCR)。
終末期:梗死體積(TTC染色)、神經(jīng)功能(轉(zhuǎn)棒/轉(zhuǎn)角試驗(yàn))、血腦屏障(伊文思藍(lán)滲出)。
關(guān)鍵數(shù)據(jù)及研究意義
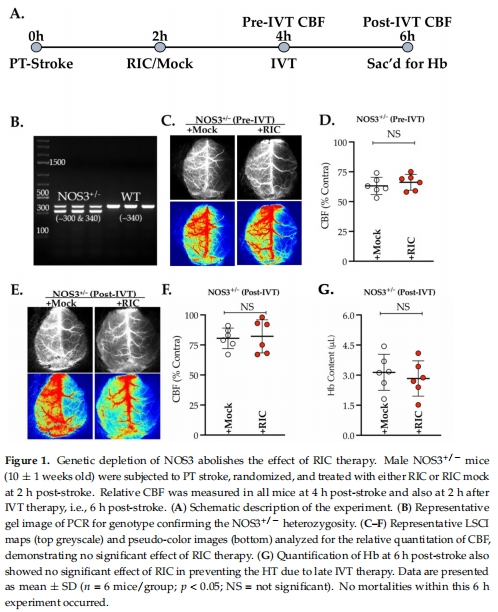
1. NOS3功能障礙消除RIC保護(hù)作用(圖1)
數(shù)據(jù):
NOS3+/-小鼠中,RIC未能改善CBF(圖1B-C)或減少溶栓后出血(圖1F)。
意義:首次證明 內(nèi)皮功能完整性 是RIC起效的必要條件,解釋臨床中性結(jié)果。
2. 糖尿病卒中早期GSNOR活性升高(圖2)
數(shù)據(jù):
卒中后3h,糖尿病小鼠血漿/腦微血管內(nèi)皮細(xì)胞(BMECs)中 GSNOR活性↑2倍(圖2B-C),蛋白表達(dá)同步增加(圖2D-E)。
血漿亞硝酸鹽(NO??)水平不變(圖2A),提示SNO儲(chǔ)庫(kù)(非NO??)是關(guān)鍵靶點(diǎn)。
意義:發(fā)現(xiàn)糖尿病卒中 早期生物標(biāo)志物(GSNOR),為治療時(shí)間窗提供依據(jù)。
3. GRI-RIC協(xié)同改善腦血流與預(yù)后(圖3-5)
數(shù)據(jù):
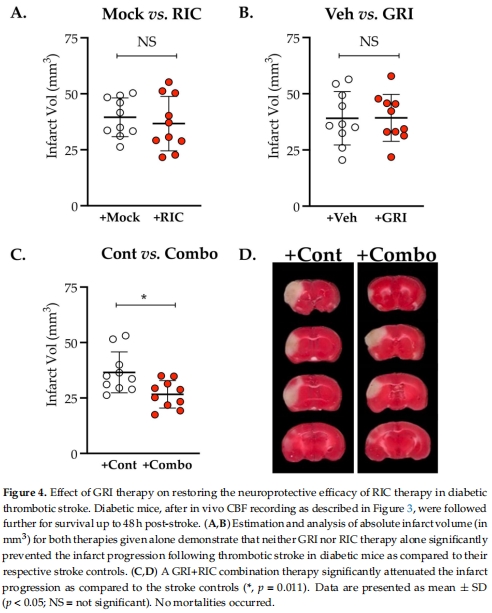
單藥無(wú)效:GRI或RIC單獨(dú)使用對(duì)CBF無(wú)改善(圖3B)、梗死體積無(wú)減少(圖4A-B)。
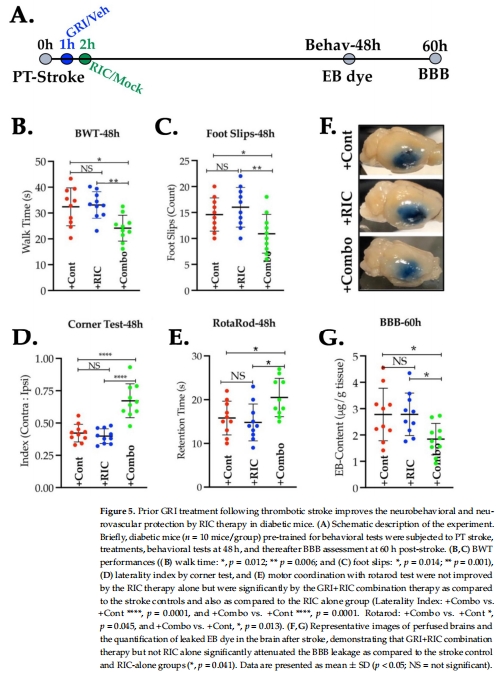
聯(lián)合有效:GRI+RIC提升CBF 40%(圖3C)、減少梗死30%(圖4C)、改善運(yùn)動(dòng)功能(圖5B-D)。
意義:確立 "GSNOR抑制+RIC" 的協(xié)同機(jī)制,突破糖尿病卒中治療瓶頸。
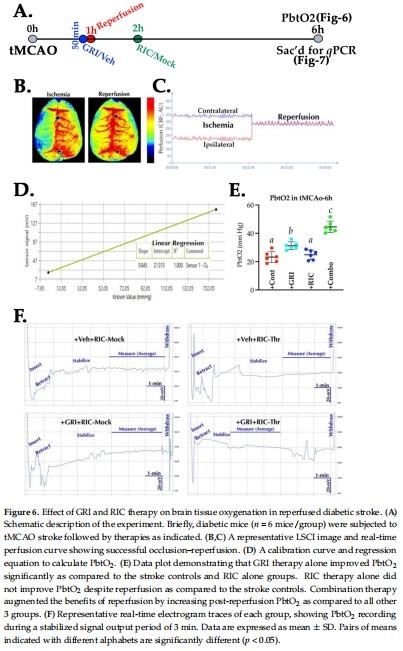
4. Unisense電極直接驗(yàn)證腦組織氧合恢復(fù)(圖6)
數(shù)據(jù):
技術(shù)原理:Unisense極譜微電極(尖端50μm)實(shí)時(shí)監(jiān)測(cè)腦組織氧分壓(PbtO?)(方法2.13)。
關(guān)鍵發(fā)現(xiàn):
GRI單藥提升tMCAO模型早期PbtO?(圖6E,*p=0.01)。
GRI+RIC聯(lián)合進(jìn)一步顯著增強(qiáng)PbtO?(p=0.0001),證實(shí) 微循環(huán)再灌注成功(圖6E-F)。
研究意義:
直接證據(jù):首次在體證明聯(lián)合療法改善深部腦組織氧合,克服間接指標(biāo)(如CBF)的局限性。
技術(shù)優(yōu)勢(shì):高時(shí)空分辨率(60Hz采樣)捕捉動(dòng)態(tài)氧合變化,為再灌注療效提供金標(biāo)準(zhǔn)。
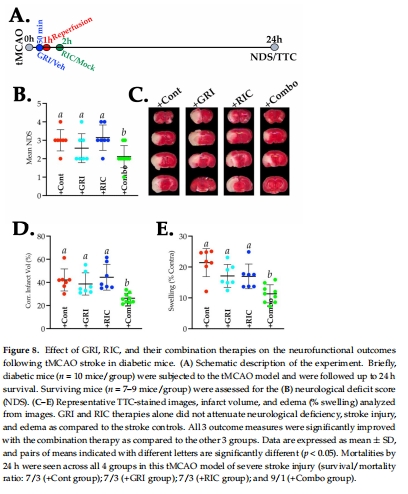
5. 聯(lián)合療法抑制炎癥并保護(hù)血腦屏障(圖7-8)
數(shù)據(jù):
RIC單藥 意外升高炎癥因子(IL-6、iNOS等),而GRI+RIC聯(lián)合顯著抑制(圖7)。
聯(lián)合療法減少腦水腫(圖8D)和伊文思藍(lán)滲出(圖5F-G),證實(shí) 血腦屏障保護(hù)。
意義:揭示GRI通過(guò) 抑制GSNOR-SNO失衡 阻斷炎癥級(jí)聯(lián),協(xié)同RIC實(shí)現(xiàn)神經(jīng)血管保護(hù)。
核心結(jié)論
糖尿病卒中早期事件:GSNOR活性快速升高,降解SNO儲(chǔ)庫(kù),導(dǎo)致RIC失效。
協(xié)同機(jī)制:GRI抑制GSNOR,保護(hù)內(nèi)源性SNO(如GSNO),恢復(fù)RIC的eNOS激活能力。
治療突破:GRI-RIC聯(lián)合方案在糖尿病模型中顯著改善CBF、PbtO?及神經(jīng)功能,為臨床轉(zhuǎn)化提供依據(jù)。
研究啟示
機(jī)制創(chuàng)新:
提出 "GSNOR-SNO軸" 作為糖尿病卒中治療新靶點(diǎn)。
闡明RIC失效的分子基礎(chǔ)(GSNOR活性上調(diào))。
臨床轉(zhuǎn)化:
個(gè)體化治療:合并糖尿病卒中患者需聯(lián)合GSNOR抑制劑以恢復(fù)RIC療效。
療效監(jiān)測(cè):GSNOR活性或SNO水平可作為治療反應(yīng)生物標(biāo)志物。
技術(shù)亮點(diǎn):
Unisense電極的應(yīng)用:提供 腦組織氧合直接證據(jù),優(yōu)于間接血流指標(biāo),為療效評(píng)估提供高置信度數(shù)據(jù)。