熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Fluorinated Hyaluronic Acid Encapsulated Perfluorocarbon Nanoparticles as Tumor-Targeted Oxygen Carriers to Enhance Radiotherapy
氟化透明質(zhì)酸封裝的全氟化碳納米顆粒作為腫瘤靶向氧載體以增強放射治療
來源: Mol. Pharmaceutics 2022, 19, 3948?3958
一、摘要概述
論文開發(fā)了一種基于氟化透明質(zhì)酸(FHA)包裹全氟化碳(PFC)的納米氧載體(O?@PFC@FHA NPs),用于靶向緩解腫瘤缺氧并增強放療療效:
核心設(shè)計:
通過氟化修飾的透明質(zhì)酸(FHA)封裝O?飽和的全氟化碳(PFC),形成納米顆粒(~195 nm)。
FHA通過CD44受體介導(dǎo)的靶向作用增強腫瘤蓄積(圖1)。
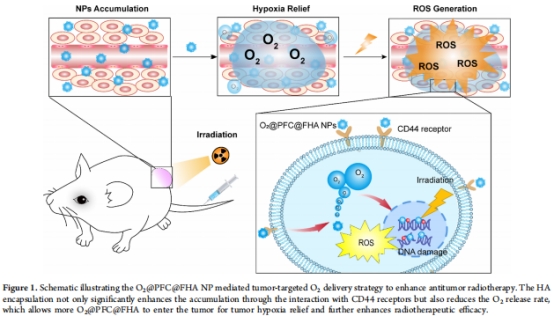
關(guān)鍵效果:
緩釋氧氣:FHA封裝使O?釋放時間延長至60分鐘以上(vs 普通PFC的20分鐘),顯著緩解腫瘤缺氧(HIF-1α表達(dá)降低50%)。
放療增敏:聯(lián)合放療使腫瘤抑制率提升近3倍(vs 單獨放療),且無系統(tǒng)毒性。
臨床意義:所有組分(HA、PFC)均臨床可用,具轉(zhuǎn)化潛力。
二、研究目的
解決腫瘤缺氧導(dǎo)致的放療抵抗問題:
傳統(tǒng)方法局限:
高壓氧艙操作復(fù)雜且易致氧中毒;普通PFC乳劑需聯(lián)合高氧呼吸,引發(fā)全身氧化應(yīng)激。
現(xiàn)有納米氧載體(如MnO?)依賴腫瘤內(nèi)源性H?O?,效率受限且金屬離子殘留致毒。
本研究目標(biāo):開發(fā)安全、靶向的氧遞送系統(tǒng),通過CD44靶向和緩釋特性實現(xiàn)局部缺氧緩解,避免全身毒性。
三、研究思路
納米載體構(gòu)建(圖2a):
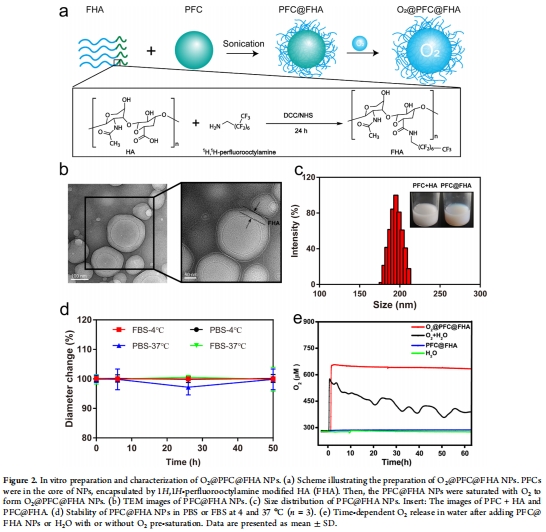
合成氟化透明質(zhì)酸(FHA):HA與1H,1H-全氟辛胺偶聯(lián)(1?F NMR驗證)。
乳化法制備PFC@FHA NPs:超聲乳化PFC與FHA,形成核殼結(jié)構(gòu)(PFC核 + FHA殼)。
氧飽和處理:純氧飽和得O?@PFC@FHA NPs。
體外驗證(圖3):
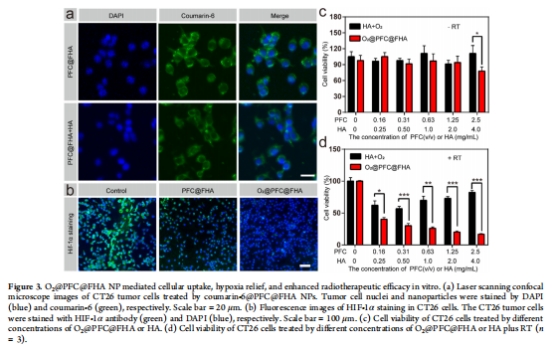
靶向性:共聚焦顯微鏡顯示CT26細(xì)胞通過CD44介導(dǎo)內(nèi)吞攝取NPs(競爭抑制后攝取減少)。
缺氧緩解:O?@PFC@FHA處理使HIF-1α表達(dá)降低(圖3b)。
放療增敏:聯(lián)合放療(5 Gy)使細(xì)胞存活率降至20%(vs 單獨放療的80%)。
體內(nèi)評估(圖4-6):
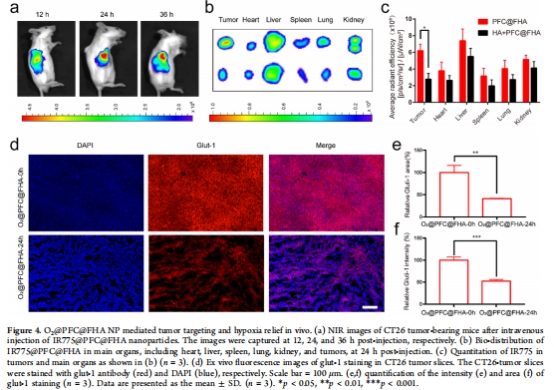
靶向蓄積:近紅外成像(IR775標(biāo)記)顯示腫瘤內(nèi)NPs富集(24小時峰值),競爭抑制證實CD44依賴(圖4a-c)。
缺氧緩解:Glut-1免疫熒光顯示腫瘤缺氧區(qū)域減少(圖4d-f)。
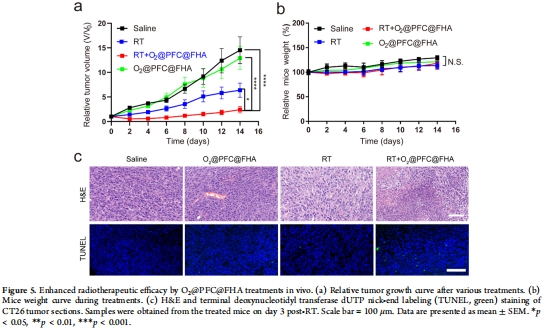
療效與安全:聯(lián)合放療顯著抑制腫瘤生長(圖5a),H&E和血清生化證實無肝腎毒性(圖6)。
四、測量的數(shù)據(jù)及其研究意義
1. 納米載體特性
數(shù)據(jù)來源:圖2b-e(形態(tài)、尺寸、穩(wěn)定性、氧釋放)。
關(guān)鍵結(jié)果:
尺寸:~195 nm(DLS/TEM);
穩(wěn)定性:50小時內(nèi)尺寸穩(wěn)定(PBS/FBS中);
氧緩釋:O?濃度>650 μM,緩釋>60分鐘(普通PFC僅20分鐘)。
研究意義:
緩釋設(shè)計價值:延長O?作用時間,減少全身暴露風(fēng)險,增加腫瘤遞送效率(圖2e)。
臨床適配性:尺寸適中(<200 nm)利于腫瘤EPR效應(yīng)蓄積。
2. 體外靶向與缺氧緩解
數(shù)據(jù)來源:圖3a-b(細(xì)胞攝取、HIF-1α表達(dá))。
關(guān)鍵結(jié)果:
細(xì)胞攝取:競爭抑制(HA預(yù)孵育)使熒光強度降低50%;
HIF-1α:O?@PFC@FHA處理組表達(dá)量降至對照組1/2。
研究意義:
靶向機制:證實CD44受體介導(dǎo)的主動靶向(圖3a)。
功能驗證:納米載體直接緩解細(xì)胞缺氧,為放療增敏奠定基礎(chǔ)。
3. 放療增敏機制
數(shù)據(jù)來源:圖3d(細(xì)胞存活率)、ROS生成。
關(guān)鍵結(jié)果:
細(xì)胞存活:RT + O?@PFC@FHA組存活率20% vs RT組80%(圖3d);
ROS水平:聯(lián)合治療組ROS增加2倍。
研究意義:
氧增強比:局部供氧提升輻射誘導(dǎo)的ROS生成,增強DNA損傷。
協(xié)同機制:克服缺氧相關(guān)放療抵抗的核心途徑。
4. 體內(nèi)靶向與療效
數(shù)據(jù)來源:圖4a-c(體內(nèi)分布)、圖5a-c(抑瘤效果)。
關(guān)鍵結(jié)果:
腫瘤蓄積:24小時腫瘤熒光強度達(dá)峰值(競爭抑制后降低60%);
抑瘤率:RT + O?@PFC@FHA組腫瘤體積抑制率85%(vs RT組30%)。
研究意義:
靶向效率:CD44靶向提升腫瘤藥物遞送效率(圖4c)。
治療突破:首次實現(xiàn)無高氧呼吸的腫瘤靶向氧療,克服傳統(tǒng)毒性。
5. 生物安全性
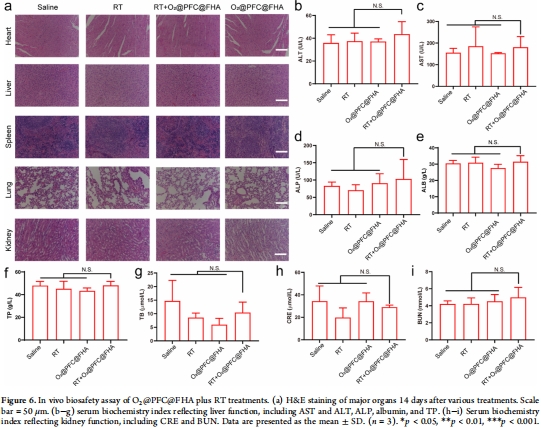
數(shù)據(jù)來源:圖6(H&E染色、血清生化)。
關(guān)鍵結(jié)果:
器官病理:心肝脾肺腎無損傷(H&E);
血清指標(biāo):ALT/AST/BUN等均正常(圖6b-i)。
研究意義:
臨床安全性:成分(HA、PFC)均FDA批準(zhǔn),支持臨床轉(zhuǎn)化。
五、結(jié)論
核心創(chuàng)新:
首創(chuàng)FHA封裝PFC的靶向氧載體,實現(xiàn)緩釋、腫瘤特異性遞送。
突破傳統(tǒng)氧載體需聯(lián)合高氧呼吸的限制,避免全身氧化損傷。
療效驗證:
顯著緩解腫瘤缺氧(Glut-1/HIF-1α下調(diào)),放療抑瘤率提升3倍。
全組分臨床可應(yīng)用,具備快速轉(zhuǎn)化潛力。
六、丹麥Unisense電極數(shù)據(jù)的詳細(xì)解讀
1. 測量方法與數(shù)據(jù)位置
技術(shù)原理:
使用Unisense OX25氧電極(Clark微傳感器),通過電化學(xué)法實時檢測溶解氧濃度。
測量條件:缺氧環(huán)境(1% O?),模擬腫瘤微環(huán)境。
數(shù)據(jù)來源:圖2e(主)、圖S2(補充對比)。
2. 關(guān)鍵結(jié)果與機制意義
結(jié)果(圖2e):
O?@PFC@FHA NPs在60分鐘內(nèi)維持O?濃度>400 μM,而普通PFC在20分鐘內(nèi)降至基線。
初始O?濃度:650 μM(vs 飽和水的300 μM)。
機制解讀:
緩釋設(shè)計:FHA外殼延緩O?擴散,延長作用時間(圖2e)。
腫瘤遞送優(yōu)勢:緩慢釋放使更多NPs能深入缺氧腫瘤核心(傳統(tǒng)PFC過早釋氧,無法抵達(dá)深部)。
3. 研究意義
技術(shù)價值:
精準(zhǔn)量化:Unisense電極提供高時空分辨率氧分布數(shù)據(jù),是納米載體氧動力學(xué)研究的金標(biāo)準(zhǔn)。
臨床前預(yù)測:緩釋曲線(>60分鐘)匹配腫瘤血管滲透時間(~30分鐘),預(yù)示體內(nèi)有效性。
領(lǐng)域貢獻:
為"無高氧呼吸的靶向氧療"提供直接證據(jù),解決領(lǐng)域核心瓶頸(全身毒性問題)。
確立緩釋特性為氧載體設(shè)計關(guān)鍵參數(shù),推動下一代納米氧載體開發(fā)。