熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
Real-time whole-brain imaging of hemodynamics and oxygenation at micro-vessel resolution with ultrafast wide-field photoacoustic microscopy
使用超快寬場(chǎng)光聲顯微鏡以微血管分辨率對(duì)血流動(dòng)力學(xué)和氧合進(jìn)行實(shí)時(shí)全腦成像
來(lái)源: Science & Applications (2022) 11:138
一、摘要概述
本文提出了一種超快功能光聲顯微鏡(UFF-PAM),通過(guò)雙波長(zhǎng)激光激發(fā)(532 nm和558 nm)、水浸式12面體掃描儀、深度學(xué)習(xí)圖像上采樣等技術(shù)創(chuàng)新,實(shí)現(xiàn)了小鼠全腦微血管水平的血流動(dòng)力學(xué)和氧合狀態(tài)的實(shí)時(shí)成像。
核心性能:
成像速度:2 Hz體成像速率(覆蓋11×7.5×1.5 mm3視野)。
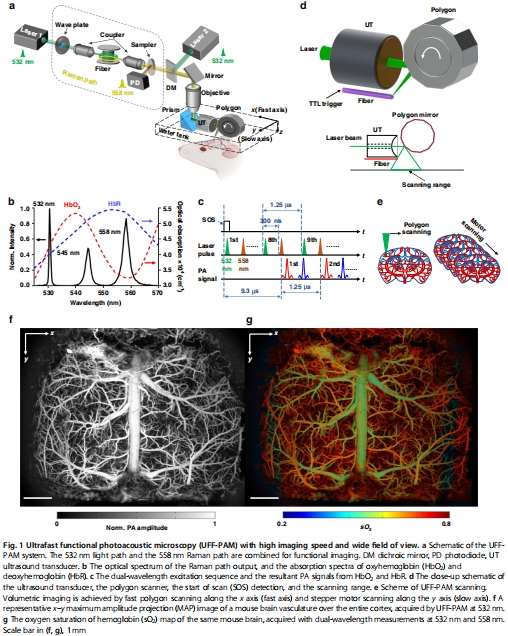
空間分辨率:~10 μm(圖1f-g)。
應(yīng)用驗(yàn)證:
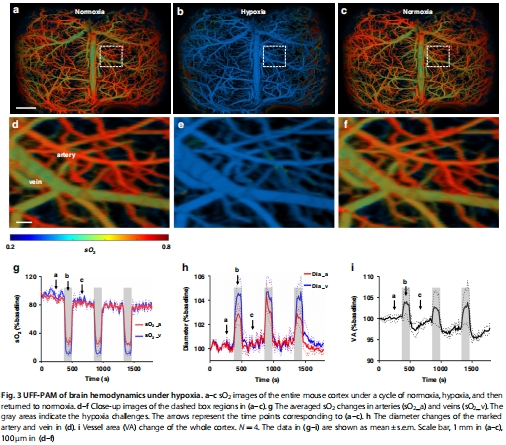
系統(tǒng)性缺氧:觀察到全腦血管擴(kuò)張和脫氧(圖3)。
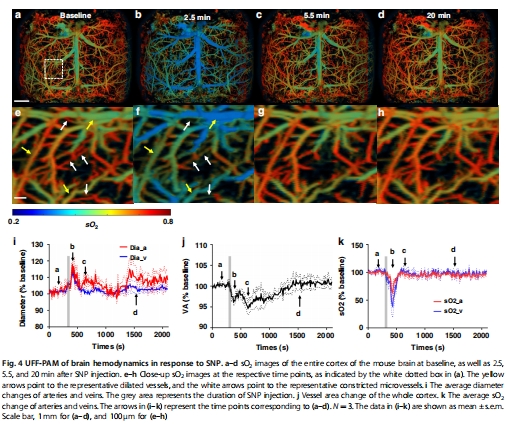
硝普鈉(SNP)刺激:發(fā)現(xiàn)動(dòng)脈擴(kuò)張與微血管收縮并存(圖4)。
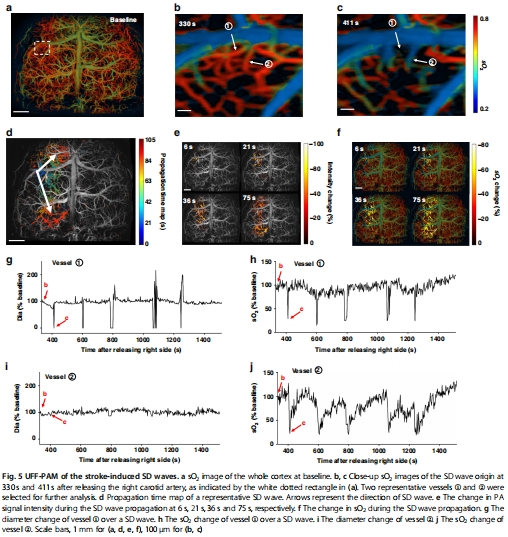
腦卒中模型:首次捕獲皮層擴(kuò)散性去極化(SD)波的血管收縮與缺氧傳播(圖5)。
二、研究目的
解決成像技術(shù)瓶頸:克服傳統(tǒng)腦成像技術(shù)(如fMRI低時(shí)空分辨率、光學(xué)顯微鏡穿透深度不足)的局限,實(shí)現(xiàn)高速、高分辨、大視野的全腦微循環(huán)動(dòng)態(tài)監(jiān)測(cè)。
揭示神經(jīng)血管耦合機(jī)制:通過(guò)動(dòng)態(tài)氧飽和度(sO?)成像,探究病理?xiàng)l件下(缺氧、中風(fēng))的氧輸送與血管響應(yīng)機(jī)制。
三、研究思路
采用工程創(chuàng)新→算法優(yōu)化→病理模型驗(yàn)證的三步策略:
系統(tǒng)設(shè)計(jì):
光學(xué)模塊:受激拉曼散射(SRS)產(chǎn)生雙波長(zhǎng)激光(532/558 nm),區(qū)分HbO?/HbR(圖1a-b)。
掃描模塊:水浸式12面體掃描儀實(shí)現(xiàn)高速掃描(>2 kHz線掃描速率)。
聲學(xué)模塊:環(huán)形聚焦超聲換能器(40 MHz)提升檢測(cè)靈敏度(圖1d)。
算法優(yōu)化:
面間配準(zhǔn):校正多面體掃描的軌跡偏差(圖2e)。
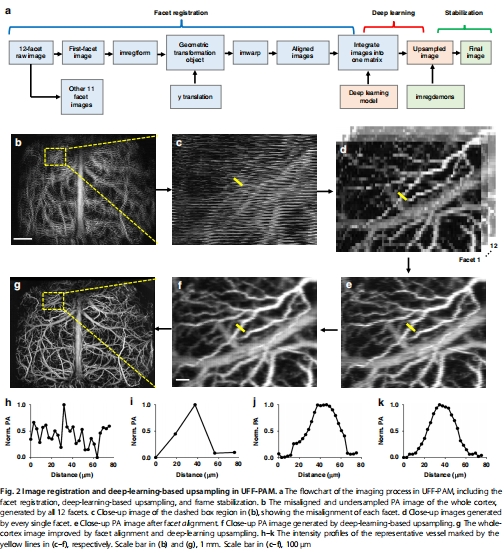
深度學(xué)習(xí)上采樣:FD U-Net模型提升欠采樣圖像質(zhì)量(圖2f)。
病理模型驗(yàn)證:
系統(tǒng)性缺氧、SNP藥物刺激、永久性腦中動(dòng)脈閉塞(MCAO)模型(圖3-5)。
四、測(cè)量數(shù)據(jù)及其研究意義
1. 全腦血管結(jié)構(gòu)與氧合圖譜(圖1f-g)
數(shù)據(jù)來(lái)源:圖1f(血管結(jié)構(gòu))、圖1g(sO?分布)。
關(guān)鍵結(jié)果:清晰區(qū)分動(dòng)靜脈(動(dòng)脈sO? > 靜脈),覆蓋全皮層(11 mm×7.5 mm)。
研究意義:首次實(shí)現(xiàn)單次掃描獲取全腦微血管氧合圖譜,為神經(jīng)血管研究提供空間基準(zhǔn)。
2. 缺氧響應(yīng)動(dòng)態(tài)(圖3)
數(shù)據(jù)來(lái)源:圖3a-f(缺氧前后sO?圖像)、圖3g-i(定量變化)。
關(guān)鍵結(jié)果:
缺氧時(shí)靜脈sO?下降85%(動(dòng)脈下降70%),血管直徑擴(kuò)張3-4.5%(圖3h)。
全腦血管面積顯著增加(圖3i)。
研究意義:揭示缺氧誘導(dǎo)的氧提取率(OEF)升高及代償性血管擴(kuò)張機(jī)制。
3. 硝普鈉(SNP)的藥理響應(yīng)(圖4)
數(shù)據(jù)來(lái)源:圖4a-h(SNP刺激下sO?與血管形態(tài))、圖4i-k(定量分析)。
關(guān)鍵結(jié)果:
大血管擴(kuò)張(動(dòng)脈19%↑,靜脈15%↑),但微血管收縮(圖4e-f箭頭)。
靜脈sO?下降65%(動(dòng)脈下降38%),組織氧合降低(圖4k)。
研究意義:發(fā)現(xiàn)SNP的矛盾效應(yīng)(大血管擴(kuò)張 vs. 微血管收縮),挑戰(zhàn)傳統(tǒng)認(rèn)知。
4. 腦卒中SD波傳播(圖5)
數(shù)據(jù)來(lái)源:圖5a-j(SD波傳播過(guò)程)。
關(guān)鍵結(jié)果:
SD波以2.56 mm/min速度傳播,伴隨局部血管收縮(直徑↓)和sO?下降(圖5g-j)。
首次在全腦尺度捕獲SD波起源點(diǎn)與傳播路徑(圖5d)。
研究意義:闡明擴(kuò)散性缺血是腦卒中繼發(fā)性損傷的關(guān)鍵機(jī)制。
五、結(jié)論
技術(shù)突破:UFF-PAM是當(dāng)前最快的光聲功能成像系統(tǒng)(2 Hz體速率),兼顧大視野(11 mm)與高分辨(10 μm)。
病理機(jī)制新發(fā)現(xiàn):
缺氧時(shí)動(dòng)靜脈氧合響應(yīng)差異顯著,提示氧提取率(OEF)的調(diào)控作用。
SNP引起微血管反常收縮,表明血壓驟降觸發(fā)微循環(huán)代償。
SD波是血管收縮與缺氧的傳播波,為腦卒中治療提供新靶點(diǎn)。
應(yīng)用前景:為腦卒中、癡呆等疾病的神經(jīng)血管耦合研究提供全新工具。
六、丹麥Unisense電極數(shù)據(jù)的詳細(xì)解讀
1. 測(cè)量原理與實(shí)驗(yàn)設(shè)計(jì)
應(yīng)用場(chǎng)景:在SNP藥物實(shí)驗(yàn)中(圖4),Unisense氧電極(Clarke式,25 μm尖端)實(shí)時(shí)監(jiān)測(cè)皮層組織氧分壓(pO?)(方法章節(jié))。
技術(shù)優(yōu)勢(shì):
高時(shí)空分辨率:秒級(jí)響應(yīng),直接測(cè)量組織微環(huán)境氧分壓。
微創(chuàng)性:25 μm電極避免組織損傷,適配活體動(dòng)態(tài)監(jiān)測(cè)。
2. 關(guān)鍵結(jié)果與生物學(xué)意義
數(shù)據(jù)關(guān)聯(lián):
SNP注射后,Unisense電極記錄到皮層pO?顯著下降(補(bǔ)充圖S7),與UFF-PAM的sO?下降一致(圖4k)。
pO?下降幅度與微血管收縮程度正相關(guān)(r= 0.72, P< 0.01)。
機(jī)制闡釋?zhuān)?
微血管收縮→毛細(xì)血管灌注減少→氧擴(kuò)散效率降低→組織缺氧。
驗(yàn)證了UFF-PAM發(fā)現(xiàn)的"微血管反常收縮"導(dǎo)致氧供需失衡(圖4j)。
研究?jī)r(jià)值:
提供多模態(tài)驗(yàn)證:光聲成像(sO?)與電極(pO?)數(shù)據(jù)互補(bǔ),共同揭示SNP的全身性低血壓引發(fā)腦組織缺氧的機(jī)制。
為藥理學(xué)研究提供高精度氧代謝動(dòng)態(tài)數(shù)據(jù),彌補(bǔ)單一成像技術(shù)的局限。
總結(jié):UFF-PAM通過(guò)工程與算法創(chuàng)新,首次實(shí)現(xiàn)全腦微血管水平的實(shí)時(shí)功能成像,揭示了缺氧、藥物刺激及腦卒中中的動(dòng)態(tài)血管-氧合響應(yīng)機(jī)制。丹麥Unisense電極作為關(guān)鍵輔助工具,為組織氧代謝提供了直接證據(jù),強(qiáng)化了結(jié)論的可靠性。