熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
Electron Transfer to the Trinuclear Copper Cluster in Electrocatalysis by the Multicopper Oxidases
多銅氧化酶電催化中電子向三核銅簇的轉(zhuǎn)移機(jī)制
來源:J. Am. Chem. Soc. 2021, 143(41), 17236-17249
《美國(guó)化學(xué)會(huì)志》2021年 第143卷 第41期17236-17249頁
摘要內(nèi)容
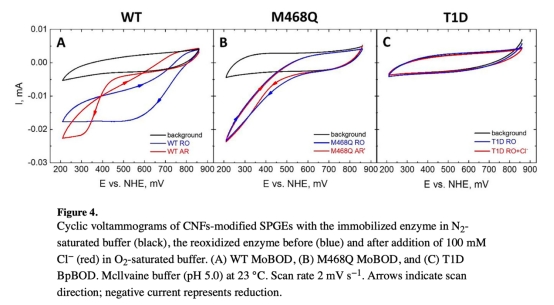
高電位多銅氧化酶(MCOs)是優(yōu)異的氧還原反應(yīng)(ORR)催化劑,但其電催化機(jī)制存在爭(zhēng)議:電子傳遞是通過I型銅(T1)位點(diǎn)還是直接轉(zhuǎn)移至三核銅簇(TNC)。本研究通過位點(diǎn)定向突變(M468Q MoBOD和T1D BpBOD)結(jié)合電化學(xué)測(cè)試和動(dòng)力學(xué)建模,揭示T1位點(diǎn)是主要電子受體(圖4A-B)。TNC的高重組能(1.5 eV)阻礙直接電子傳遞,但"替代靜息態(tài)"(AR, Cl?誘導(dǎo))因重組能降低(0.75 eV)可實(shí)現(xiàn)首輪直接電子傳遞(圖4A-B紅曲線)。Unisense氧電極證實(shí)T1突變體均相催化活性喪失,支持電化學(xué)結(jié)論。
研究目的
闡明MCOs電催化ORR中電子傳遞路徑(T1 vs. TNC),解析TNC氧化態(tài)與重組能對(duì)電子轉(zhuǎn)移的影響,指導(dǎo)高效生物陰極設(shè)計(jì)。
研究思路
1. 酶突變體設(shè)計(jì):構(gòu)建T1軸向配體突變(M468Q)和T1缺失突變體(T1D),保持TNC結(jié)構(gòu)完整(圖1 EPR/UV-Vis驗(yàn)證);
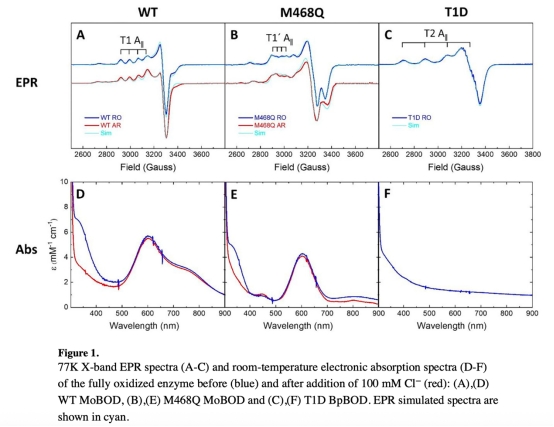
2. 溶液相表征:
? EPR/UV-Vis分析銅位點(diǎn)狀態(tài)(圖1);
? 停流光譜測(cè)O?反應(yīng)動(dòng)力學(xué)(圖2-3);
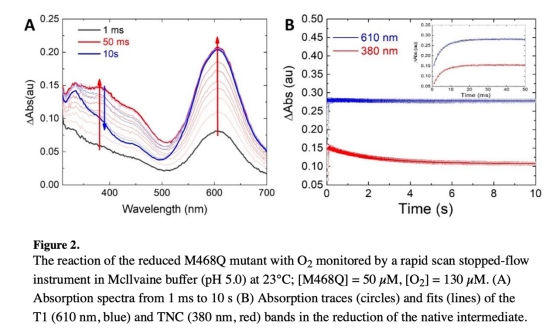
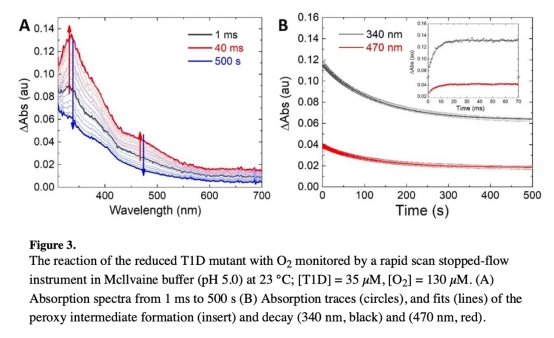
? Unisense氧電極測(cè)均相催化活性;
3. 電化學(xué)測(cè)試:
? 碳糊電極測(cè)循環(huán)伏安(CV)和線性掃描伏安(LSV)(圖4-5);
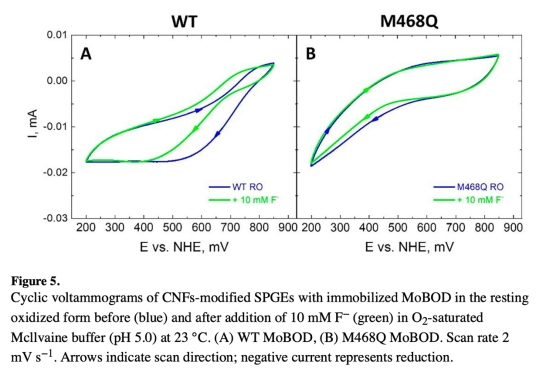
? 氟/氯離子抑制效應(yīng)(圖4-5);
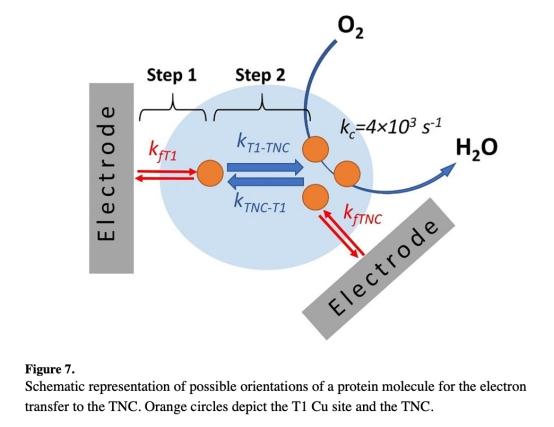
4. 動(dòng)力學(xué)建模:結(jié)合Marcus理論構(gòu)建電子傳遞模型(圖6-7),擬合實(shí)驗(yàn)數(shù)據(jù)。

測(cè)量數(shù)據(jù)及其研究意義
1. 突變體催化活性數(shù)據(jù)
? 測(cè)量?jī)?nèi)容:T1D突變體均相ORR活性完全喪失(Clark電極測(cè)O?消耗)。
? 研究意義:證實(shí)T1位點(diǎn)是溶液相催化必需的電子傳遞通道。
2. 電催化起始電位數(shù)據(jù)(圖4A-B, 5)
? 測(cè)量?jī)?nèi)容:
? WT起始電位800 mV vs. NHE,M468Q降至610 mV(T1電位降低);
? Cl?處理后二者起始電位均降至460 mV(AR態(tài)TNC直接電子傳遞)。
? 研究意義:電位偏移揭示TNC在AR態(tài)可成為首輪電子受體。
3. 計(jì)時(shí)電流數(shù)據(jù)
? 測(cè)量?jī)?nèi)容:AR態(tài)酶在過電位區(qū)間(710-610 mV)無電流累積。
? 研究意義:排除T1間接還原AR-TNC路徑,支持直接電子傳遞。
4. LSV擬合參數(shù)(表3-4)
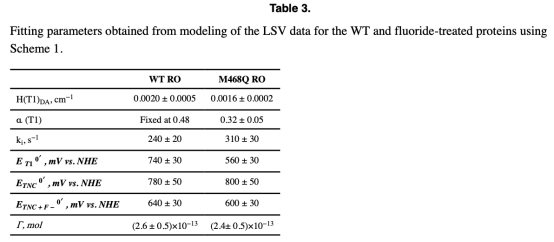
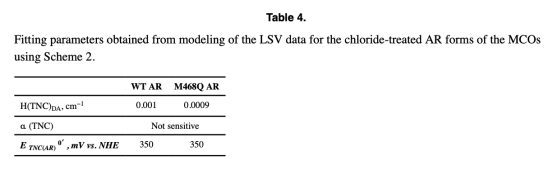
? 測(cè)量?jī)?nèi)容:T1/電極耦合常數(shù)H(DA)~0.002 cm?1,TNC/電極~0.001 cm?1。
? 研究意義:電子耦合強(qiáng)度相似,但TNC高重組能(1.5 eV)致其直接電子傳遞速率比T1路徑低10?倍(圖7)。
結(jié)論
1. 電子傳遞路徑:T1是主要電子入口,因TNC高重組能(1.5 eV)阻礙直接電子傳遞(T1D突變體無催化活性);
2. AR態(tài)作用:Cl?誘導(dǎo)的AR態(tài)(重組能0.75 eV)可實(shí)現(xiàn)首輪直接電子傳遞至TNC(圖6B),但后續(xù)輪次仍經(jīng)T1位點(diǎn);
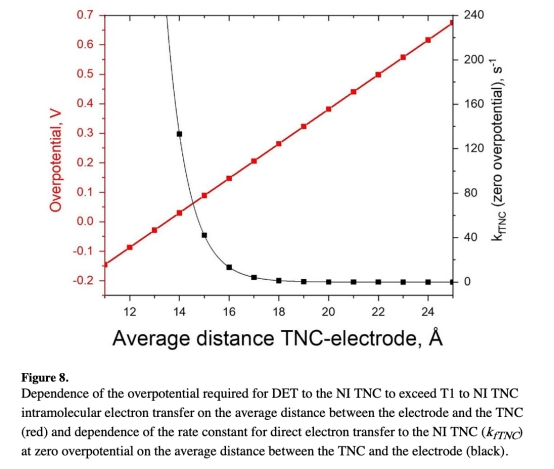
3. 生物陰極設(shè)計(jì):定向固定酶使TNC平均距離電極<19 ?可降低過電位>300 mV(圖8),突破T1-TNC電子傳遞瓶頸。
丹麥Unisense電極測(cè)量意義
研究中采用Unisense Clark氧電極(實(shí)驗(yàn)方法)監(jiān)測(cè)溶液相酶催化O?消耗動(dòng)力學(xué),其核心價(jià)值在于:
? 克服氣相檢測(cè)局限:直接測(cè)量溶解氧濃度(0.1 M H?SO?, pH 5.0),避免傳統(tǒng)頂空氣相色譜(GC)因O?溶解度變化導(dǎo)致的定量誤差;
? 高時(shí)間分辨率:秒級(jí)監(jiān)測(cè)捕捉突變體反應(yīng)初期動(dòng)力學(xué),證實(shí)T1D無催化活性(對(duì)比圖2-3停流光譜的毫秒級(jí)數(shù)據(jù));
? 驗(yàn)證催化機(jī)制:通過O?消耗與電子轉(zhuǎn)移的定量關(guān)聯(lián)(TON計(jì)算),支持電化學(xué)結(jié)論——T1位點(diǎn)是溶液相催化必經(jīng)途徑。
該技術(shù)為酶催化動(dòng)力學(xué)研究提供了原位、高靈敏的氧定量方案,尤其適用于低通量快速反應(yīng)體系。