熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Hydrogen improves cell viability partly through inhibition of autophagy and activation of PI3K/Akt/GSK3β signal pathway in a microvascular endothelial cell model of traumatic brain injury
在創傷性腦損傷的微血管內皮細胞模型中,氫氣部分通過抑制自噬和激活 PI3K Akt GSK3β 信號通路來提高細胞活力
來源:NEUROLOGICAL RESEARCH 2020, VOL. 42, NO. 6, 487–496
1. 論文摘要核心內容
研究通過建立腦微血管內皮細胞(bEnd.3)劃痕損傷模型模擬TBI,探究氫氣(H?)的保護機制。核心發現:
氫氣顯著提升TBI后細胞活力(MTT檢測),并激活PI3K/Akt/GSK3β信號通路(Western blot驗證)。
氫氣抑制自噬激活(降低LC3-II/I、Beclin-1表達),而自噬誘導劑雷帕霉素(Rapamycin)可逆轉氫氣的保護作用。
PI3K抑制劑(LY294002)阻斷氫氣效應,證實PI3K/Akt/GSK3β通路是氫氣抑制自噬的關鍵上游機制。
結論:氫氣通過激活PI3K/Akt/GSK3β通路抑制自噬,改善TBI后內皮細胞存活,為氫氣治療TBI提供新機制依據。
2. 研究目的
闡明氫氣減輕TBI后血腦屏障(BBB)損傷的分子機制。
驗證氫氣是否通過調控PI3K/Akt/GSK3β信號通路和自噬發揮保護作用。
探索氫氣治療TBI的潛在臨床應用價值。
3. 研究思路
1.模型建立:
采用小鼠腦微血管內皮細胞(bEnd.3)建立劃痕損傷模型(模擬TBI機械損傷)。
分組:假手術組(Sham)、假手術+氫氣組(Sham+H?)、TBI組、TBI+氫氣組(TBI+H?)、TBI+氫氣+PI3K抑制劑組(TBI+H?+LY)、TBI+氫氣+自噬誘導劑組(TBI+H?+Rap)。
2.干預設計:
氫氣干預:使用富氫培養基(0.60 ± 0.03 mM,Unisense電極標定)。
通路調控:PI3K抑制劑(LY294002)和自噬誘導劑(雷帕霉素)。
3.檢測指標:
細胞形態與活力:劃痕愈合率(圖1)、MTT細胞活力(圖2a, 4a, 6a)。
信號通路蛋白:p-Akt、p-GSK3β(Western blot,圖2b-d, 4b-d, 6b-d)。
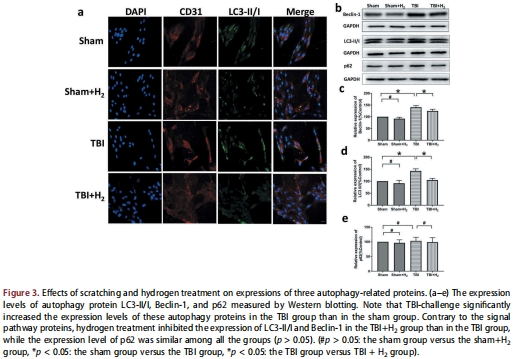
自噬標志物:LC3-II/I、Beclin-1、p62(Western blot/免疫熒光,圖3, 5, 7)。
4. 關鍵數據及研究意義
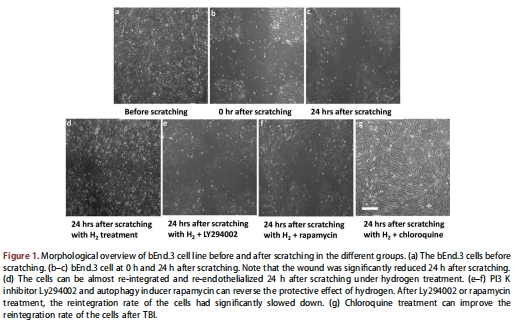
(1) 氫氣促進細胞修復(圖1)
數據:劃痕后24小時,TBI+H?組細胞再內皮化程度顯著高于TBI組(圖1d),而PI3K抑制劑(LY294002)或自噬誘導劑(Rap)削弱該效應(圖1e-f)。
意義:氫氣通過促進內皮細胞修復減輕BBB損傷,且依賴PI3K通路和自噬抑制。
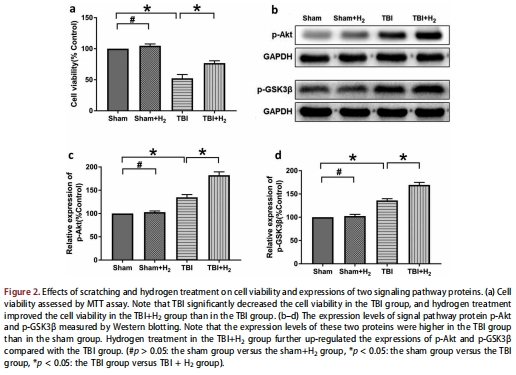
(2) 氫氣提升細胞活力(圖2a, 4a, 6a)
數據:
TBI組細胞活力顯著下降(vs Sham組),氫氣干預后活力恢復(圖2a)。
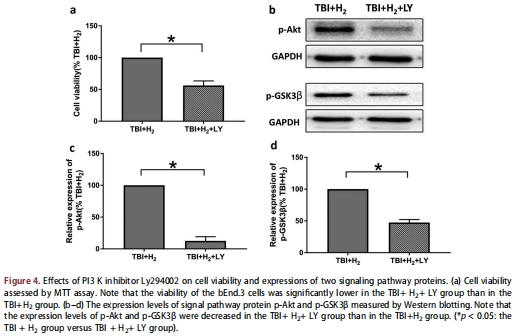
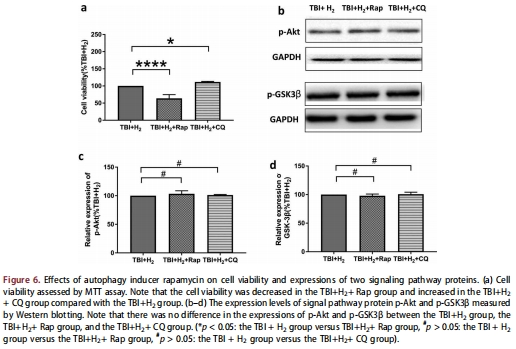
LY294002或雷帕霉素處理取消氫氣保護作用(圖4a, 6a)。
意義:氫氣保護作用依賴PI3K/Akt/GSK3β通路激活和自噬抑制。
(3) 氫氣激活PI3K/Akt/GSK3β通路(圖2b-d, 4b-d)
數據:
TBI激活p-Akt/p-GSK3β,氫氣進一步強化該效應(圖2b-d)。
LY294002抑制通路蛋白表達(圖4b-d)。
意義:PI3K/Akt/GSK3β是氫氣保護作用的核心信號軸。
(4) 氫氣抑制自噬(圖3, 5, 7)
數據:
TBI誘導自噬(LC3-II/I、Beclin-1↑),氫氣顯著抑制其表達(圖3a-d)。
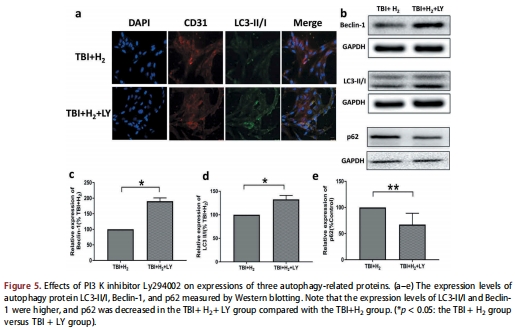
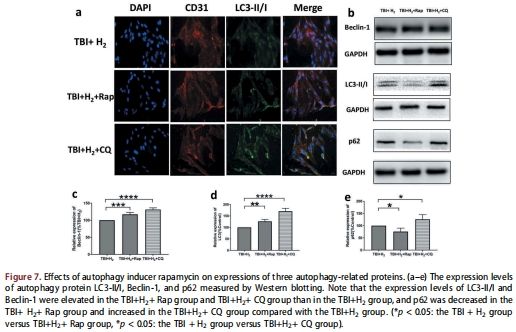
LY294002解除氫氣對自噬的抑制(圖5a-d),雷帕霉素激活自噬并降低細胞活力(圖7a-e)。
意義:氫氣通過PI3K/Akt/GSK3β通路抑制自噬,維持內皮細胞穩態。
5. 研究結論
1.氫氣通過激活PI3K/Akt/GSK3β通路抑制自噬,改善TBI后內皮細胞活力與修復能力。
2.自噬在TBI中具有損傷作用,氫氣通過抑制自噬發揮保護效應。
3.PI3K抑制劑(LY294002)和自噬誘導劑(雷帕霉素)可逆轉氫氣保護作用,證實機制特異性。
4.氫氣治療TBI具有潛在臨床轉化價值,需進一步探索體內驗證及劑量優化。
6. 丹麥Unisense電極的核心價值
(1) 技術角色
精確標定氫氣濃度:
使用Unisense針型氫傳感器(Unisense A/S, Aarhus, Denmark)實時檢測富氫培養基濃度(0.60 ± 0.03 mM),確保實驗條件一致性(方法部分)。
解決氣體治療關鍵難題:氫氣溶解度低、易擴散,Unisense電極提供高精度、實時濃度監測,排除劑量偏差對結果的干擾。
(2) 研究意義
1.機制可靠性保障:
精確的氫氣濃度控制確保PI3K/自噬機制結論的可重復性,避免濃度波動導致的假陽性/陰性。
2.方法學創新:
為氣體治療研究提供標準化方案,推動氫氣在神經保護領域的應用。
3.臨床轉化橋梁:
Unisense電極的定量數據為未來臨床劑量設計提供參考(如吸入氫氣濃度、富氫液體輸注方案)。
(3) 領域貢獻
填補技術空白:解決體外氣體治療濃度監測難題,提升實驗嚴謹性。
推動精準醫療:為氫氣治療TBI的劑量-效應關系研究奠定基礎。
核心圖示:氫氣保護機制通路
TBI損傷 → [PI3K/Akt/GSK3β通路抑制] + [自噬激活] → 細胞活力↓
↓
氫氣干預 → 激活PI3K/Akt/GSK3β → 抑制自噬 → 細胞修復↑
總結:
本研究通過細胞模型闡明氫氣治療TBI的新機制,Unisense電極在氫氣濃度標定中的關鍵作用保障了機制的可靠性,為靶向PI3K/自噬通路的神經保護策略提供理論依據。未來需結合動物模型驗證,并探索Unisense技術在體內氫氣監測中的應用潛力。