熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
CeO2 Nanoparticles Regulate the Propagation of Antibiotic Resistance Genes by Altering Cellular Contact and Plasmid Transfer
CeO2納米顆粒通過改變細(xì)胞接觸和質(zhì)粒轉(zhuǎn)移來調(diào)節(jié)抗生素抗性基因的傳播
來源:Environmental Science & Technology 2020 54 (16), 10012-10021
1. 論文摘要核心內(nèi)容
研究揭示 CeO?納米顆粒(NPs)通過調(diào)控細(xì)菌細(xì)胞接觸和質(zhì)粒轉(zhuǎn)移影響ARGs水平傳播:
核心發(fā)現(xiàn):
低濃度CeO? NPs(1–5 mg/L):抑制ARGs接合轉(zhuǎn)移(降低24–25%),機(jī)制包括清除ROS、減少胞外聚合物(EPS)合成、降低細(xì)胞粘附力、抑制能量代謝(圖2a, 圖4c)。
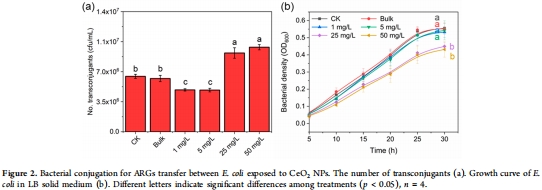
高濃度CeO? NPs(25–50 mg/L):促進(jìn)ARGs轉(zhuǎn)移(增加42–53%),機(jī)制涉及誘導(dǎo)氧化應(yīng)激、激活SOS響應(yīng)、增加EPS合成、提升ATP供應(yīng)(圖2a, 圖3a, 圖5b)。
技術(shù)亮點(diǎn):首次結(jié)合土壤模型(自然/無菌土壤)和LB平板系統(tǒng),通過多組學(xué)分析(轉(zhuǎn)錄組、代謝組)闡明CeO? NPs的雙向劑量效應(yīng)。
環(huán)境意義:為農(nóng)業(yè)納米技術(shù)安全應(yīng)用提供劑量指導(dǎo)(推薦≤5 mg/kg),抑制ARGs環(huán)境傳播。
2. 研究目的
探究CeO? NPs(農(nóng)業(yè)納米技術(shù)常用材料)對(duì)土壤中ARGs水平轉(zhuǎn)移(HGT)的影響。
揭示NPs劑量依賴性效應(yīng)的分子機(jī)制(氧化應(yīng)激、細(xì)胞粘附、能量代謝)。
評(píng)估納米顆粒在真實(shí)土壤環(huán)境中的生態(tài)風(fēng)險(xiǎn),提出安全應(yīng)用閾值。
3. 研究思路
1.多尺度模型設(shè)計(jì):
自然土壤:豬場(chǎng)土壤暴露于CeO? NPs(0, 5, 50 mg/kg),檢測(cè)ARGs豐度變化(圖1a)。
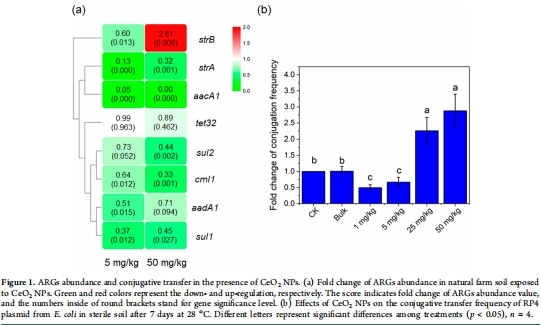
無菌土壤:接種大腸桿菌(含RP4質(zhì)粒),測(cè)定接合轉(zhuǎn)移頻率(圖1b)。
LB平板模型:精確控制NPs濃度(0–50 mg/L),量化接合轉(zhuǎn)移、ROS、EPS、ATP等(圖2–6)。
2.機(jī)制驗(yàn)證:
氧化應(yīng)激:流式細(xì)胞術(shù)測(cè)ROS,酶活檢測(cè)(SOD/CAT),轉(zhuǎn)錄組分析SOS響應(yīng)基因(圖3)。
細(xì)胞粘附:EPS含量測(cè)定(多糖/蛋白),細(xì)菌粘附實(shí)驗(yàn),基因表達(dá)分析(圖4)。
能量代謝:Unisense電極測(cè)呼吸速率,ATP含量檢測(cè),電子傳遞鏈(ETC)基因表達(dá)(圖5)。
3.環(huán)境關(guān)聯(lián):對(duì)比實(shí)驗(yàn)室模型與真實(shí)土壤結(jié)果,評(píng)估生態(tài)風(fēng)險(xiǎn)。
4. 關(guān)鍵數(shù)據(jù)及研究意義
(1) ARGs豐度與接合轉(zhuǎn)移(圖1, 圖2)
數(shù)據(jù):
自然土壤:50 mg/kg CeO? NPs降低多數(shù)ARGs豐度(如aacA1↓),但strB顯著↑(圖1a)。
無菌土壤/LB平板:低濃度NPs(1–5 mg/L)抑制接合轉(zhuǎn)移頻率↓24–25%,高濃度(25–50 mg/L)促進(jìn)↑42–53%(圖1b, 圖2a)。
意義:首次發(fā)現(xiàn)CeO? NPs對(duì)ARGs傳播的雙向劑量效應(yīng),挑戰(zhàn)“NPs單向促進(jìn)ARGs”的傳統(tǒng)認(rèn)知。
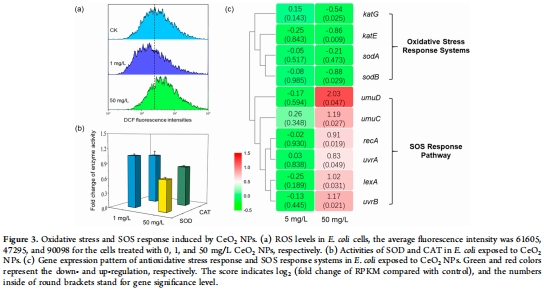
(2) 氧化應(yīng)激與SOS響應(yīng)(圖3)
數(shù)據(jù):
高濃度CeO? NPs(50 mg/L):ROS↑90%,SOD/CAT活性↓,SOS基因(lexA/recA)↑2倍(圖3a–c)。
低濃度(1 mg/L):ROS↓,抗氧化酶無變化(圖3a)。
意義:闡明NPs通過ROS-SOS軸調(diào)控質(zhì)粒轉(zhuǎn)移,高濃度激活DNA修復(fù)機(jī)制促進(jìn)HGT。
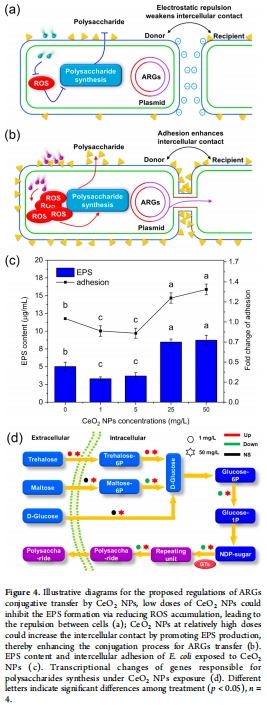
(3) 細(xì)胞粘附與EPS調(diào)控(圖4)
數(shù)據(jù):
低濃度NPs:EPS多糖↓33–42%,細(xì)胞粘附力↓15–17%(圖4c)。
高濃度NPs:EPS多糖↑86–89%,粘附力↑(圖4c);多糖合成基因(如GTs)顯著上調(diào)(圖4d)。
意義:EPS是細(xì)胞接觸的關(guān)鍵介質(zhì),其劑量依賴性變化直接決定接合轉(zhuǎn)移效率。
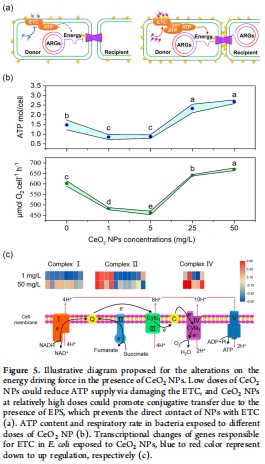
(4) 能量代謝與ATP驅(qū)動(dòng)(圖5)
數(shù)據(jù):
低濃度:呼吸速率↓20%,ATP↓57–59%,ETC基因(nuo系列)下調(diào)(圖5b–c)。
高濃度:呼吸速率↑13%,ATP↑158–181%,ETC復(fù)合體II/IV基因(frdA/cydB)上調(diào)(圖5b–c)。
意義:能量供應(yīng)是接合轉(zhuǎn)移的限速步驟,ATP水平與轉(zhuǎn)移頻率正相關(guān)。
(5) 質(zhì)粒轉(zhuǎn)移基因表達(dá)(圖6)
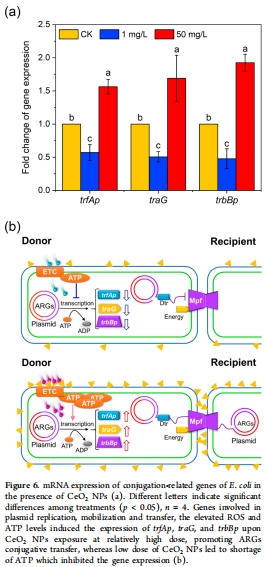
數(shù)據(jù):
高濃度NPs:接合相關(guān)基因(trbBp, trfAp, traG)顯著上調(diào)(圖6a)。
低濃度:基因表達(dá)受抑(圖6a)。
意義:NPs通過調(diào)控質(zhì)粒編碼的轉(zhuǎn)移裝置基因(Mpf/Dtr)直接影響ARGs傳播。
5. 研究結(jié)論
1.雙向劑量效應(yīng):
低劑量CeO? NPs(≤5 mg/kg):抑制ARGs傳播,機(jī)制為清除ROS→減少EPS→降低細(xì)胞接觸→抑制能量合成。
高劑量(≥25 mg/kg):促進(jìn)ARGs傳播,機(jī)制為誘導(dǎo)ROS→激活SOS→增加EPS→提升ATP供應(yīng)。
2.納米特異性:CeO? NPs效應(yīng)顯著強(qiáng)于塊體顆粒(BPs),證實(shí)“尺寸效應(yīng)”(圖2a)。
3.環(huán)境推薦:農(nóng)業(yè)應(yīng)用CeO? NPs時(shí)應(yīng)控制濃度≤5 mg/kg,以兼顧植物促生與ARGs抑制。
4.機(jī)制框架:建立“氧化應(yīng)激–細(xì)胞粘附–能量代謝”三聯(lián)調(diào)控模型(圖4, 圖5, 圖6b)。
6. 丹麥Unisense電極的核心價(jià)值
(1) 技術(shù)優(yōu)勢(shì)
高精度實(shí)時(shí)監(jiān)測(cè):Unisense微呼吸系統(tǒng)(電極尖端500 μm)直接測(cè)定細(xì)菌呼吸速率(圖5b),靈敏度達(dá)單細(xì)胞水平。
動(dòng)態(tài)能量代謝解析:同步關(guān)聯(lián)呼吸速率與ATP含量,揭示CeO? NPs對(duì)電子傳遞鏈(ETC)的劑量效應(yīng):
低濃度抑制ETC(復(fù)合體I/II基因下調(diào))→ 呼吸↓ → ATP↓ → 接合轉(zhuǎn)移受限。
高濃度激活替代ETC路徑(復(fù)合體II/IV基因上調(diào))→ 呼吸↑ → ATP↑ → 接合轉(zhuǎn)移增強(qiáng)。
(2) 科學(xué)突破
1.揭示能量代謝的核心地位:
Unisense數(shù)據(jù)首次證實(shí):ATP水平是接合轉(zhuǎn)移的限速因子(圖5b)。
低濃度NPs通過抑制ETC減少ATP合成,直接限制質(zhì)粒轉(zhuǎn)移的能量需求(圖5c)。
2.解析納米-生物界面相互作用:
呼吸速率變化反映NPs對(duì)ETC的直接影響:
低濃度:NPs穿透細(xì)胞膜→ 破壞ETC復(fù)合體→ 電子泄漏↓ → 呼吸抑制。
高濃度:EPS屏障形成→ 減少NPs接觸→ ETC代償性增強(qiáng)→ 呼吸促進(jìn)。
(3) 環(huán)境應(yīng)用意義
劑量閾值確定:Unisense數(shù)據(jù)支撐“5 mg/kg”安全閾值,低于此濃度時(shí)呼吸抑制→能量受限→ARGs傳播受阻。
納米毒性預(yù)警:呼吸速率可作為NPs生態(tài)風(fēng)險(xiǎn)的敏感指標(biāo),早于傳統(tǒng)毒性終點(diǎn)(如生長抑制)。
精準(zhǔn)調(diào)控策略:通過設(shè)計(jì)NPs表面修飾(如增強(qiáng)ROS清除能力),優(yōu)化低劑量抑菌增效應(yīng)。
核心圖示:CeO? NPs的雙向調(diào)控機(jī)制
低濃度CeO? NPs → 清除ROS → EPS↓ → 細(xì)胞接觸↓ + ETC抑制→ATP↓ → 抑制接合轉(zhuǎn)移
↓
高濃度CeO? NPs → 誘導(dǎo)ROS → EPS↑ → 細(xì)胞接觸↑ + ETC激活→ATP↑ → 促進(jìn)接合轉(zhuǎn)移
總結(jié):
本研究通過整合 土壤-平板-分子 多模型,揭示CeO? NPs對(duì)ARGs傳播的雙向劑量效應(yīng)。丹麥Unisense電極的 高分辨率呼吸監(jiān)測(cè) 為“能量代謝核心調(diào)控”理論提供關(guān)鍵技術(shù)支撐,不僅闡明NPs的生態(tài)風(fēng)險(xiǎn)機(jī)制,也為農(nóng)業(yè)納米技術(shù)的安全設(shè)計(jì)提供理論依據(jù)。