熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
Fungal biofilm architecture produces hypoxic microenvironments that drive antifungal resistance
真菌生物膜結(jié)構(gòu)產(chǎn)生低氧微環(huán)境,驅(qū)動抗真菌耐藥性
來源: PNAS | September 8, 2020 | vol. 117 | no. 36 | 22473–22483
1. 摘要核心內(nèi)容
論文揭示了絲狀真菌生物膜抗藥性的新機(jī)制:
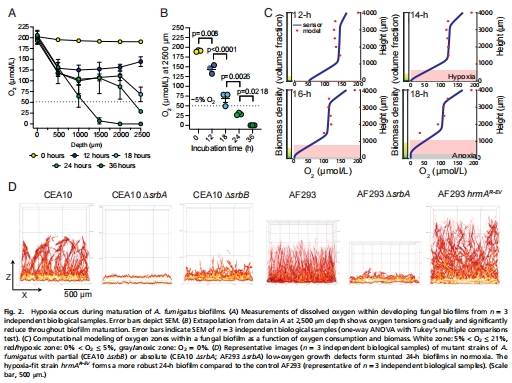
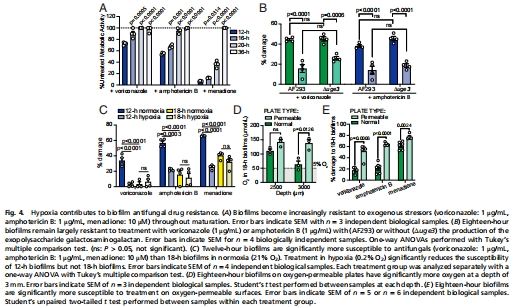
核心發(fā)現(xiàn):煙曲霉(Aspergillus fumigatus)生物膜在成熟過程中自發(fā)形成缺氧微環(huán)境(圖2),這種缺氧狀態(tài)驅(qū)動生物膜對抗真菌藥物(如伏立康唑、兩性霉素B)產(chǎn)生耐藥性(圖4)。
機(jī)制解析:
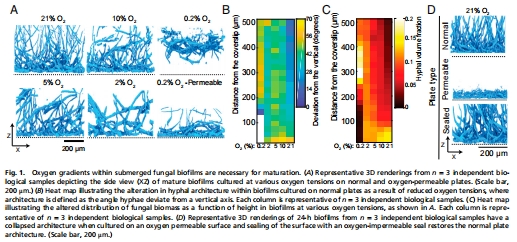
生物膜的垂直菌絲結(jié)構(gòu)消耗氧氣,導(dǎo)致基底缺氧(圖1D);
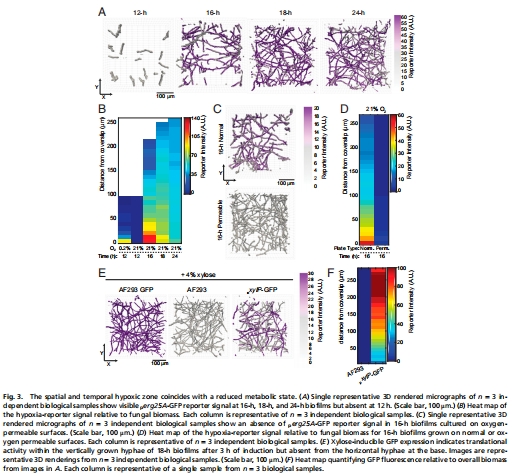
缺氧區(qū)域細(xì)胞代謝活性降低(圖3E-F),成為耐藥細(xì)胞庫;
增氧處理(如氧滲透板)可顯著增強(qiáng)藥物敏感性(圖4E)。
意義:缺氧微環(huán)境是細(xì)菌和真菌生物膜耐藥的共同機(jī)制,為克服抗真菌耐藥提供了新靶點(diǎn)。
2. 研究目的
解決關(guān)鍵科學(xué)問題:
1.耐藥性矛盾:為何體外藥敏試驗(yàn)敏感的煙曲霉在體內(nèi)感染中治療失敗?
2.生物膜特性:絲狀真菌生物膜的獨(dú)特結(jié)構(gòu)(開放菌絲網(wǎng)絡(luò))如何影響缺氧微環(huán)境形成?
3.機(jī)制空白:缺氧微環(huán)境是否直接導(dǎo)致抗真菌耐藥?其分子機(jī)制是什么?
3. 研究思路
采用多尺度驗(yàn)證策略:
1.模型構(gòu)建:
體外培養(yǎng)煙曲霉生物膜(正常板 vs. 氧滲透板);
對比不同氧濃度(21% O? vs. 0.2% O?)對生物膜結(jié)構(gòu)的影響(圖1A-C)。
2.缺氧可視化:
構(gòu)建缺氧報(bào)告菌株(p<sub>erg25A</sub>-GFP),實(shí)時(shí)監(jiān)測缺氧區(qū)域(圖3A-B);
丹麥Unisense微電極定量生物膜內(nèi)溶解氧梯度(圖2A-B)。
3.耐藥性驗(yàn)證:
藥敏試驗(yàn)(XTT法)檢測伏立康唑/兩性霉素B對生物膜的殺傷效果(圖4);
基因敲除株(ΔsrbA, ΔsrbB)驗(yàn)證缺氧響應(yīng)通路的作用(圖2D)。
4.機(jī)制探索:
翻譯活性報(bào)告菌株(p<sub>xylP</sub>-GFP)定位代謝靜止細(xì)胞(圖3E-F);
呼吸增強(qiáng)劑(FCCP)和三羧酸循環(huán)(TCA)中間體調(diào)控缺氧(圖5)。
4. 測量數(shù)據(jù)及研究意義
(1)生物膜結(jié)構(gòu)與氧梯度(圖1-2)
數(shù)據(jù):
微電極測量顯示:生物膜深層(2.5 mm)氧濃度從21%降至近0%(圖2B);
計(jì)算模型預(yù)測缺氧區(qū)(O? ≤ 5%)在14-16小時(shí)形成(圖2C)。
意義:首次證實(shí)絲狀真菌生物膜自發(fā)形成三維氧梯度,顛覆“開放結(jié)構(gòu)無缺氧”的認(rèn)知。
(2)缺氧與代謝靜止(圖3)
數(shù)據(jù):
p<sub>erg25A</sub>-GFP報(bào)告基因顯示基底缺氧(圖3B);
p<sub>xylP</sub>-GFP揭示基底菌絲翻譯活性降低(圖3F)。
意義:缺氧區(qū)域細(xì)胞進(jìn)入代謝靜止?fàn)顟B(tài),成為耐藥細(xì)胞庫。
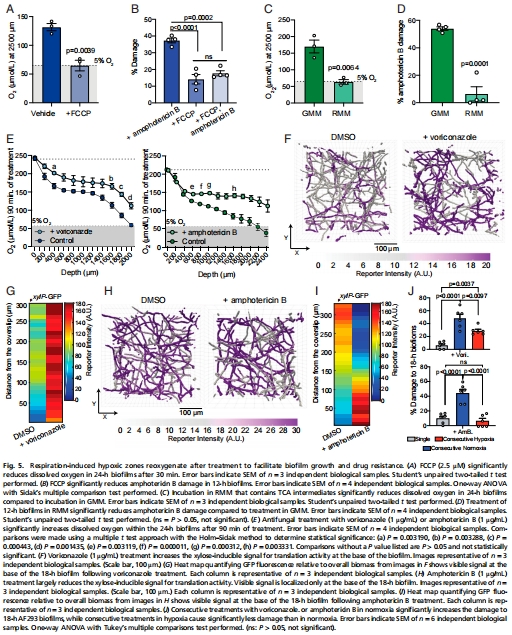
(3)缺氧驅(qū)動耐藥(圖4-5)
數(shù)據(jù):
成熟生物膜(18 h)耐藥性顯著高于未成熟生物膜(12 h)(圖4A);
增氧處理(氧滲透板)使兩性霉素B殺傷率↑45%(圖4E);
呼吸增強(qiáng)劑FCCP加劇缺氧,降低藥物敏感性(圖5B)。
意義:缺氧是獨(dú)立于胞外基質(zhì)的耐藥新機(jī)制,靶向缺氧可逆轉(zhuǎn)耐藥。
(4)治療啟示(圖5J)
數(shù)據(jù):
連續(xù)給藥在常氧下增效,但在缺氧下失效(圖5J);
抗真菌藥物處理后氧濃度反常上升(圖5E),提示殺死耗氧菌體。
意義:臨床需聯(lián)合增氧策略(如高壓氧)以增強(qiáng)抗真菌療效。
5. 結(jié)論
1.缺氧是耐藥核心驅(qū)動力:煙曲霉生物膜通過菌絲呼吸消耗氧氣,形成基底缺氧微環(huán)境,誘導(dǎo)代謝靜止和耐藥;
2.結(jié)構(gòu)-功能關(guān)聯(lián):垂直菌絲朝向氧源生長(“趨氧性”)是缺氧微環(huán)境形成的前提;
3.治療新策略:破壞缺氧微環(huán)境(如氧滲透材料、呼吸抑制劑)可克服生物膜耐藥;
4.進(jìn)化保守性:缺氧耐藥機(jī)制在細(xì)菌和真菌中保守存在,是跨物種抗菌新靶點(diǎn)。
6. 丹麥Unisense電極的研究意義
技術(shù)應(yīng)用背景(Materials and Methods部分)
"Dissolved oxygen was quantified using a Unisense Oxygen Measuring System... with a 25-μm Clark-type sensor"
核心貢獻(xiàn):
1.高分辨率氧測繪:
實(shí)現(xiàn)空間分辨率200-500 μm的溶解氧動態(tài)監(jiān)測(圖2A);
首次直接證實(shí)生物膜深層氧濃度梯度(基底O? ≈ 0%),推翻“菌絲間隙無擴(kuò)散限制”假說。
2.關(guān)鍵機(jī)制驗(yàn)證:
發(fā)現(xiàn)抗真菌藥物升高氧濃度(圖5E),證明藥物主要?dú)⑺篮难蹙w,殘留缺氧細(xì)胞存活;
證實(shí)呼吸增強(qiáng)劑FCCP加劇缺氧(圖5A),確立真菌呼吸消耗與缺氧的因果關(guān)系。
3.技術(shù)優(yōu)勢與局限:
優(yōu)勢:微創(chuàng)實(shí)時(shí)監(jiān)測,支持復(fù)雜三維結(jié)構(gòu)分析;
局限:電極脆弱(深度>3 mm時(shí)易損),無法穿透致密菌絲區(qū)。
領(lǐng)域價(jià)值:為微生物生物膜研究提供了金標(biāo)準(zhǔn)氧檢測工具,推動缺氧靶向抗菌策略發(fā)展。