熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Seizure-induced microvascular injury is associated with impaired neurovascular coupling and blood-brain barrier dysfunction
癲癇發作誘導的微血管損傷與神經血管耦合受損和血腦屏障功能障礙相關
來源:Epilepsia, 2019, pages 1-15
《癲癇》,2019年,第1-15頁
摘要:
這篇論文研究了癲癇發作如何導致微血管損傷,并探討了其與神經血管耦合受損和血腦屏障功能障礙的關聯。摘要指出,反復癲癇發作會引起周細胞損傷、線粒體去極化、血管反應性降低和血腦屏障通透性增加。研究使用腦切片培養和體內模型,發現癲癇發作導致周細胞膜電流變化、毛細血管收縮和BBB破壞,這些變化可能與癲癇并發癥如認知障礙和神經退行性疾病相關。
研究目的:
研究目的是探討反復癲癇發作對周細胞功能的影響,特別是周細胞膜電流、血管舒張能力和BBB完整性的變化,以及這些變化如何導致神經血管解耦和微血管損傷。研究旨在揭示癲癇發作中微血管功能障礙的機制,為治療癲癇相關并發癥提供新見解。
研究思路:
研究思路采用多方法 approach,包括使用腦切片培養和體內實驗。在腦切片培養中,使用4-氨基吡啶或低鎂條件誘導癲癇發作,測量周細胞膜電流、毛細血管直徑變化、BBB通透性和線粒體功能。在體內實驗中,使用麻醉大鼠,通過電皮質圖記錄癲癇活動,同時使用Unisense電極測量組織氧分壓,并結合血管成像技術監測 arteriolar 直徑、BBB通透性和細胞損傷。研究通過比較切片和體內數據,驗證癲癇發作對神經血管耦合和BBB的影響。
測量的數據及研究意義:
1 數據:周細胞膜電流變化,包括癲癇發作誘導的內向電流和外向電流。研究意義:這些電流變化反映了周細胞在癲癇活動中的電生理響應,表明周細胞參與血管調節。來源:圖2D。

2 數據:毛細血管直徑變化和 pericytic length 變化,顯示癲癇發作初期血管舒張,但隨反復發作逐漸變為血管收縮。研究意義:表明神經血管耦合在反復發作中逐漸受損,周細胞功能衰退。來源:圖3A、圖4B。
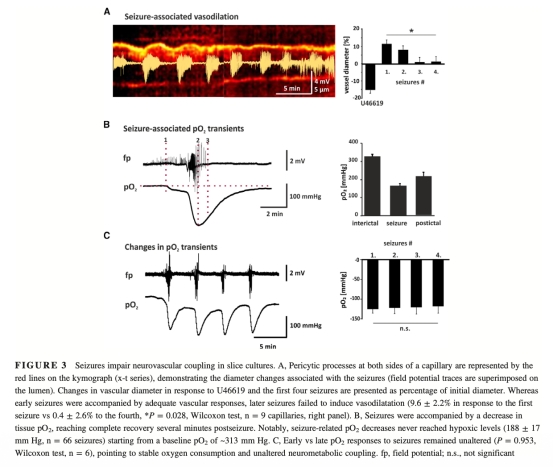
3 數據:組織氧分壓(pO2)測量,顯示癲癇發作期間pO2下降但保持高氧狀態,無缺氧。研究意義:表明神經血管解耦不是由缺氧引起,而是周細胞線粒體損傷所致。來源:圖3B、圖6C。
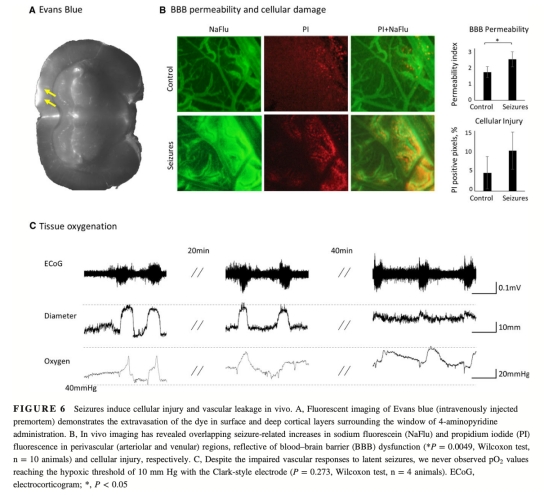
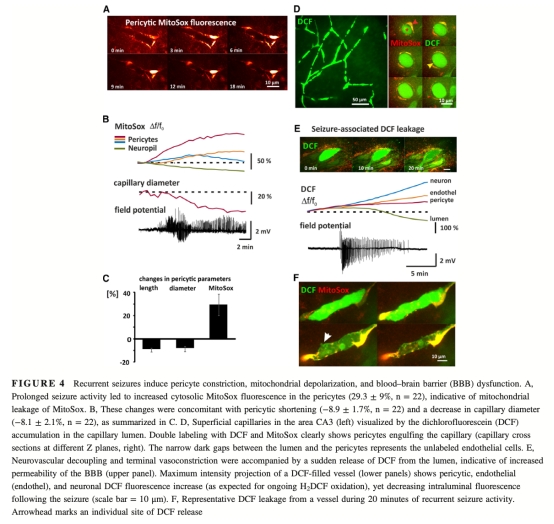
4 數據:BBB通透性變化,通過DCF熒光檢測,顯示癲癇發作導致染料從血管腔泄漏。研究意義:表明反復發作破壞BBB完整性,可能與周細胞損傷相關。來源:圖4E、圖6B。
5 數據:線粒體 depolarization,通過MitoSox熒光變化,顯示周細胞線粒體功能受損。研究意義:線粒體損傷可能導致周細胞收縮和血管功能障礙。來源:圖4A。
6 數據:體內arteriolar直徑變化和BBB通透性,顯示癲癇發作后血管反應性降低和染料滲出。研究意義:證實切片發現,表明微血管損傷在整體水平發生。來源:圖5、圖6。
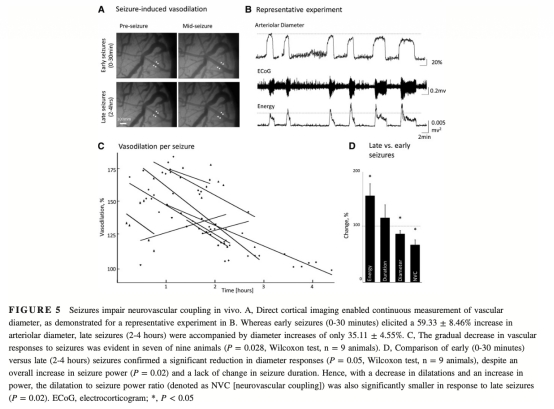
結論:
1 反復癲癇發作導致周細胞損傷,包括膜電流異常和線粒體去極化,進而引起血管收縮和神經血管解耦。
2 神經血管耦合逐漸受損,表現為血管舒張反應降低,最終導致血管無反應性,這與周細胞功能衰退相關。
3 BBB通透性增加,與周細胞損傷和血管收縮同步發生,表明周細胞在維持BBB完整性中起關鍵作用。
使用丹麥Unisense電極測量數據的研究意義:
丹麥Unisense電極用于測量組織氧分壓(pO2),在研究中顯示癲癇發作期間pO2下降(從約313 mmHg降至188 mmHg),但組織仍保持高氧狀態,未達到缺氧水平(缺氧閾值通常為10 mmHg)。這些數據表明,神經血管解耦和微血管損傷不是由組織缺氧引起,因為pO2在發作后迅速恢復,且反復發作中pO2響應保持穩定。相反,pO2測量支持周細胞線粒體損傷作為主要原因,因為線粒體 depolarization 導致周細胞收縮和血管功能障礙。Unisense電極的高精度測量提供了關鍵證據,排除了缺氧作為直接因素,突出了周細胞在癲癇發作微血管損傷中的核心作用。