熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Facile Deposition of Manganese Dioxide to Albumin-Bound Paclitaxel Nanoparticles for Modulation of Hypoxic Tumor Microenvironment To Improve Chemoradiation Therapy
二氧化錳輕松沉積到白蛋白結合紫杉醇納米顆粒上以調節缺氧腫瘤微環境改善化學放療治療
來源:Molecular Pharmaceutics, Volume 15, pages 447-457, 2018
《分子藥劑學》,第15卷,第447-457頁,2018年
摘要
這篇論文開發了一種簡單方法將錳二氧化物(MnO2)沉積到白蛋白結合紫杉醇納米顆粒(ANPs-PTX)表面,形成MnO2功能化的MANPs-PTX。在腫瘤微環境中,MANPs-PTX能消耗過量過氧化氫(H2O2)產生氧氣,從而改善腫瘤缺氧,增強化學放療效果。同時,釋放的Mn2+離子具有優異的T1磁共振成像(MRI)性能,用于腫瘤檢測。MANPs-PTX作為一種治療診斷劑,具有潛在的臨床應用前景。
研究目的
研究目的是開發一種新型納米顆粒MANPs-PTX,通過調節腫瘤微環境中的缺氧和H2O2水平,來增強化學放療的療效,并提供MRI成像能力,從而解決結腸癌治療中因缺氧和氧化應激導致的治療抵抗問題。
研究思路
研究思路是通過一步氧化法將KMnO4添加到ANPs-PTX懸浮液中,使MnO2沉積在納米顆粒表面,形成MANPs-PTX。隨后對MANPs-PTX進行表征,包括尺寸、電位、形貌和氧氣生成能力。通過體外實驗測試細胞攝取、細胞毒性和放療增強效果,體內實驗評估生物分布、MRI性能、H2O2消耗、氧氣生成以及治療效果和毒性。使用丹麥Unisense電極測量氧氣分壓,以量化氧氣生成。
測量的數據及研究意義
1 數據:納米顆粒的尺寸、zeta電位和形貌,通過動態光散射(DLS)和透射電鏡(TEM)測量。研究意義:確認MnO2成功沉積在ANPs-PTX表面,納米顆粒尺寸約140 nm,zeta電位-30.3 mV,形貌粗糙,表明MnO2涂層形成。來源:圖2a、b、c。
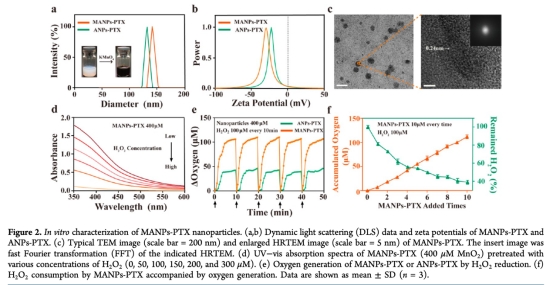
2 數據:氧氣生成和H2O2消耗能力,使用Clark氧氣探頭測量。研究意義:MANPs-PTX在H2O2存在下可持續生成氧氣,同時消耗H2O2,證明其能改善腫瘤缺氧。來源:圖2e、f。
3 數據:細胞攝取和內化途徑,通過流式細胞術和共聚焦顯微鏡測量。研究意義:MANPs-PTX主要通過網格蛋白和小窩蛋白介導的內吞途徑進入細胞,定位于溶酶體,為藥物遞送提供機制 insight。來源:圖3a、b、c。
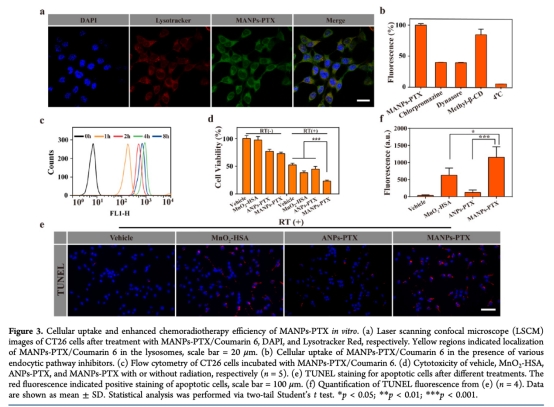
4 數據:細胞毒性和放療增強效果,通過CCK-8 assay和TUNEL染色測量。研究意義:MANPs-PTX聯合放療顯著降低細胞活力,誘導凋亡,顯示增強的化療放療協同效應。來源:圖3d、e、f。
5 數據:體內生物分布,通過近紅外熒光成像測量。研究意義:MANPs-PTX在腫瘤中積累,峰值在48小時,表明EPR效應介導的靶向性,利于局部治療。來源:圖4a、b、c、d。
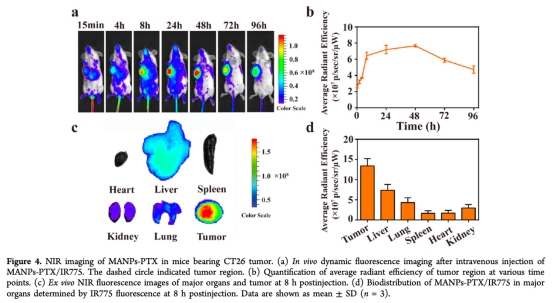
6 數據:MRI性能,通過T1加權成像測量。研究意義:MANPs-PTX在腫瘤中釋放Mn2+,增強T1信號,用于腫瘤檢測和監測。來源:圖5a、b、c、d、e。
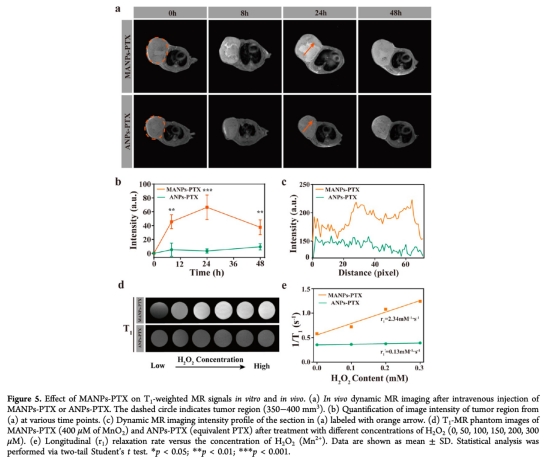
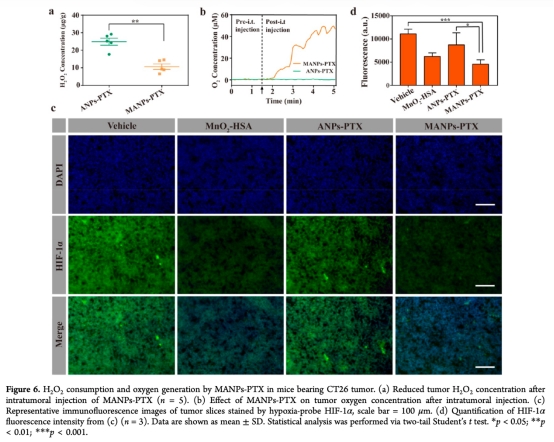
7 數據:體內H2O2消耗和氧氣生成,通過Clark氧氣探頭和H2O2 assay kit測量。研究意義:MANPs-PTX在腫瘤中消耗H2O2并生成氧氣,直接改善缺氧,降低HIF-1α表達。來源:圖6a、b、c、d。
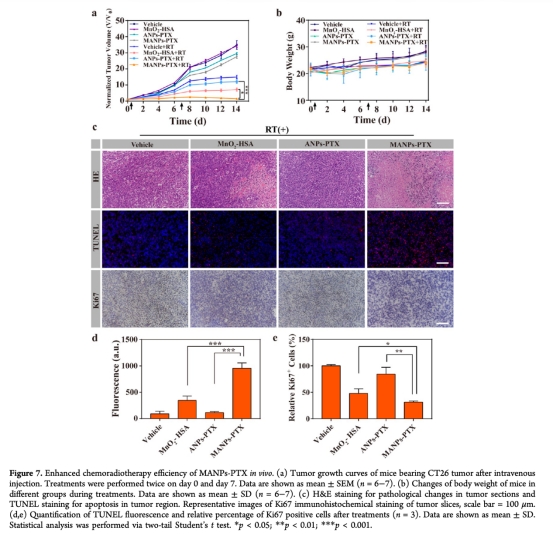
8 數據:體內治療效果,通過腫瘤體積測量和免疫組化評估。研究意義:MANPs-PTX聯合放療顯著抑制腫瘤生長,減少Ki67陽性細胞,增加凋亡,證明治療 efficacy。來源:圖7a、b、c、d、e。
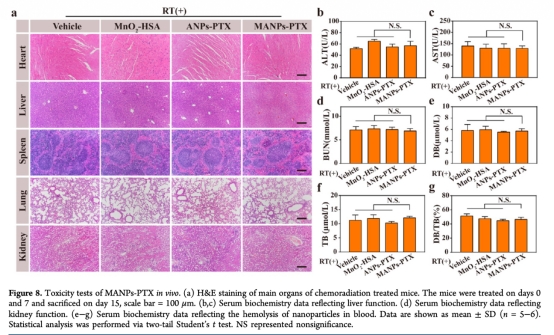
9 數據:毒性測試,通過血清生化和組織切片評估。研究意義:MANPs-PTX對肝、腎功能無顯著影響,顯示良好生物安全性。來源:圖8a、b、c、d、e、f、g。
結論
1 MANPs-PTX通過沉積MnO2,能有效消耗腫瘤H2O2并生成氧氣,改善缺氧微環境,從而增強化學放療療效。
2 MANPs-PTX釋放的Mn2+提供優異的T1 MRI成像能力,實現治療診斷一體化。
3 體內外實驗證實MANPs-PTX具有良好的腫瘤靶向性、治療效果和安全性,是一種有前景的結腸癌治療策略。
使用丹麥Unisense電極測量數據的研究意義
丹麥Unisense電極用于測量氧氣分壓(pO2),在研究中關鍵用于量化MANPs-PTX的氧氣生成能力。在體外實驗中,電極監測到MANPs-PTX與H2O2反應后氧氣濃度顯著上升(圖2e),證實其能持續生成氧氣。在體內實驗中,電極插入腫瘤組織,直接測量到MANPs-PTX注射后氧氣濃度增加約50 μM(圖6b),證明其能有效逆轉腫瘤缺氧。這些數據提供了直接證據,表明MANPs-PTX通過化學反應改善腫瘤微環境,從而增強放療敏感性,這是研究的核心機制。Unisense電極的高精度和實時監測能力確保了數據的可靠性,為治療策略提供了實驗基礎。