熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Natural antisense transcripts are linked to the modulation of mitochondrial function and teliospore dormancy in Ustilago maydis
天然反義轉錄本與玉米黑粉菌線粒體功能調節及休眠孢子休眠性相關
來源:Molecular Microbiology[2017] 103[5], 745-763
《分子微生物學》,2017年,第103卷,第5期,第745-763頁
摘要
這篇論文研究了在玉米黑粉菌Ustilago maydis中,天然反義轉錄本(NATs)如何調節線粒體功能和冬孢子休眠。重點關注了as-ssm1 NAT,它互補于線粒體絲氨酸-tRNA合成酶基因(ssm1)。通過異位表達as-ssm1,發現它導致生長率、毒力、線粒體膜電位和氧消耗減少,并形成雙鏈RNA,增加ssm1轉錄水平但不改變蛋白質水平。這表明as-ssm1通過dsRNA形成和減少線粒體功能來促進冬孢子休眠。
研究目的
研究目的是探究NATs在調節線粒體功能和冬孢子休眠中的作用,特別是在U. maydis中。旨在驗證NATs通過調節核編碼的線粒體蛋白基因表達來調控代謝休眠的假說,并闡明as-ssm1在休眠過程中的具體功能。
研究思路
研究思路包括:首先通過EST庫和RNA-seq分析識別在冬孢子中特異性表達的NATs,特別是針對線粒體相關基因的NATs;選擇as-ssm1作為候選NAT,因其在冬孢子中高表達;通過異位表達as-ssm1在單倍體細胞中研究其功能;評估其對細胞生長、致病性、線粒體功能等的影響;使用分子生物學方法檢測dsRNA形成和轉錄/蛋白質水平變化;并比較相關物種以驗證保守性。
測量的數據及研究意義
1. NATs表達模式:通過 strand-specific RT-PCR 檢測 as-ssm1 在冬孢子中的特異性表達,以及其在植物感染時間過程中的出現時機。來自圖1、圖3、圖4。研究意義:證實NATs在休眠階段特異性表達,支持其參與休眠調節的假說。
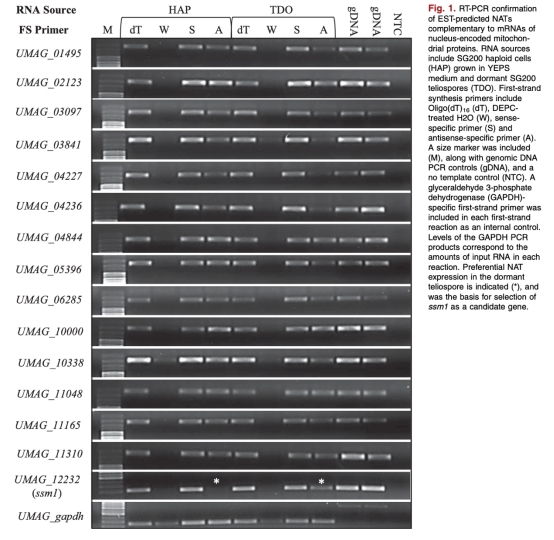
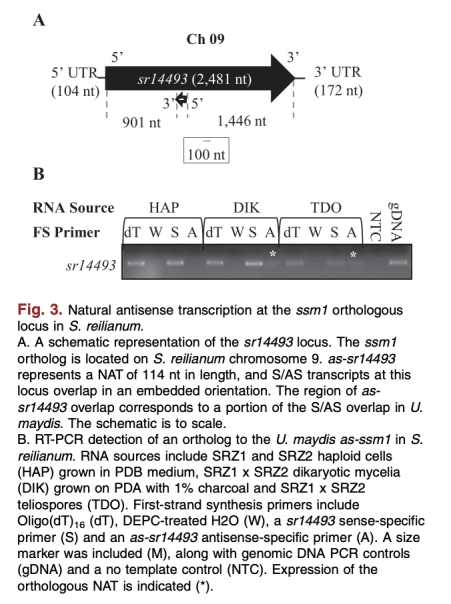

2. ssm1基因重要性:通過刪除實驗顯示ssm1是細胞存活所必需的,缺失導致細胞裂解。來自圖5。研究意義:表明ssm1對線粒體功能和細胞完整性關鍵,間接支持NATs可能通過調節此類基因影響休眠。
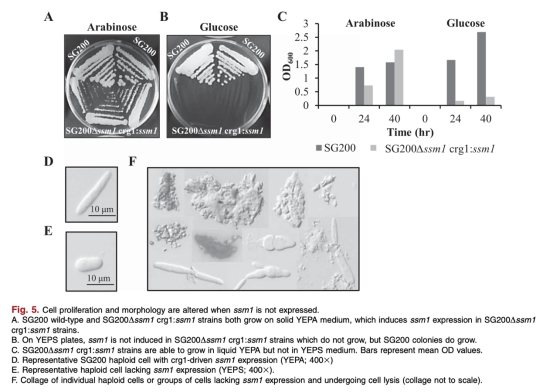
3. as-ssm1表達對ssm1 mRNA的影響:異位表達as-ssm1增加ssm1轉錄水平并形成dsRNA。來自圖6A和6B。研究意義:提示NATs可能通過dsRNA穩定mRNA,在休眠中保存轉錄本以供萌發時快速翻譯。
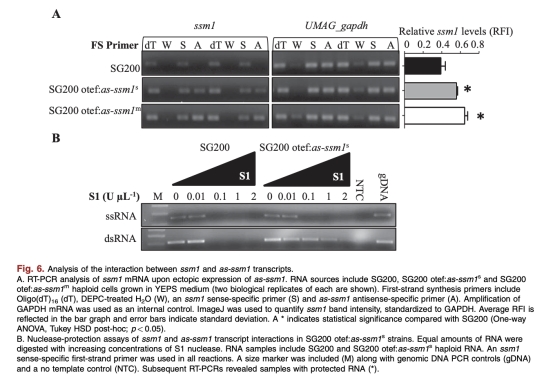
4. 生長率和致病性:as-ssm1表達降低細胞生長率和植物感染中的毒力。來自圖7A和7B。研究意義:表明NATs表達可模擬休眠狀態下的代謝減緩,支持其參與發育調節。
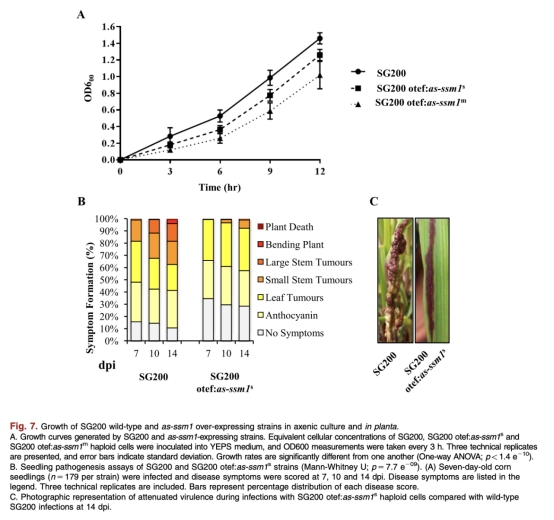
5. 冬孢子發育:as-ssm1表達延遲冬孢子形成。來自圖8。研究意義:證實NATs在休眠過渡中起作用,影響發育時間線。
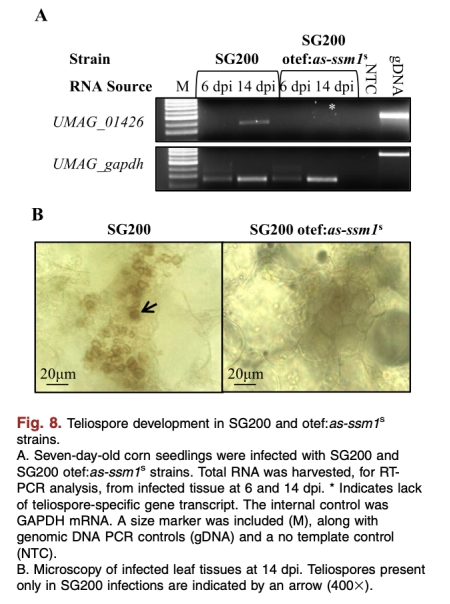
6. 線粒體膜電位:使用MitoTracker染色顯示as-ssm1表達降低膜電位。來自圖9A。研究意義:直接顯示線粒體功能受損,與休眠的低代謝一致。
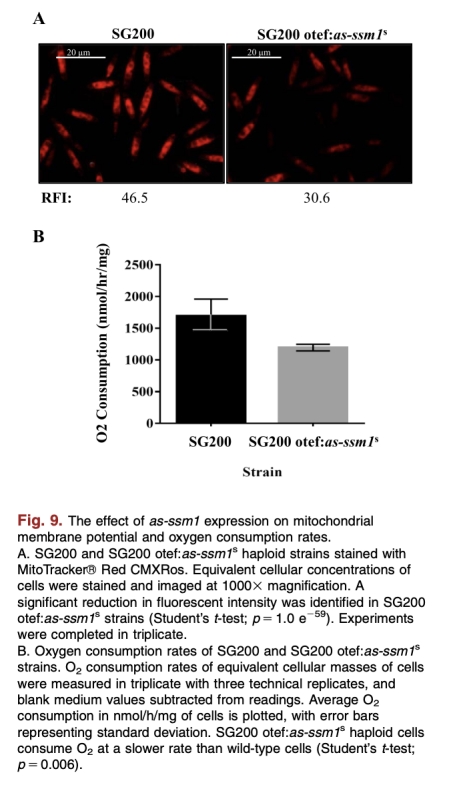
7. 氧消耗率:使用Clark-type微呼吸計(丹麥Unisense電極)測量顯示as-ssm1表達降低氧消耗。來自圖9B。研究意義:定量證明呼吸作用減少,強化NATs在抑制代謝中的角色。
8. Ssm1蛋白質水平:Western blot顯示as-ssm1表達不改變蛋白質水平。來自圖10。研究意義:表明NATs可能通過翻譯干擾而非蛋白質降解調節功能,提示RNA介導的機制。
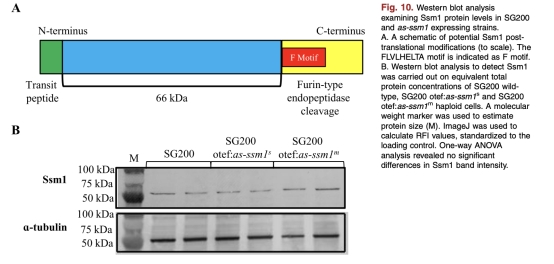
結論
論文得出結論:as-ssm1 NAT通過形成dsRNA和可能通過RNA介導的機制調節線粒體功能,從而促進冬孢子休眠。NATs在休眠入口和維持中起關鍵作用,通過可逆地穩定mRNA并抑制翻譯,使細胞在萌發時快速恢復代謝。該研究支持NATs作為重要調節因子在真菌發育過程中的作用。
使用丹麥Unisense電極測量數據的研究意義
使用丹麥Unisense電極(Clark-type微呼吸計)測量的氧消耗數據(來自圖9B)顯示,as-ssm1表達菌株的氧消耗率比野生型低1.4倍。這一數據的研究意義在于:它直接定量地證明了線粒體呼吸功能受損,為NATs降低代謝活動提供了實驗證據。氧消耗減少與休眠狀態的低呼吸率一致,支持as-ssm1通過抑制氧化磷酸化來誘導代謝暫停的假說。此外,該方法的高靈敏度允許精確檢測細微的呼吸變化,強化了NATs在調節細胞能量代謝中的功能性角色,并為理解休眠的分子機制提供了關鍵指標。