熱線:021-66110810,66110819
手機(jī):13564362870


熱線:021-66110810,66110819
手機(jī):13564362870
Abscisic acid enhances glucose disposal and induces brown fat activity in adipocytes in vitro and in vivo
脫落酸在體外和體內(nèi)增強(qiáng)葡萄糖處置并誘導(dǎo)脂肪細(xì)胞棕色脂肪活性
來(lái)源:Biochimica et Biophysica Acta, Volume 1862, 2017, Pages 131-144
《生物化學(xué)與生物物理學(xué)報(bào)》,第1862卷,2017年,第131-144頁(yè)
摘要
這篇論文研究了脫落酸(ABA)在脂肪細(xì)胞葡萄糖處置和棕色脂肪活性誘導(dǎo)中的作用。ABA是一種植物激素,在動(dòng)物中也存在,通過(guò)其受體LANCL2調(diào)節(jié)先天免疫細(xì)胞功能和葡萄糖處置。研究發(fā)現(xiàn),ABA通過(guò)LANCL2刺激脂肪細(xì)胞葡萄糖攝取,減少甘油三酯積累,增加氧消耗和二氧化碳產(chǎn)生,并誘導(dǎo)棕色脂肪標(biāo)記基因(如UCP1、PGC-1α)表達(dá)。在體外,ABA處理增強(qiáng)3T3-L1脂肪細(xì)胞葡萄糖代謝和棕色化;在體內(nèi),口服ABA增加大鼠棕色脂肪葡萄糖攝取和小鼠白色脂肪棕色化基因表達(dá)。結(jié)果表明ABA可能通過(guò)誘導(dǎo)棕色脂肪活性改善糖耐量和能量平衡。
研究目的
研究目的是探究ABA/LANCL2系統(tǒng)在脂肪細(xì)胞葡萄糖攝取和代謝調(diào)節(jié)中的作用,特別是ABA是否能夠誘導(dǎo)脂肪細(xì)胞棕色化(browning),從而增強(qiáng)葡萄糖處置和能量消耗,為代謝疾病治療提供新見解。
研究思路
研究思路包括體外和體內(nèi)實(shí)驗(yàn)。體外使用3T3-L1小鼠脂肪細(xì)胞和人類脂肪間充質(zhì)干細(xì)胞(ATMSC),通過(guò)ABA處理、LANCL2沉默或過(guò)表達(dá),測(cè)量葡萄糖攝取、氧消耗、基因表達(dá)和代謝產(chǎn)物;體內(nèi)通過(guò)口服ABA處理大鼠和小鼠,評(píng)估棕色脂肪葡萄糖攝取(微PET成像)和組織基因表達(dá)。關(guān)鍵實(shí)驗(yàn)包括:ABA對(duì)葡萄糖轉(zhuǎn)運(yùn)蛋白GLUT4表達(dá)的影響、氧消耗測(cè)量(使用丹麥Unisense電極)、棕色脂肪標(biāo)記基因分析,以及長(zhǎng)期ABA處理對(duì)脂肪組織重塑的作用。
測(cè)量的數(shù)據(jù)及研究意義
1 葡萄糖攝取和GLUT4表達(dá):ABA處理增加3T3-L1脂肪細(xì)胞GLUT4蛋白表達(dá)和葡萄糖攝取,類似胰島素效應(yīng),但依賴PI3K通路。LANCL2沉默消除ABA和胰島素的刺激作用,而過(guò)表達(dá)增強(qiáng)基礎(chǔ)葡萄糖攝取。數(shù)據(jù)來(lái)自圖1和圖3。研究意義:表明ABA通過(guò)LANCL2受體激活胰島素樣信號(hào)通路,增強(qiáng)脂肪細(xì)胞葡萄糖處置,為ABA改善糖代謝提供機(jī)制證據(jù)。
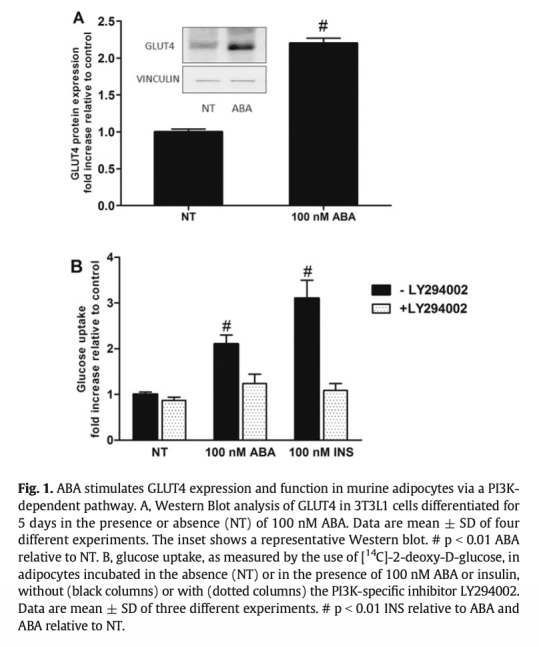
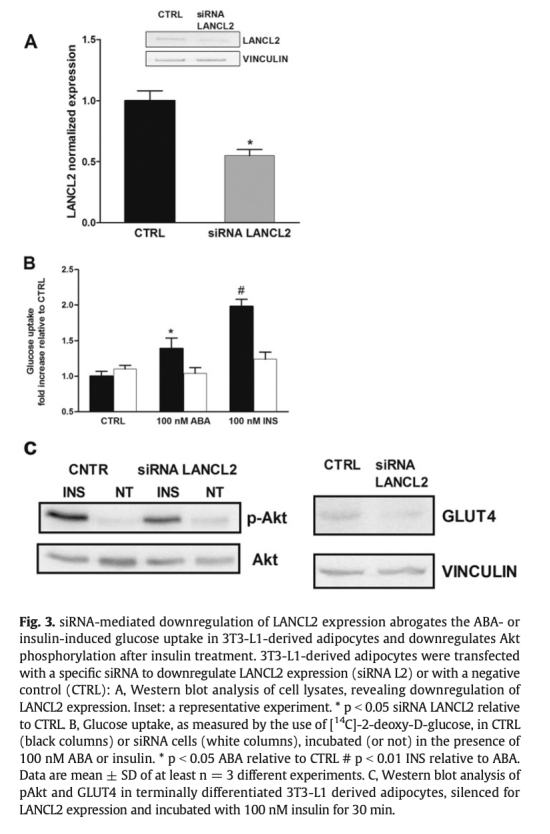
2 氧消耗測(cè)量:使用丹麥Unisense微電極系統(tǒng)測(cè)量脂肪細(xì)胞氧消耗,ABA處理顯著增加3T3-L1脂肪細(xì)胞氧消耗率(約30%),表明代謝活性增強(qiáng)。數(shù)據(jù)來(lái)自圖2。研究意義:直接證明ABA提升脂肪細(xì)胞呼吸速率,支持其誘導(dǎo)產(chǎn)熱和能量消耗的作用,與棕色化表型一致。
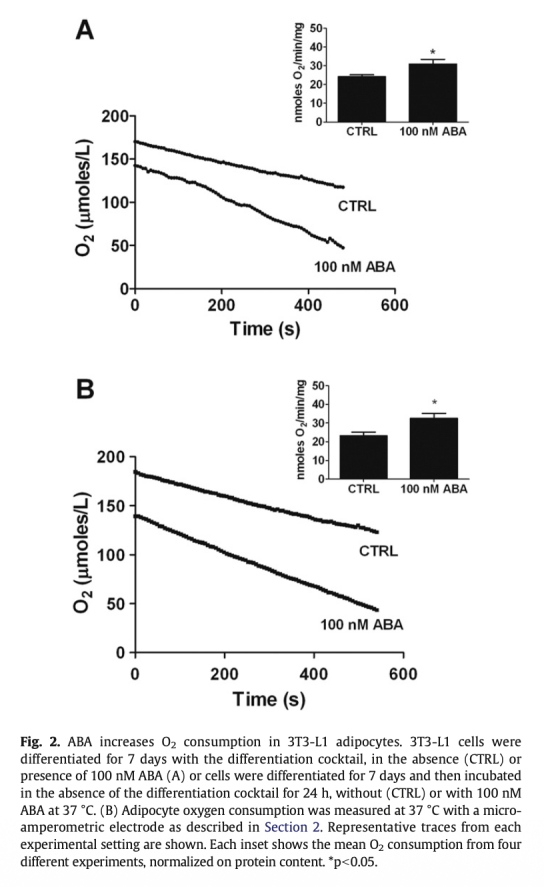
3 基因表達(dá)分析:ABA上調(diào)棕色脂肪標(biāo)記基因(UCP1、PGC-1α、PRDM16、CIDE-A等)在脂肪細(xì)胞中的表達(dá),并增加線粒體DNA含量。數(shù)據(jù)來(lái)自圖6、圖7和圖9。研究意義:證實(shí)ABA誘導(dǎo)白色脂肪棕色化,促進(jìn)產(chǎn)熱相關(guān)基因編程,可能有助于對(duì)抗肥胖和胰島素抵抗。
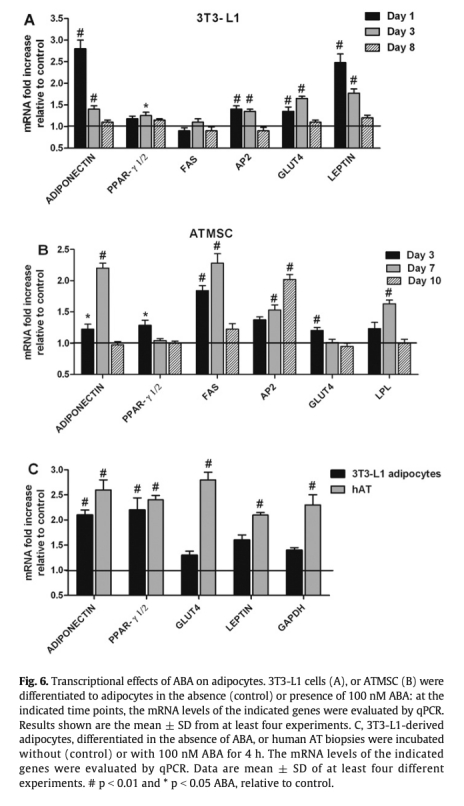
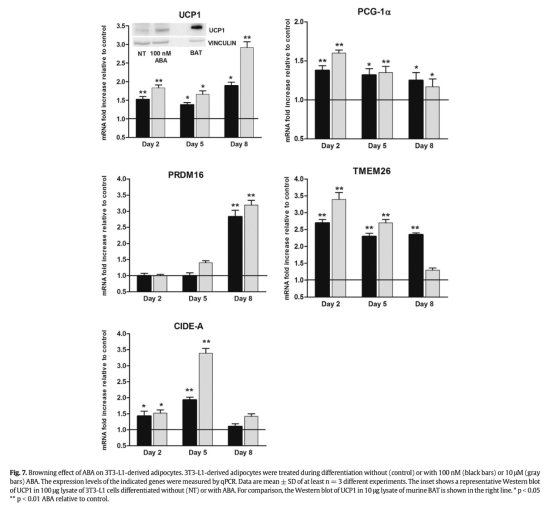
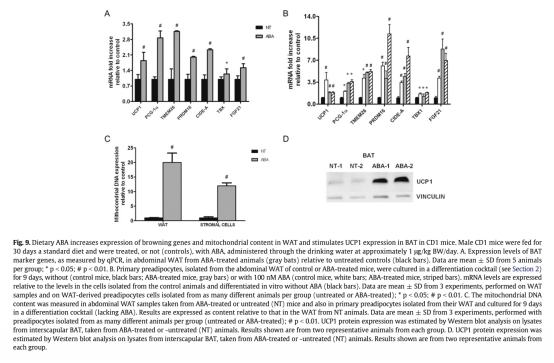
4 體內(nèi)葡萄糖攝取和組織變化:口服ABA(1μg/kg)增加大鼠棕色脂肪葡萄糖攝取(微PET顯示2倍升高),長(zhǎng)期處理上調(diào)小鼠白色脂肪棕色基因和線粒體含量。數(shù)據(jù)來(lái)自圖8和圖9。研究意義:顯示ABA在整體動(dòng)物水平激活棕色脂肪代謝,改善葡萄糖處置,提示其治療代謝疾病的潛力。
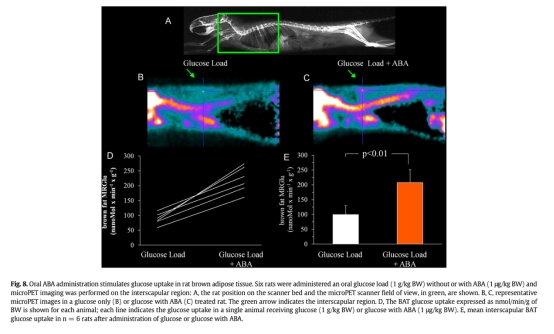
5 代謝產(chǎn)物測(cè)量:ABA減少脂肪細(xì)胞甘油三酯積累,但增加CO2產(chǎn)生,表明葡萄糖氧化增強(qiáng)而非脂質(zhì)儲(chǔ)存。數(shù)據(jù)來(lái)自圖5。研究意義:反映ABA促進(jìn)能量消耗型代謝,與棕色化表型相符,可能減少脂質(zhì)蓄積。
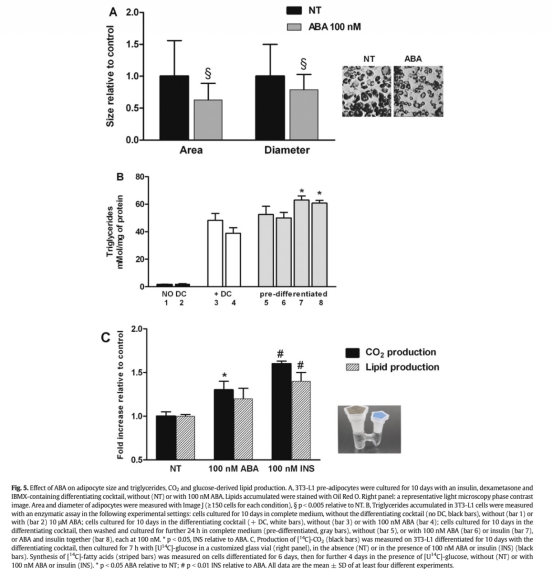
結(jié)論
論文得出結(jié)論:ABA通過(guò)LANCL2受體增強(qiáng)脂肪細(xì)胞葡萄糖攝取和氧消耗,誘導(dǎo)白色脂肪棕色化,上調(diào)產(chǎn)熱基因表達(dá)和線粒體生物發(fā)生。在體內(nèi),ABA激活棕色脂肪葡萄糖攝取和白色脂肪重塑,改善糖代謝。這些發(fā)現(xiàn)表明ABA可能作為調(diào)節(jié)能量平衡和糖耐量的新靶點(diǎn),為肥胖和糖尿病治療提供策略。
使用丹麥Unisense電極測(cè)量數(shù)據(jù)的研究意義
使用丹麥Unisense電極測(cè)量的氧消耗數(shù)據(jù)(圖2)為研究提供了關(guān)鍵的功能性證據(jù)。這些數(shù)據(jù)直接顯示ABA處理使3T3-L1脂肪細(xì)胞氧消耗率從22±2 nmol O2/min/mg蛋白增加到28±4 nmol O2/min/mg蛋白(增加約30%),表明ABA顯著增強(qiáng)細(xì)胞呼吸活性。研究意義在于:Unisense電極的高精度測(cè)量量化了ABA對(duì)代謝率的即時(shí)影響,支持ABA誘導(dǎo)產(chǎn)熱表型的假設(shè)。這種實(shí)時(shí)氧消耗監(jiān)測(cè)排除了間接因素干擾,直接 linking ABA處理到線粒體功能增強(qiáng)。結(jié)果與基因表達(dá)數(shù)據(jù)(如UCP1上調(diào))一致,共同證明ABA通過(guò)提升細(xì)胞呼吸促進(jìn)能量消耗。此外,該技術(shù)驗(yàn)證了ABA在脂肪代謝中的積極作用,為開發(fā)代謝疾病療法提供了實(shí)驗(yàn)依據(jù)。