熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Defects in mitochondrial energetic function compels Fanconi Anaemia cells to glycolytic metabolism
線粒體能量功能缺陷迫使范可尼貧血細胞轉向糖酵解代謝
來源:BBA- Molecular Basis of Disease, Volume 1863, 2017, Pages 1214-1221
《BBA-分子疾病基礎》,第1863卷,2017年,第1214-1221頁
摘要
這篇論文研究了范可尼貧血(FA)細胞能量代謝的缺陷,特別是線粒體氧化磷酸化(OXPHOS)功能受損如何導致細胞轉向糖酵解代謝。FA是一種遺傳性疾病,特征包括骨髓衰竭和癌癥易感性,與DNA修復缺陷和氧化應激相關。研究發現,FA細胞中線粒體復合物I到III的電子傳遞受損,降低了OXPHOS效率,但糖酵解通量增加以補償能量不足。同時,谷氨酰胺分解途徑減弱。強制FA細胞使用OXPHOS代謝會增加氧化應激和線粒體膜去極化,表明糖酵解是一種保護性適應機制。這項工作首次系統探討了FA能量代謝, linking這些缺陷 to骨髓衰竭。
研究目的
研究目的是探究FA細胞能量代謝的缺陷,特別是理解在OXPHOS受損的情況下,FA細胞如何通過替代代謝途徑(如糖酵解)產生ATP來維持細胞功能。同時,研究旨在揭示這些代謝變化與FA病理生理學(如骨髓衰竭)之間的關聯,為潛在治療策略提供見解。
研究思路
研究思路包括使用FA細胞系(Fanc-A淋巴oblast細胞),與野生型(Wt)和基因糾正的FA細胞(FA-corr)進行比較。通過測量氧消耗(使用丹麥Unisense電極)、ATP/AMP水平、糖酵解和TCA循環酶活性、乳酸釋放、NADH/NAD+比率以及氧化應激指標(如ROS和MDA),評估代謝狀態。使用藥物調制代謝,如rotenone(復合物I抑制劑)、antimycin A(復合物III抑制劑)、DCA和galactose(OXPHOS增強劑),以模擬代謝壓力。研究還通過Western blot分析AMPK磷酸化水平,以評估能量感應通路。
測量的數據及研究意義
1 氧消耗測量:使用Unisense電極測量細胞呼吸。數據顯示FA細胞基礎氧消耗低于對照組,對pyruvate+malate(激活復合物I-III-IV通路)的反應弱,但對succinate(激活復合物II-III-IV通路)的反應增強。這些數據來自Fig.1和Table 1。研究意義:表明FA細胞線粒體復合物I-III通路受損,但復合物II-IV通路代償性激活,揭示了OXPHOS缺陷的具體機制,為代謝重組提供證據。
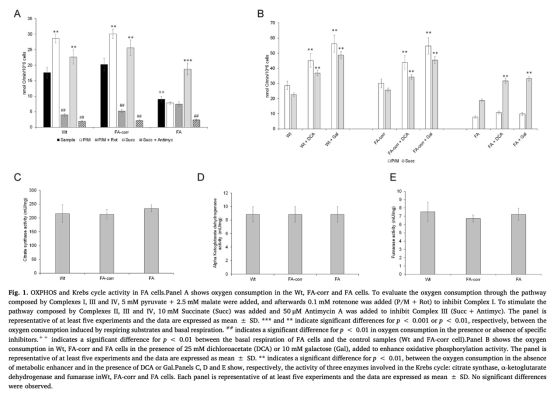
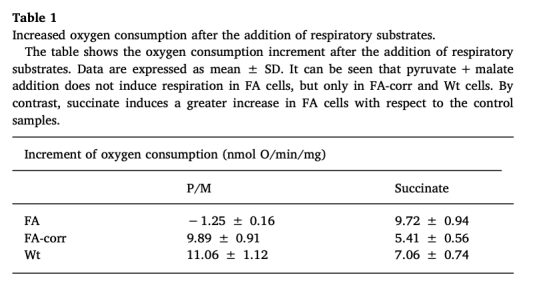
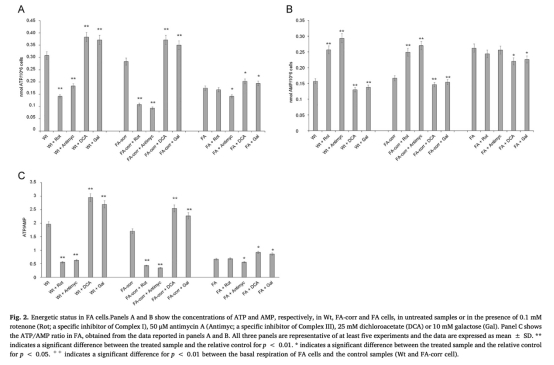
2 ATP和AMP水平:FA細胞顯示ATP濃度降低,AMP積累,ATP/AMP比率下降。數據來自Fig.2。研究意義:反映FA細胞能量狀態失衡,OXPHOS缺陷導致ATP生產不足,觸發AMPK激活以刺激替代能量途徑如糖酵解。
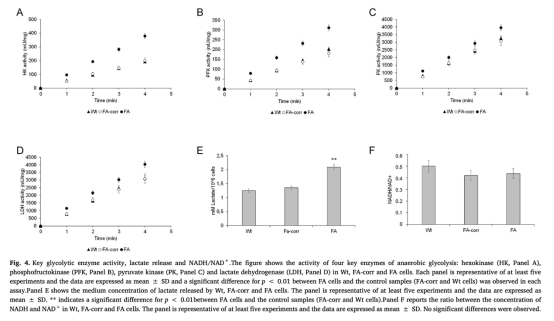
3 糖酵解酶活性和乳酸釋放:HK、PFK、PK和LDH活性在FA細胞中增加,乳酸釋放升高。數據來自Fig.4。研究意義:證實FA細胞依賴糖酵解作為主要能量來源,糖酵解通量增加有助于維持NAD+/NADH平衡,但能量效率低,可能與細胞未成熟狀態相關。
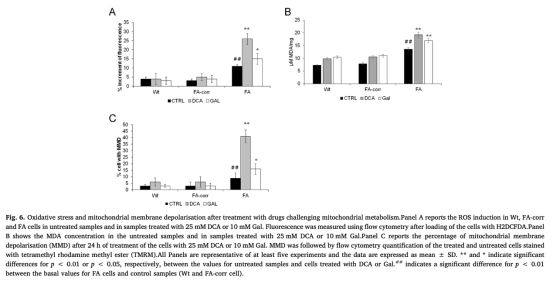
4 氧化應激指標:FA細胞基礎ROS和MDA水平升高,線粒體膜去極化增加。強制使用OXPHOS(如DCA處理)進一步加劇氧化應激。數據來自Fig.6。研究意義:表明OXPHOS缺陷導致氧化應激積累,強制代謝切換會損害細胞健康,這可能與FA中造血干細胞耗竭和骨髓衰竭相關。
結論
論文得出結論:FA細胞由于線粒體OXPHOS缺陷(特別是復合物I-III通路受損),被迫依賴糖酵解作為主要能量來源。這種代謝轉換是一種適應性反應,以維持細胞存活,但能量效率低,且強制回歸OXPHOS會增加氧化應激,可能導致造血干細胞在分化過程中耗竭,與FA的骨髓衰竭病理相關。研究強調了代謝缺陷在FA疾病機制中的核心作用。
使用丹麥Unisense電極測量數據的研究意義
使用丹麥Unisense電極測量的氧消耗數據提供了FA細胞線粒體呼吸功能的直接證據。測量顯示,FA細胞基礎氧消耗降低,且對pyruvate+malate(激活復合物I通路)的反應微弱,但對succinate(激活復合物II通路)的反應增強,這表明復合物I-III電子傳遞鏈特異性受損,而復合物II-IV通路代償性上調。這種測量方法的高靈敏度允許定量檢測細微的呼吸變化,揭示了FA細胞線粒體功能的不平衡。研究意義在于:Unisense電極的數據證實了OXPHOS缺陷的分子基礎,支持代謝重組假說,即FA細胞通過增強糖酵解來補償線粒體功能障礙。此外,這種實時呼吸測量有助于理解代謝適應性在疾病進展中的作用,為靶向代謝通路治療FA提供了理論依據。例如,強制FA細胞使用OXPHOS會加劇氧化應激,提示任何干預策略需謹慎避免破壞代謝平衡。