熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Visceral White Adipose Tissue after Chronic Intermittent and Sustained Hypoxia in Mice
慢性間歇性缺氧和持續性缺氧對小鼠內臟白色脂肪組織的影響
來源:American Journal of Respiratory Cell and Molecular Biology, Volume 56, Number 4, April 2017, pages 477-487
《美國呼吸細胞與分子生物學雜志》,第56卷,第4期,2017年4月,頁碼477-487
摘要
這篇論文研究了慢性間歇性缺氧(IH)和持續性缺氧(SH)對小鼠內臟白色脂肪組織(vWAT)的影響。摘要表明,IH和SH雖然都導致體重減輕,但誘導的胰島素抵抗程度不同,提示缺氧誘導因子(HIF)-1α活性存在差異。研究發現,IH引起vWAT血管稀疏、促炎巨噬細胞增加和胰島素抵抗,而SH則促進vWAT褐變和血管生成,并保持胰島素敏感性。機制上,SH能持續激活HIF-1α轉錄活性,而IH的早期HIF-1α激活隨時間的推移無法維持。這些發現揭示了IH和SH通過差異調節HIF-1α通路導致vWAT代謝功能的不同變化。
研究目的
本研究旨在比較IH和SH對vWAT代謝功能的影響,并探討HIF-1α信號通路在其中的作用。具體目的是確定IH和SH是否通過差異調節HIF-1α轉錄活性、血管生成、炎癥反應和脂肪細胞表型轉換,從而導致不同的胰島素敏感性和代謝結局。
研究思路
研究采用8周齡雄性C57BL/6J小鼠,將其暴露于IH(模擬阻塞性睡眠呼吸暫停的缺氧模式)、SH(持續性缺氧)或室內空氣(RA)中,持續6小時或6周。通過體內外實驗評估vWAT的胰島素敏感性(pAKT/AKT比值)、HIF-1α轉錄活性(染色質免疫沉淀測序)、血管生成(免疫組化)、脂肪細胞標志物基因表達(qPCR或微陣列)以及巨噬細胞極化(流式細胞術)。使用丹麥Unisense氧微電極測量組織氧分壓(tPO2),并通過統計學分析比較組間差異。
測量的數據及研究意義
1 體重和vWAT重量:IH和SH暴露6周后小鼠體重和vWAT重量均減輕(SH > IH > RA)。研究意義在于確認缺氧導致代謝消耗增加,但不同缺氧模式對體脂分布影響不同。數據來自圖2A。
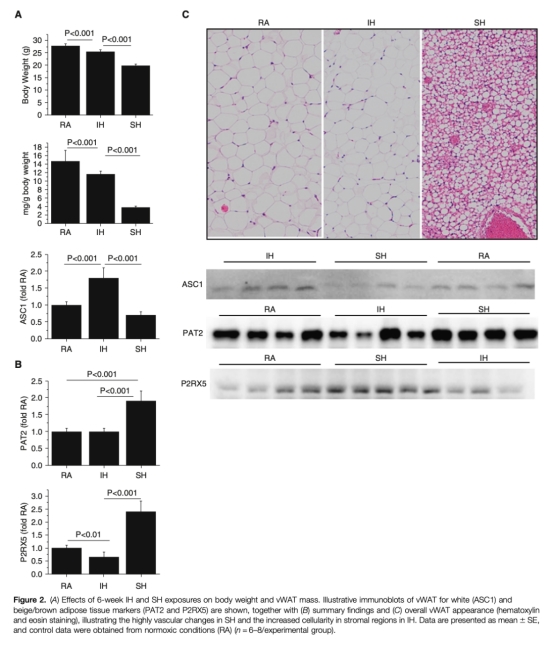
2 脂肪細胞表型標志物:IH組白色脂肪標志物ASC-1表達增加,SH組褐變標志物PAT2和P2RX5表達上調。研究意義表明IH促進vWAT白化,而SH誘導褐變,提示缺氧模式決定脂肪細胞分化方向。數據來自圖2B。
3 組織形態學:H&E染色顯示SH組vWAT呈現褐色脂肪樣 phenotype,IH組則出現細胞浸潤和炎癥。研究意義在于直觀展示缺氧模式對脂肪組織結構的差異影響。數據來自圖2C。
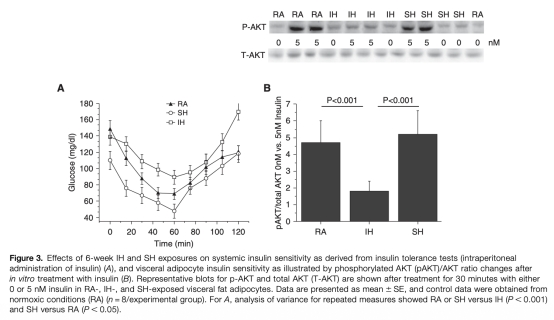
4 胰島素敏感性:IH組小鼠出現系統性胰島素抵抗和vWAT胰島素信號通路受損(pAKT/AKT降低),SH組則保持敏感。研究意義在于揭示IH特異性導致代謝功能障礙。數據來自圖3A和3B。
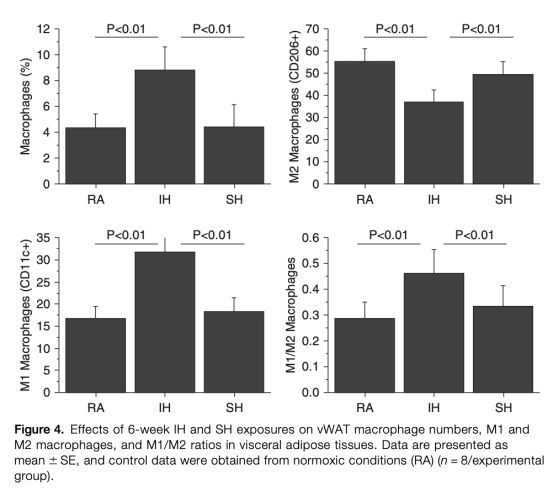
5 巨噬細胞浸潤:IH組vWAT中M1型促炎巨噬細胞增加,M2型減少,SH組無此變化。研究意義在于表明IH通過炎癥加劇胰島素抵抗。數據來自圖4。
6 血管生成相關指標:IH組VEGF、eNOS表達和CD31+毛細血管密度降低,SH組則升高。研究意義在于證明血管生成差異是代謝功能分化的關鍵。數據來自圖5A-5C。
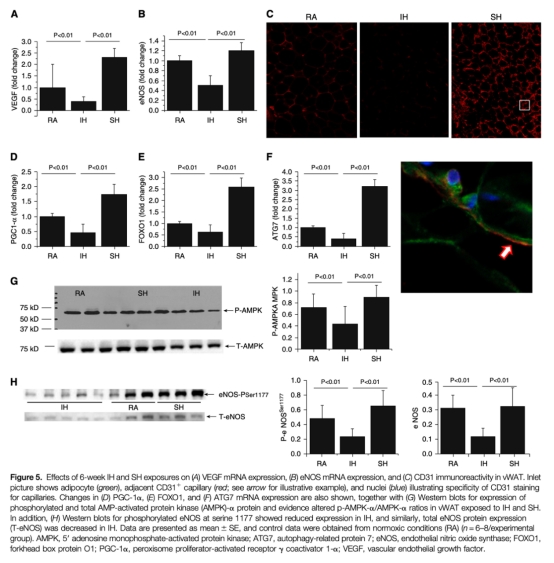
7 代謝調節因子:IH組PGC-1α、FOXO1、ATG7和p-AMPKα表達下降,SH組無變化或升高。研究意義在于提示IH抑制線粒體生物發生和自噬,導致代謝紊亂。數據來自圖5D-5G。
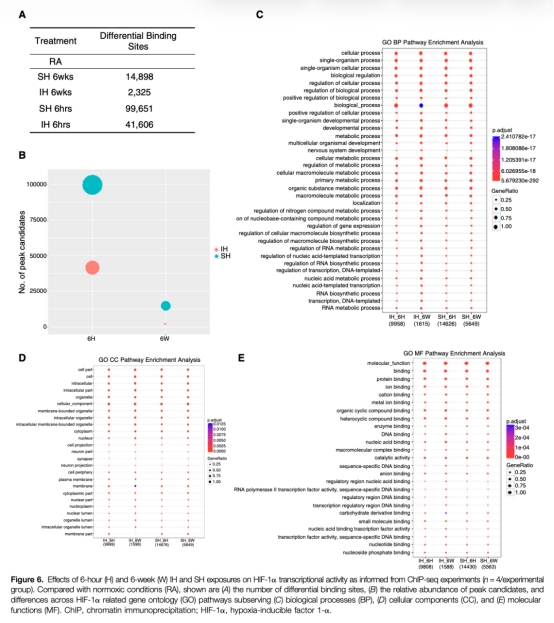
8 HIF-1α轉錄活性:ChIP-seq顯示SH組在6小時和6周時HIF-1α結合位點顯著增加,IH組早期激活但后期消失。研究意義在于明確HIF-1α持續性是決定代謝結局的核心因素。數據來自圖6。
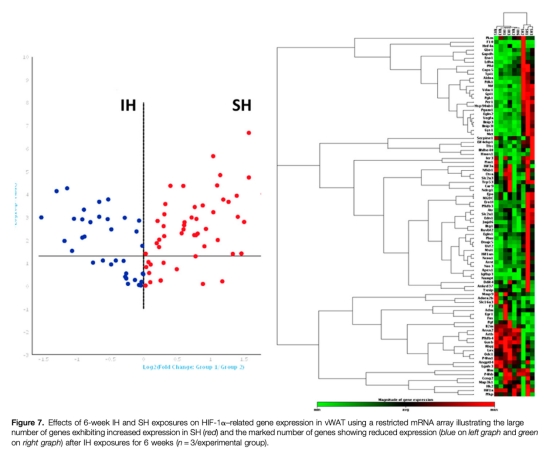
9 HIF-1α靶基因表達:微陣列顯示SH組多基因上調,IH組則下調。研究意義在于從轉錄組層面驗證HIF-1α通路活性的差異。數據來自圖7。
結論
1 IH通過誘導vWAT白化、血管稀疏、炎癥和胰島素抵抗促進代謝功能障礙,而SH通過褐變和血管生成保持代謝健康。
2 HIF-1α轉錄活性的持續性差異是IH和SH效應分化的關鍵機制,IH早期激活HIF-1α但無法維持,SH則實現持續激活。
3 研究提示阻塞性睡眠呼吸暫停相關的IH可能通過破壞HIF-1α通路驅動肥胖相關代謝疾病,為治療提供了新靶點。
使用丹麥Unisense電極測量數據的研究意義
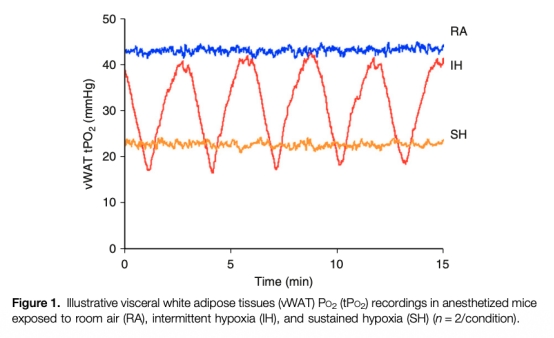
本研究使用丹麥Unisense氧微電極(型號OX-50)測量vWAT組織氧分壓(tPO2)。該電極具有高空間分辨率(50μm尖端)和快速響應時間(<2秒),能實時監測缺氧暴露下的局部氧動態。測量數據顯示,IH和SH模式下tPO2存在特征性差異(圖1),為缺氧模式的生理真實性提供了直接證據。Unisense電極的精確量化能力確保了IH(波動性缺氧)與SH(穩定缺氧)模型的可靠性,避免了間接推論的偏差。這一技術意義在于:首先,它驗證了不同缺氧暴露方案的生物效應差異源于實際的氧張力變化,而非其他混雜因素;其次,高分辨率測量為后續分子機制(如HIF-1α活性)研究奠定了堅實的生理學基礎;最后,該方法的應用強調了在代謝研究中直接監測組織微環境的重要性,為缺氧相關疾病模型的標準化提供了技術參考。