熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Effects of Nutrient Loading and Mercury Chemical Speciation on the Formation and Degradation of Methylmercury in Estuarine Sediment
營養負荷和汞的化學形態對河口沉積物中甲基汞的形成和降解的影響
來源:Environ. Sci. Technol. 2016, 50, 6983?6990
論文總結
一、論文摘要概述
本論文研究了營養負荷(氮和磷)和汞化學形態對河口沉積物中甲基汞(MeHg)形成和降解的影響。摘要指出,通過使用汞同位素示蹤劑在 brackish 水-沉積物 mesocosm 模型生態系統中的實驗,發現甲基汞的形成速率僅在對甲基化具有高可用性的汞形態(如易溶解的 Hg(II) 復合物)中隨營養負荷增加而增加;而對低可用性汞形態(如與天然有機質結合的 Hg(II))無顯著響應。這表明甲基汞的形成受微生物活動(間接由營養負荷促進的浮游生物生產驅動)和汞化學形態的共同控制。研究強調了在預測海洋沉積物中汞生物地球化學循環時,需同時考慮環境因素和汞的化學特異性。
二、研究目的
本研究的主要目的包括:
評估營養負荷的效應:探究向水體添加營養鹽(N 和 P)如何通過促進浮游生物生產,間接影響沉積物中甲基汞的形成和降解。
闡明汞化學形態的作用:比較不同化學形態的汞(如易溶解汞與結合態汞)對甲基化過程的響應,識別高可用性和低可用性汞庫。
揭示機制交互作用:理解營養負荷與汞形態的交互如何調控凈甲基汞產量,為管理汞污染提供理論依據。
三、研究思路
研究采用 mesocosm 模型生態系統與同位素示蹤結合的系統方法:
實驗設計:在室內建立 6 個大型 mesocosm 系統(5 m 高,0.75 m 直徑),模擬河口環境。系統包含沉積物核心和水柱,控制溫度(上層 15°C,下層 10°C)、光照(12 小時光暗循環)和營養添加(低濃度第 1-2 周,高濃度第 3-4 周)。
汞示蹤劑添加:
原位添加:將預平衡的汞同位素示蹤劑(如 β-201HgSsed、200HgII-NOMsed)注入沉積物或加入水柱,模擬不同化學形態汞(如硫化物結合態、NOM 結合態)。
離體添加:在沉積物 slurry 培養實驗中添加易溶解汞示蹤劑(如 204HgII(aq)),測量甲基化速率常數(km)和去甲基化速率常數(kd)。
采樣與測量:定期采集水體和沉積物樣品,測量葉綠素 a、營養鹽濃度、初級生產速率,以及汞形態濃度(使用 ICP-MS 和 GC-ICP-MS)。
環境監測:使用丹麥 Unisense 微電極傳感器集成到 CTD 系統中,原位測量水柱的溶解氧(DO)飽和度和沉積物氧滲透深度(OPD),以表征氧化還原條件(方法部分)。
數據分析:通過統計模型(如 ANOVA)和相關性分析,評估營養負荷、汞形態與甲基汞通量的關系。
四、測量數據及研究意義(注明來源)
本研究測量了多類數據,其來源和意義如下:
初級生產與葉綠素 a 動態(來自 Figure 1a):
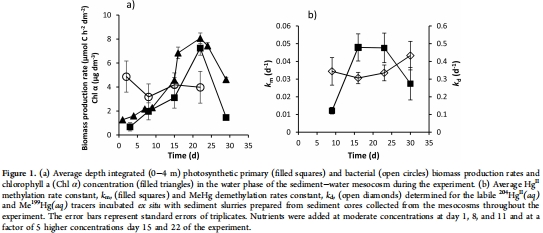
數據:Figure 1a顯示葉綠素 a 濃度和初級生產速率隨營養添加而增加,在第 22 天達峰值(葉綠素 a ~2.5 μg dm?3,初級生產 ~8 μmol C dm?2 h?1),隨后因浮游動物捕食下降。
研究意義:這些數據直接證實營養負荷促進了浮游生物 blooms,增加了有機質沉積,從而間接刺激沉積物微生物活動。葉綠素 a 作為生物量代理,與甲基化速率顯著相關(R2=0.96),突出了底棲-水體耦合在汞循環中的關鍵作用。
汞甲基化與去甲基化速率(來自 Figure 1b):
數據:Figure 1b顯示易溶解汞示蹤劑(204HgII(aq))的甲基化速率常數(km)在營養負荷增加期(第9-16天)上升約4倍,而去甲基化速率(kd)變化較小(<40%)。
研究意義:km 的急劇增加表明高可用性汞形態對微生物活動敏感,支持“電子供體假說”——營養負荷通過增加新鮮有機質輸入,激活甲基化菌。kd 的穩定性提示去甲基化過程受其他因素主導,如光降解或細菌群落結構。
凈甲基汞形成比率(來自 Figure 2 和 Figure 3):
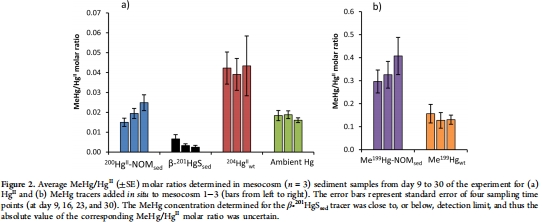
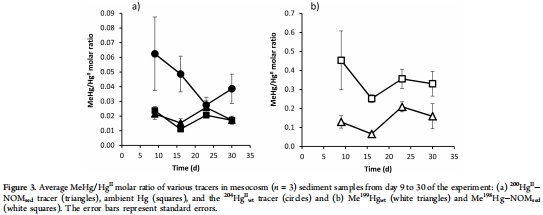
數據:Figure 2a顯示不同汞示蹤劑的 MeHg/HgII 摩爾比差異顯著:204HgIIwt(水柱添加)最高(0.041),200HgII-NOMsed(沉積物添加)中等(0.020),β-201HgSsed 最低(0.004)。Figure 3顯示比率隨時間變化,水柱添加示蹤劑響應更明顯。
研究意義:這些比率揭示汞化學形態的“分級響應”:高可用性汞(如溶解態)凈甲基化強,而低可用性汞(如硫化物結合態)幾乎無響應。這解釋了野外觀測中甲基汞變異的機制,強調了汞形態分析在風險評估中的重要性。
環境參數(來自方法部分和附表):
數據:測量了溶解氧(DO)、氧滲透深度(OPD)、沉積物孔隙度、C/N 比等。例如,OPD 為 1-2 mm,指示氧化層薄;C/N 比下降(從 10.7 到 8.6)反映自生有機質輸入增加。
研究意義:這些參數關聯氧化還原條件與汞轉化:低 OPD 和缺氧環境促進厭氧甲基化菌活動,而 C/N 比變化指示有機質質量調控微生物代謝底物。
五、研究結論
本研究主要結論如下:
營養負荷的選擇性效應:營養添加僅增強高可用性汞形態(如溶解 Hg(II))的甲基化,對低可用性形態(如 HgS 或 NOM 結合態)影響不顯著,表明汞生物可用性是限制因子。
微生物活動的核心作用:營養負荷通過增加浮游生物生產,沉積新鮮有機質,為甲基化菌提供電子供體,間接驅動甲基汞形成,支持“生物活動假說”。
化學形態的決定性:汞的化學形態(如溶解態 vs. 結合態)控制其甲基化潛力,高可用性汞庫在富營養化環境中更易轉化為甲基汞,增加生態風險。
管理啟示:預測汞風險需同時考慮營養負荷和汞形態分布,富營養化水域中,高可用性汞污染可能加劇甲基汞積累。
六、丹麥Unisense電極測量數據的詳細研究意義
本研究中使用的丹麥Unisense氧微電極數據具有關鍵研究意義,盡管未在圖表中直接展示,但方法部分提及其用于監測環境條件:
氧化還原梯度量化:Unisense電極以高分辨率實時測量水柱溶解氧(DO)飽和度和沉積物-水界面的氧滲透深度(OPD)。這些數據提供了沉積物氧化狀態的直接指標,例如OPD約1-2 mm,表明表層沉積物為氧化層,深層為缺氧區,這直接影響汞甲基化菌(如硫酸鹽還原菌)的活性區分布。
關聯環境條件與生物地球化學:DO和OPD數據幫助確認沉積物為鐵還原至低硫化物條件(溶解硫化物<0.05-1.0 μM),這種缺氧環境是汞甲基化的熱點。Unisense測量驗證了mesocosm系統的生態真實性,確保實驗結果可外推至自然河口環境。
支持機制解釋:通過DO動態,研究間接推斷營養負荷促進有機質礦化,消耗氧氣,加深缺氧層,從而創造更有利的甲基化條件。Unisense數據彌補了化學測量的不足,為“營養負荷→缺氧→甲基化增強”的因果鏈提供物理化學證據。
技術優勢:Unisense電極的原位、無損測量避免了采樣擾動,提供了連續氧數據,增強了時間序列分析的可靠性。在汞循環模型中,這些數據可作為關鍵輸入參數,預測氣候變化下(如變暖加劇缺氧)甲基汞產率變化。
總之,丹麥Unisense電極數據雖未直接參與汞通量計算,但通過表征氧化還原環境,為理解營養-汞交互作用提供了底層機制支持,突出了多參數監測在復雜生物地球化學研究中的價值。