熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Monitoring Biodegradation of Magnesium Implants with Sensors
利用氫氣傳感器監測鎂植入物材料的生物降解
來源:JOM, Vol. 68, No. 4, 2016
論文摘要總結
本研究聚焦于鎂及其合金作為生物可降解金屬植入材料的應用,利用傳感器實時監測其腐蝕過程。鎂的腐蝕產物包括鎂離子(Mg2?)、氫氧根離子(OH?)和氫氣(H?)。論文開發了一種腐蝕表征系統(CCS),集成自制毛細管pH和Mg2?微傳感器,用于體外實時監測鎂腐蝕。同時,采用氫氣傳感器通過無創方式監測體內鎂合金的降解,利用氫氣的高皮膚滲透性,在皮膚表面檢測皮下植入物產生的H?。該系統為鎂基植入物的生物降解評估提供了創新工具。
研究目的
本研究旨在解決鎂合金植入物降解過程監測的挑戰,傳統方法(如重量損失、氫收集、pH測量等)無法實時、多參數跟蹤。具體目標包括:
開發多傳感器平臺:構建CCS系統,同步測量pH、Mg2?濃度、溶解H?及電化學阻抗譜(EIS),實現體外腐蝕的實時分析。
實現體內無創監測:利用氫氣傳感器,通過透皮檢測H?,跟蹤皮下鎂植入物的降解速率,避免二次手術或大型影像設備依賴。
優化傳感器微型化:研制毛細管微電極,提升空間分辨率,適用于生物醫學環境中的局部測量。
研究思路
研究思路分為四個階段:
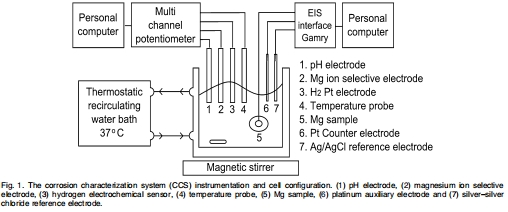
系統構建與優化:設計CCS系統(圖1),集成pH電極、Mg2?離子選擇電極、H?電化學傳感器、溫度探頭和參比電極,在恒溫(37°C)攪拌條件下進行腐蝕實驗。系統通過Ag/AgCl參比電極確保電位穩定性。
微傳感器開發:基于玻璃毛細管制備pH和Mg2?微電極(圖2),尖端直徑約50μm,內部填充MgCl?溶液和離子選擇性膜,提升生物相容性和空間分辨率。微電極通過校準驗證線性響應。

體外腐蝕監測:在0.9% NaCl溶液中測試99.9%鎂的腐蝕,實時記錄pH變化、Mg2?釋放及EIS譜圖,分析腐蝕動力學和表面膜形成。
體內驗證:使用Unisense H?微傳感器在小鼠模型中監測皮下植入鎂單晶產生的H?,通過透皮測量繪制H?濃度分布圖,評估無創監測可行性。
測量數據及研究意義
以下關鍵數據均來自論文中的圖表,其研究意義如下:
pH微電極校準與腐蝕響應(圖3a-b)
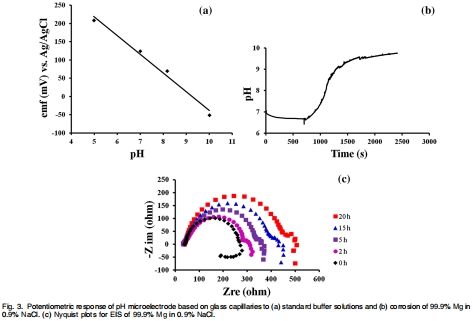
數據來源:圖3a顯示pH微電極在pH 5-10緩沖液中的校準曲線(電位vs. pH);圖3b展示鎂在0.9% NaCl中腐蝕時pH隨時間的變化。
研究意義:校準曲線線性良好(R2=0.99),證明微電極的準確性(圖3a)。腐蝕實驗中pH在浸入后700秒內迅速從基線升至約9(圖3b),表明OH?快速生成,隨后Mg(OH)?沉淀減緩腐蝕。意義:實時反映腐蝕起始和鈍化過程,為降解速率提供動態指標。
電化學阻抗譜(EIS)數據(圖3c)
數據來源:圖3c顯示鎂在0.9% NaCl中腐蝕0-20小時的Nyquist圖。
研究意義:高頻區電容環直徑隨浸泡時間增加,表明電荷轉移電阻(Rct)和表面膜電阻(Rf)增大,反映Mg(OH)?保護層的形成。意義:EIS與傳感器數據互補,揭示腐蝕產物對金屬的保護作用,增強腐蝕機制的理解。
氫氣微傳感器空間映射(圖4)
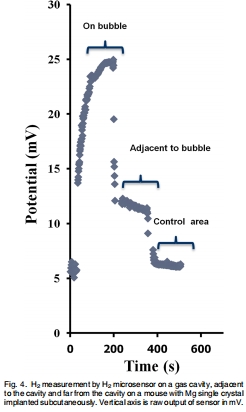
數據來源:圖4展示H?微傳感器在小鼠皮下植入鎂合金部位測量的H?濃度(原始輸出電壓mV),包括氣體腔正上方、鄰近區域和遠離區域的對比。
研究意義:傳感器響應快速(<1分鐘),氣體腔上方H?濃度最高,鄰近區域顯著降低,遠處幾乎無信號(圖4)。意義:證實H?可透皮擴散,且濃度梯度反映腐蝕局部性,為體內降解提供空間分辨率。
微電極結構驗證(圖2)
數據來源:圖2a為pH和Mg2?微電極示意圖,圖2b顯示實際微電極照片。
研究意義:微電極尖端微小(~50μm),支持局部測量,避免整體溶液干擾。意義:為未來活體細胞水平監測或表面掃描顯微鏡應用奠定基礎,提升腐蝕研究的空間精度。
結論
本研究成功開發并驗證了多傳感器監測平臺,主要結論如下:
CCS系統有效性:實時同步監測pH、Mg2?、H?和EIS,全面捕捉鎂腐蝕動力學,體外實驗顯示pH驟升和膜形成過程。
微傳感器優勢:毛細管微電極具高空間分辨率,適用于生物環境,pH和Mg2?測量線性可靠。
無創體內監測:Unisense H?傳感器實現透皮檢測,響應快且能映射H?分布,證明其作為體內降解跟蹤工具的可行性。
應用前景:該方法簡化了監測流程,替代昂貴影像設備(如X射線、Micro-CT),為鎂基植入物的臨床評估提供低成本、高時效方案。
丹麥Unisense電極測量數據的詳細解讀
在研究中,丹麥Unisense H?微傳感器(50μm尖端直徑)被用于測量鎂腐蝕產生的氫氣,其研究意義如下:
無創體內監測的創新性:Unisense傳感器通過極化于+1000 mV,檢測皮下氣體腔中的H?濃度(圖4)。數據顯示,傳感器可直接按壓于皮膚表面獲得信號,無需侵入性操作,與腔內測量結果高度一致。這證實了H?的高皮膚滲透性,突破了傳統體內監測需手術或成像設備的限制。意義:首次實現鎂植入物降解的透皮實時跟蹤,為臨床長期監測提供新范式。
高時空分辨率與快速響應:傳感器響應時間<1分鐘,能快速捕捉H?動態變化。空間映射顯示,氣體腔上方信號最強,鄰近區域濃度下降50%以上,遠處幾乎無響應(圖4)。意義:不僅驗證腐蝕局部性,還提示降解速率的空間異質性,有助于評估植入物與組織交互影響,為優化植入設計提供數據支持。
定量關聯降解速率:每摩爾鎂腐蝕產生1摩爾H?(方程1),因此H?濃度直接正比于降解量。Unisense測量顯示,信號強度與腐蝕程度相關,且長期測試中信號變化可反映降解速率波動(如鈍化膜形成后的減緩)。意義:將H?濃度轉化為定量降解指標,彌補了傳統方法(如重量損失)無法實時跟蹤的缺陷。
技術優勢與臨床潛力:Unisense傳感器具高靈敏度(pA級電流檢測),適用于微量H?測量。結合透皮特性,該方法簡化了監測流程,降低成本和患者風險。意義:為鎂合金植入物的個性化醫療提供工具,如跟蹤愈合過程中的降解匹配,避免過早或過晚降解導致的并發癥。
總之,Unisense電極的應用不僅是檢測工具的創新,更推動了生物可降解材料監測向無創、實時、定量化發展,凸顯其在轉化醫學中的關鍵價值。