熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
SYNAPTIC TRANSMISSION DESPITE SEVERE HYPOXIA IN HIPPOCAMPAL SLICES OF THE DEEP-DIVING HOODED SEAL
深潛水海豹海馬切片在嚴重缺氧下的突觸傳遞
來源:Neuroscience, Volume 334, 2016, Pages 39-46
《神經科學》第334卷,2016年,第39-46頁
摘要:
論文摘要指出深潛水冠海豹的腦神經元具有固有的缺氧耐受性。研究通過體外場電位記錄比較海豹與非潛水哺乳動物(小鼠和馴鹿)海馬切片在嚴重缺氧下的突觸傳遞。結果顯示,海豹切片在3小時缺氧下能維持突觸活動(幅度>30%正常值),而小鼠和馴鹿的突觸活動迅速消失且無法恢復。AMPA型谷氨酸受體拮抗劑CNQX消除了海豹的信號,證實其為真實的突觸反應。海豹的配對脈沖促進(PPF)減弱,表明突觸前鈣離子(Ca2+)積累可能受限,可能與高鈣緩沖能力有關,這解釋了海豹神經元的缺氧耐受性。盡管鈣結合蛋白calbindin d28k或parvalbumin的mRNA表達無顯著上調,但近期研究顯示海豹S100B鈣結合蛋白轉錄水平高,支持這一假設。
研究目的:
研究目的是調查海豹突觸傳遞在嚴重缺氧下的耐受性,比較其與非潛水哺乳動物(小鼠和馴鹿)的差異,并探討鈣離子調節在缺氧耐受中的作用。具體目標包括:a) 評估海豹是否能維持突觸傳遞在缺氧條件下;b) 檢查海豹的PPF是否減弱;c) 測試PPF差異是否反映鈣結合蛋白表達變化。
研究思路:
研究思路采用體外海馬切片技術,記錄CA1區的場興奮性突觸后電位(fEPSP)。比較深潛水冠海豹、小鼠和馴鹿的切片,暴露于嚴重缺氧條件(95% N2/5% CO2),使用丹麥Unisense電極監測氧含量以確保缺氧嚴重性(氧分壓降至<3% within 3 min)。測量fEPSP幅度、PPF以及鈣結合蛋白基因表達(通過RT-qPCR)。數據分析包括統計比較fEPSP變化、PPF幅度和基因表達差異,以驗證缺氧耐受機制。
測量的數據及研究意義:
1 測量了fEPSP幅度在缺氧下的變化:海豹切片在3小時缺氧下維持>30%幅度,且再氧合后恢復至~50%,而小鼠和馴鹿切片在4-6分鐘內突觸活動消失且無恢復。數據來自圖1、圖2和圖3。研究意義是直接證明海豹突觸傳遞具有卓越的缺氧耐受性,為非潛水物種提供對比,突顯海豹的神經適應機制。
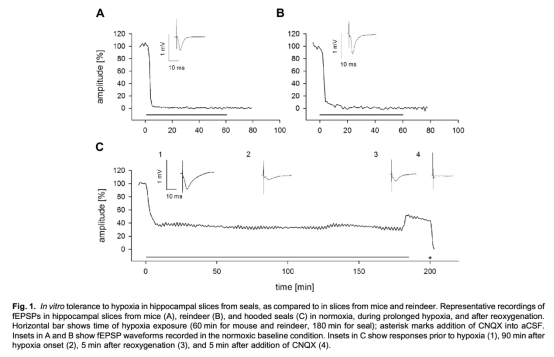
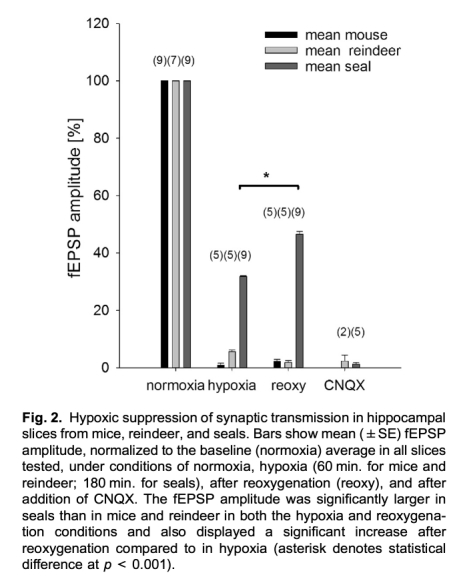
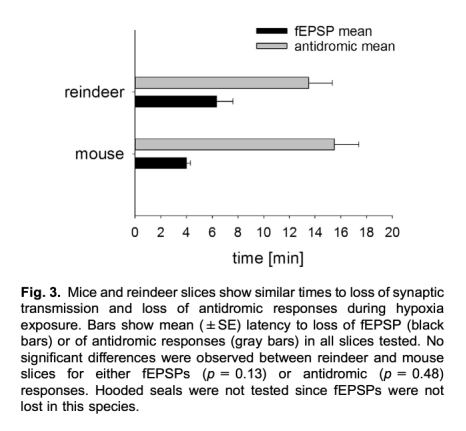
2 測量了配對脈沖促進(PPF):海豹切片的PPF顯著減弱(第二脈沖幅度<120%),而小鼠和馴鹿顯示正常PPF(140-160%)。數據來自圖4。研究意義是表明海豹突觸前鈣離子內流可能受限,減少興奮性毒性,這可能是缺氧耐受的關鍵因素。
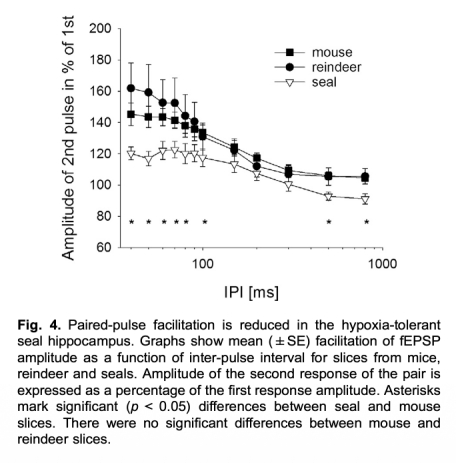
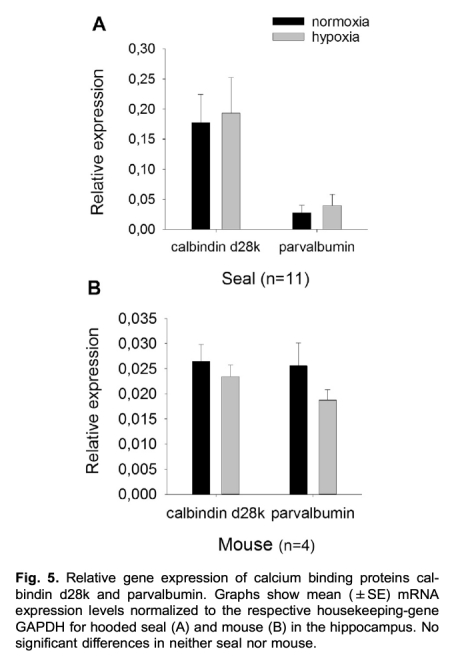
3 測量了鈣結合蛋白基因表達:通過RT-qPCR分析calbindin d28k和parvalbumin的mRNA,在缺氧和常氧下無顯著差異。數據來自圖5。研究意義是雖然未發現誘導性變化,但提示海豹可能具有組成型高鈣緩沖能力(如S100B),支持PPF減弱和缺氧耐受的假設。
結論:
1 海豹海馬切片在嚴重缺氧下能維持突觸傳遞長達3小時,而小鼠和馴鹿的突觸活動迅速失效,表明海豹具有內在的神經缺氧耐受性。
2 海豹的PPF減弱,提示突觸前鈣離子調節改變,可能通過高鈣緩沖能力限制鈣積累,減少缺氧損傷。
3 鈣結合蛋白表達分析未顯示缺氧誘導變化,但結合S100B的高表達,海豹的缺氧耐受可能與組成型增強的鈣緩沖機制有關。
使用丹麥Unisense電極測量數據的研究意義:
丹麥Unisense電極(Clark型氧分壓微傳感器,型號OX25)用于實時監測記錄室中的氧分壓(PO2),確保實驗條件的嚴格控制。測量數據顯示,缺氧后氧含量在3分鐘內降至<3%,10分鐘內降至<1%,驗證了嚴重缺氧環境的建立。研究意義在于排除了氧濃度波動的混淆因素,保證了缺氧挑戰的一致性和可靠性,使fEPSP和PPF結果更具說服力。通過精確量化缺氧程度,該電極數據支持了海豹突觸耐受性的真實性,并有助于區分生理響應與實驗偽跡,為缺氧機制研究提供了關鍵的環境控制證據。