熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Diverse electron sources support denitrification under hypoxia in the obligate methanotroph Methylomicrobium album strain BG8
不同的電子源支持專性嗜甲烷菌 Methylomicrobium album 菌株 BG8 在缺氧下的反硝化作用
來源:Front. Microbiol. 6:1072.
論文摘要
本研究探討了專性嗜甲烷菌 Methylomicrobium album菌株 BG8 在缺氧條件下利用多種電子源支持反硝化作用的能力。研究發現,BG8 菌株能夠利用甲烷、甲醇、甲醛、甲酸、乙烷、乙醇和氨作為電子供體,在亞硝酸鹽(NO??)存在下于缺氧環境中驅動反硝化過程,產生氧化亞氮(N?O)。轉錄組分析顯示,反硝化相關基因(如 nirS和 norB1)的表達在 NO?? 添加后顯著上調,同時一個推測的銅單加氧酶基因 pxmA的表達也受低氧和 NO?? 誘導。結果表明,嗜甲烷菌通過表達反硝化基因庫,能夠在氧限制下將底物氧化與氮氧化物還原偶聯,擴展了其對環境變化的代謝靈活性認知。
研究目的
本研究旨在:
驗證 M. albumBG8 是否能利用多種電子源(包括 C1 化合物、C2 化合物和無機氮源)在缺氧條件下支持反硝化活性。
確定反硝化過程的環境調控因素,特別是氧張力和 NO?? 可用性的作用。
評估 BG8 菌株反硝化基因(如 nirS、norB)和潛在新基因(如 pxmA)的表達響應。
闡明嗜甲烷菌在氮循環中的生態角色,尤其是其對 N?O 排放的潛在貢獻。
研究思路
研究采用多方法結合的實驗策略:
菌株培養與處理:在硝酸鹽礦物鹽培養基(NMS)中培養 BG8 菌株,設置對照(僅 NMS)和實驗組(添加 1 mM NaNO?),在控制氧張力(初始約 21% O?)下監測 120 小時。
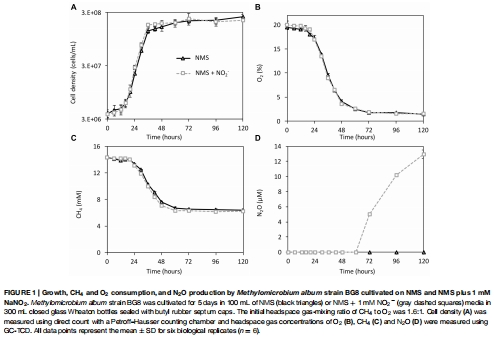
氣體動態監測:使用氣相色譜(GC-TCD)定期測量培養瓶頂空中的 O?、CH? 和 N?O 濃度,評估生長、底物消耗和反硝化產物生成(圖1)。
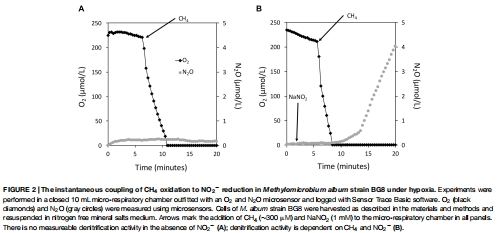
微傳感器瞬時測量:在微呼吸室(10 mL)中,使用丹麥Unisense O? 微電極和N?O 微傳感器同步監測休眠細胞在添加不同電子源(如 CH?、CH?OH、NH?Cl 等)后的溶解 O? 消耗和 N?O 生成速率(圖2、3、4)。
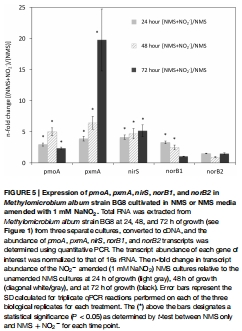
基因表達分析:通過 RNA 提取和定量 PCR(qPCR)測量反硝化基因(nirS、norB1、norB2)和代謝基因(pmoA、pxmA)的轉錄水平,比較 NO?? 添加組與對照組的差異(圖5)。
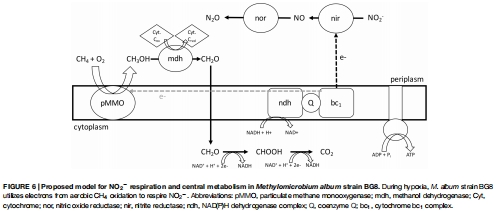
數據整合:將氣體通量數據與基因表達關聯,構建反硝化代謝模型(圖6)。
測量的數據、研究意義及來源
研究測量了多類數據,以下按類別說明其意義及圖表來源(注明圖表):
生長與氣體代謝數據:
數據內容:BG8 在添加 NO?? 后生長不受抑制,但 O? 消耗加速,且在 O? 降至約 1.8% 時開始產生 N?O(72 小時);N?O 產率達 5.1% 從添加的 NO??(100 μmol)。無 NO?? 組無 N?O 檢測。
研究意義:直接證明反硝化嚴格依賴缺氧和 NO??,且不影響菌株正常生長,凸顯 BG8 的代謝穩健性。數據來自圖1A-D(生長曲線和氣體變化)。
微傳感器瞬時O?與N?O通量數據:
數據內容:在微呼吸室中,添加 CH? 后 O? 在 3 分鐘內耗盡,隨后 NO?? 還原產生 N?O(速率 7.9 × 10?1? mol cell?1 h?1)。類似趨勢見于其他底物(如甲醇、乙烷、氨),N?O 生成與底物添加量成正比。
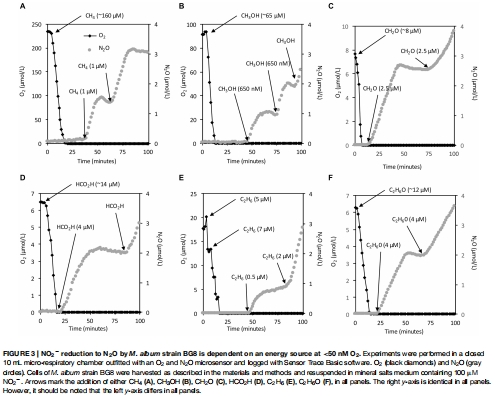
研究意義:提供電子源與反硝化活性的直接耦合證據,表明多種底物可通過共同酶學途徑驅動氮氧化物還原。數據來自圖2A-F(各底物下的 O?/N?O 曲線)和圖3(底物劑量響應)。
氨氧化耦合反硝化數據:
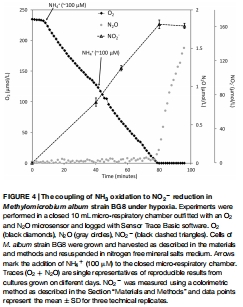
數據內容:添加 NH?? 后,O? 快速消耗,NO?? 積累至 163 μM,缺氧后 N?O 以 1.2 × 10?1? mol cell?1 h?1 速率生成。
研究意義:揭示無機氮源(氨)也可支持反硝化,擴展了嗜甲烷菌的能量獲取策略。數據來自圖4(NH?? 添加實驗)。
基因表達數據(qPCR):
數據內容:NO?? 添加組中 nirS和 norB1轉錄水平在 24-48 小時顯著升高(如 nirS增加 4.5 倍),pxmA在 72 小時上調 19.8 倍;pmoA(甲烷氧化基因)表達穩定。
研究意義:從分子層面證實反硝化基因對 NO?? 的特異性響應,提示 pxmA可能參與缺氧適應。數據來自圖5(基因表達柱狀圖)。
研究結論
M. albumBG8 在缺氧和 NO?? 存在下能進行反硝化,產生 N?O,且過程依賴多種電子源(C1/C2 化合物及氨),體現其顯著的代謝可塑性。
反硝化活性由基因表達調控驅動:nirS和 norB1對 NO?? 響應靈敏,而 pxmA的上調暗示其可能參與新型缺氧應激途徑。
嗜甲烷菌的反硝化能力可能影響自然環境中氮循環,尤其在氧限制生境(如濕地、沉積物)中貢獻于 N?O 排放。
研究為工程化利用嗜甲烷菌于溫室氣體減排(如 CH? 和 N?O 協同控制)提供了理論基礎。
詳細解讀使用丹麥Unisense電極測量出來的數據的研究意義
在本文中,使用丹麥Unisense O? 微電極和N?O 微傳感器測量的數據具有關鍵研究意義,其詳細解讀如下:
高時空分辨率實時監測代謝動態:Unisense 微傳感器是一種電化學傳感器,具備高靈敏度(檢測限達納摩爾級)和快響應時間(秒級)。本研究將其集成于微呼吸室,以秒級間隔同步測量溶解 O? 和 N?O 的濃度變化(如圖2A顯示 O? 在 3 分鐘內耗盡)。這種實時原位監測能力避免了傳統終點取樣的時間模糊性,直接捕捉了反硝化啟動的精確時刻(O? 耗盡后立即發生),為“缺氧觸發反硝化”的假設提供了動態證據。
定量驗證電子源與反硝化的直接耦合:通過添加不同底物(如 CH?、CH?OH、NH??)后記錄 O? 消耗和 N?O 生成曲線(圖2-4),Unisense 數據將抽象的“電子供體”轉化為可量化的通量速率。例如,數據顯示所有測試底物均能支持相似的 N?O 產率,證明 BG8 的反硝化酶系具有廣譜底物適應性。這種精確量化是推導代謝模型(圖6)的基礎。
揭示反硝化的瞬時調控機制:微傳感器數據顯示,N?O 生產僅在 O? 降至檢測限(<50 nM)后開始(圖2B),強有力地證實了反硝化對缺氧的絕對依賴性。同時,O? 消耗速率與底物類型相關(如 CH? 最快),將電子流效率與反硝化活性關聯,支持了“反硝化作為缺氧備用呼吸鏈”的生理模型。
方法學優勢與可靠性:Unisense 傳感器的原位校準(用無氧和空氣飽和溶液)和微創測量確保了數據準確性。在本文中,其與 GC 數據互補(如圖1),通過高時間分辨率驗證了批量培養的整體趨勢,凸顯了微傳感器在解析瞬時微生物過程中的不可替代性。
總之,丹麥Unisense電極的數據不僅是本研究中驗證反硝化活性的技術基石,更通過提供高精度實時通量信息,揭示了嗜甲烷菌在缺氧下的代謝切換機制,為理解微生物在碳氮耦合循環中的功能提供了關鍵見解。