熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Furosemide-induced urinary acidification is caused by pronounced H+ secretion in the thick ascending limb
呋塞米誘導的尿液酸化是由厚升支粗段顯著的H+分泌引起的
來源:Am J Physiol Renal Physiol. Volume 309, Issue 2, 2015
《美國生理學雜志-腎臟生理學》,第309卷第2期,2015年
摘要
這篇論文研究了呋塞米(一種袢利尿劑)誘導尿液酸化的機制。傳統觀點認為,呋塞米通過抑制厚升支粗段(TAL)的NaCl重吸收,增加遠端小管的Na+負荷,從而激活α-間介細胞(α-IC)的H+-ATPase介導的H+分泌。但本研究提出,TAL本身直接參與尿液酸化。通過體外實驗,發現呋塞米引起小鼠髓質TAL(mTAL)細胞內堿化和顯著的H+分泌,這被管腔阿米洛利和NHE3特異性拮抗劑#4167抑制。體內實驗顯示,NHE3抑制顯著減少呋塞米誘導的尿液酸化和凈酸排泄(NAE),且ENaC抑制后尿液酸化仍部分存在。結論是呋塞米通過激活TAL的頂端NHE3直接誘導H+分泌,修訂了對腎臟酸處理機制的理解。
研究目的
研究目的是探究呋塞米誘導尿液酸化的具體機制,特別是驗證TAL是否直接參與H+分泌,而非僅通過遠端小管的電壓驅動機制。挑戰傳統理論,并評估NHE3在其中的作用,為診斷遠端腎小管酸中毒(dRTA)提供新見解。
研究思路
研究結合了體外和體內實驗。體外使用分離灌注的小鼠髓質TAL(mTAL),通過熒光染料(BCECF-AM和CoroNa Green)測量細胞內pH(pHi)、管腔內pH(pHlum)和細胞內Na+濃度變化。體內使用小鼠,通過膀胱導管收集尿液,使用Unisense電極實時測量尿液pH,并計算凈酸排泄(NAE)。藥理學抑制NHE3(使用#4167)和ENaC(使用苯胺米或阿米洛利)來驗證機制。數據分析包括統計比較不同處理組的效果。
測量的數據及研究意義
1. 體外mTAL的細胞內pH(pHi)變化:呋塞米引起pHi顯著堿化(從7.27±0.06升至7.60±0.04),這被管腔阿米洛利和#4167抑制。數據來自圖1、圖2和圖3。研究意義在于證明呋塞米直接激活TAL的頂端NHE3,導致H+分泌,而非僅通過遠端效應。
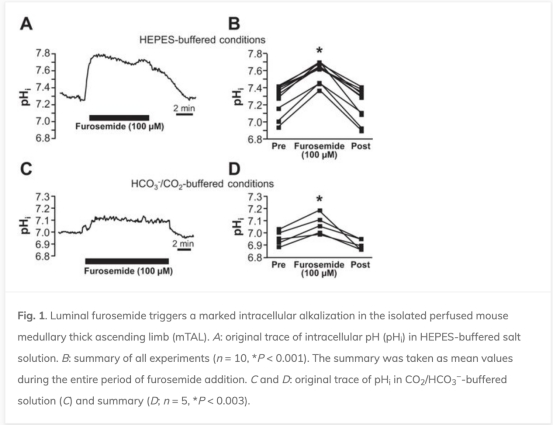
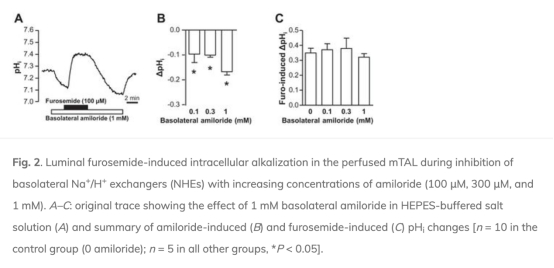
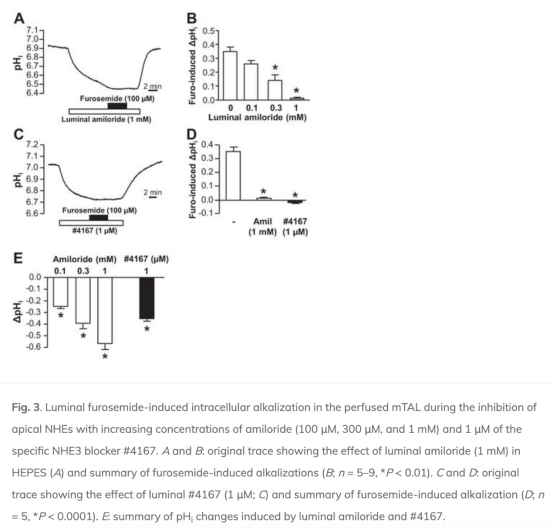
2. 體外mTAL的管腔內pH(pHlum)變化:呋塞米導致pHlum酸化(從6.92±0.04降至6.46±0.03),而阿米洛利引起堿化。數據來自圖4。研究意義在于直接證實呋塞米刺激H+分泌到管腔,鏡像pHi變化。
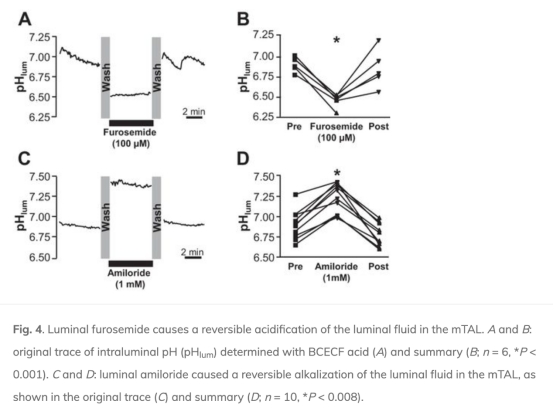
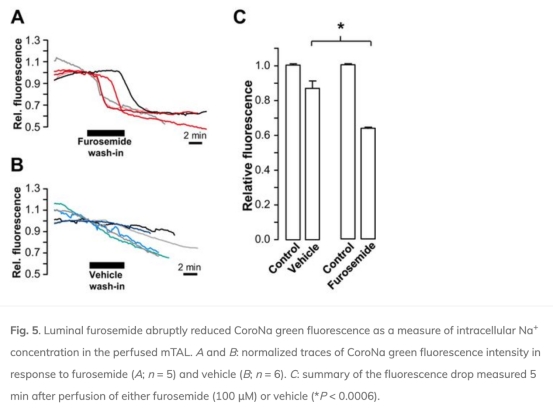
3. 體外mTAL的細胞內Na+濃度變化:呋塞米引起細胞內Na+急劇下降。數據來自圖5。研究意義在于解釋機制:呋塞米抑制Na+內流,降低細胞內Na+,增加NHE3的驅動力,促進H+分泌。
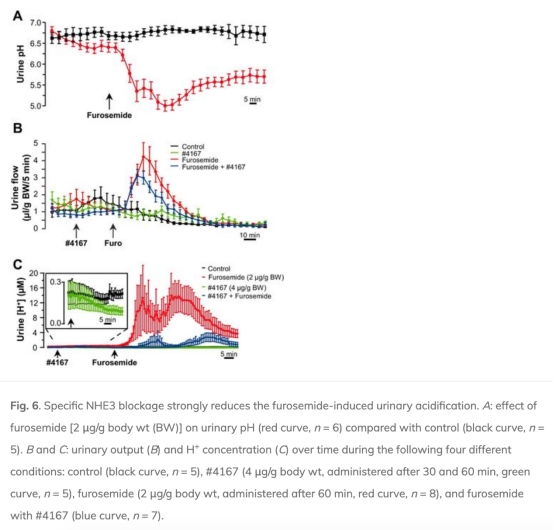
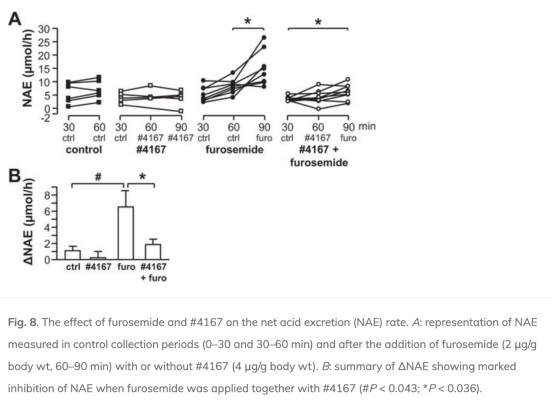
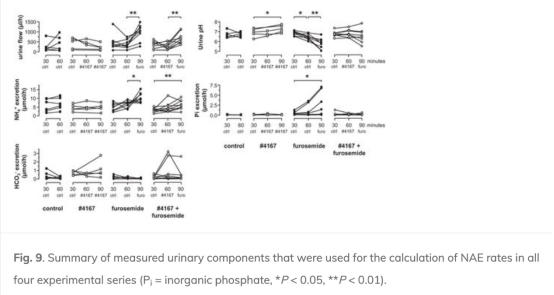
4. 體內尿液pH和凈酸排泄(NAE)變化:呋塞米誘導尿液酸化(pH下降)和NAE增加(3倍),NHE3抑制(#4167)減少NAE增加至30%。數據來自圖6、圖8和圖9。研究意義表明TAL的H+分泌貢獻顯著,且獨立于ENaC。
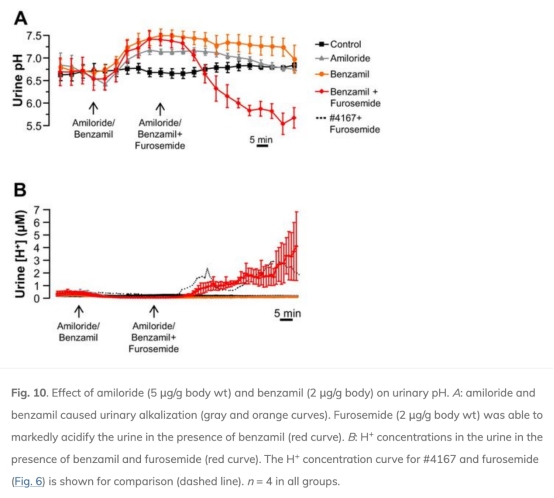
5. ENaC抑制實驗:ENaC抑制(苯胺米或阿米洛利)后,呋塞米仍能部分酸化尿液。數據來自圖10。研究意義證明呋塞米誘導的酸化部分不依賴ENaC,支持TAL的直接作用。
結論
呋塞米通過直接激活厚升支粗段(TAL)的頂端NHE3,誘導顯著的H+分泌,從而導致尿液酸化。這一機制部分獨立于ENaC介導的電壓驅動過程。研究修訂了傳統觀點,強調TAL在腎臟酸處理中的關鍵作用,并對遠端腎小管酸中毒(dRTA)的診斷測試(呋塞米測試)提供了新解釋。
使用丹麥Unisense電極測量數據的研究意義
使用丹麥Unisense電極(100μm tip微pH電極)測量尿液pH數據的研究意義在于實現了高時間分辨率(每5秒記錄)的實時尿液pH監測。這種電極允許在體內實驗中精確捕捉呋塞米和抑制劑(如#4167)的動態效應,揭示了傳統尿液收集方法可能掩蓋的細節。例如,它顯示了ENaC抑制后呋塞米仍能快速酸化尿液,以及NHE3抑制延遲和減弱了酸化反應。這增強了數據的可靠性,幫助區分TAL和遠端小管的貢獻,為機制研究提供了關鍵工具。