熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Fasting induces anti-Warburg effect that increases respiration but reduces ATP-synthesis to promote apoptosis in colon cancer models
禁食誘導抗瓦伯格效應,增加呼吸但減少ATP合成以促進結腸癌模型中的細胞凋亡
來源:Oncotarget, Volume 6, Issue 14, March 18, 2015
《Oncotarget》(《腫瘤靶點》),第6卷第14期,2015年3月18日
摘要
摘要部分闡述了短期饑餓(STS)如何通過逆轉瓦伯格效應(即癌細胞偏好有氧糖酵解的現象)來增強化療藥物奧沙利鉑(OXP)對結腸癌細胞的毒性。研究發現,STS在體外和體內模型中能降低糖酵解和谷氨酰胺分解,同時增加氧化磷酸化(OXPHOS),導致氧消耗增加但ATP合成減少,從而引發氧化應激和細胞凋亡。STS與化療聯合使用時,這種效應更加顯著,表明STS能通過代謝重編程使癌細胞對化療更敏感。
研究目的
研究目的是探究短期饑餓(STS)如何使結腸癌細胞對化療敏感化的分子機制。先前研究表明STS能保護正常細胞但增強化療對癌細胞的毒性,但具體機制尚不明確。本研究旨在驗證STS是否通過逆轉瓦伯格效應,促進氧化磷酸化并誘導代謝壓力,從而增強凋亡。
研究思路
研究思路結合了體外和體內實驗。在體內部分,使用CT26結腸癌小鼠模型,進行48小時STS循環并聯合奧沙利鉑治療,通過微PET成像監測腫瘤葡萄糖攝取和生長。在體外部分,用多種結腸癌細胞系(如CT26、HCT116、HT-29)模擬STS條件(低葡萄糖和低血清),處理48小時后加化療,評估細胞活力、代謝酶活性、氧消耗、ATP合成、ROS產生和凋亡。通過蛋白質組學、基因組學和酶學分析,探究STS對代謝通路的影響。
測量的數據及研究意義:
1. 體內腫瘤葡萄糖消耗和腫瘤生長數據:通過微PET成像測量,顯示STS和OXP聯合處理顯著降低腫瘤葡萄糖攝取和抑制生長,研究意義是證實STS能增強化療的抗腫瘤效果,數據來自圖1。
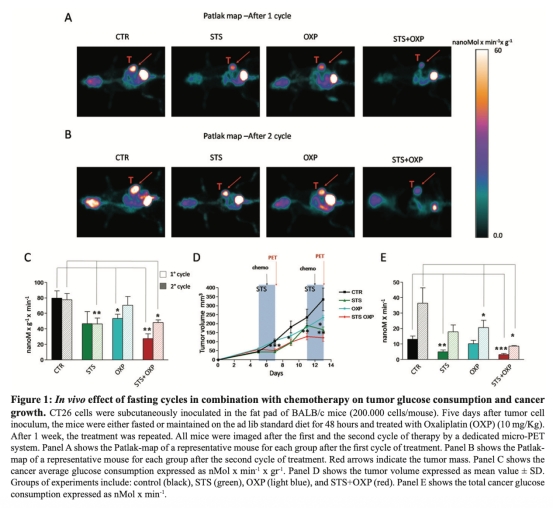
2. 體外細胞活力和葡萄糖攝取數據:通過臺盼藍染色和FDG攝取實驗測量,顯示STS和OXP聯合處理降低細胞活力和葡萄糖攝取,研究意義是驗證STS在細胞水平直接誘導代謝抑制和化療增敏,數據來自圖2。
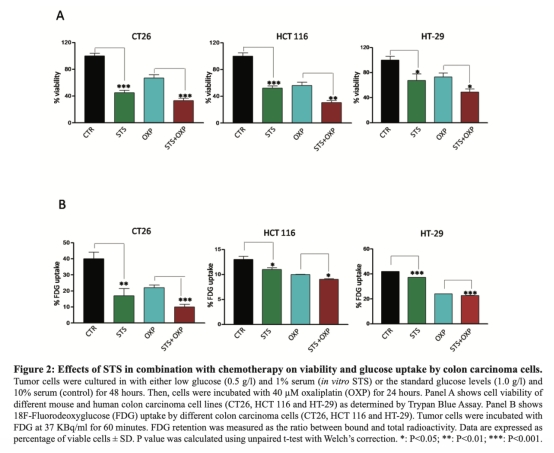
3. 代謝酶表達和活性數據:通過Western blot、酶活性測定和免疫熒光測量,顯示STS下調GLUT1、GLUT2、HKII、PFK、PK、LDH等糖酵解酶的表達和活性,研究意義是揭示STS逆轉瓦伯格效應的分子基礎,即抑制糖酵解通路,數據來自圖3。
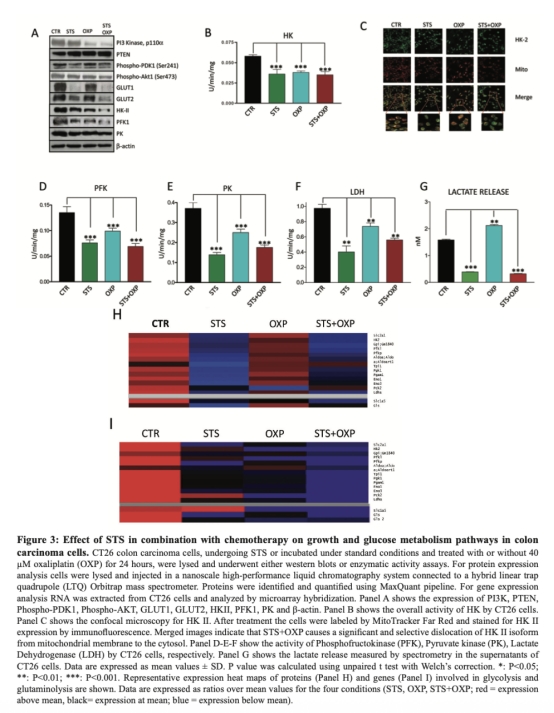
4. 線粒體氧化磷酸化數據:通過酶活性測定、氧消耗速率(OCR)和ATP合成測量,顯示STS增加復合物I和IV活性及OCR,但降低ATP合成,研究意義是證明STS引起呼吸鏈解偶聯,導致能量危機,數據來自圖4。
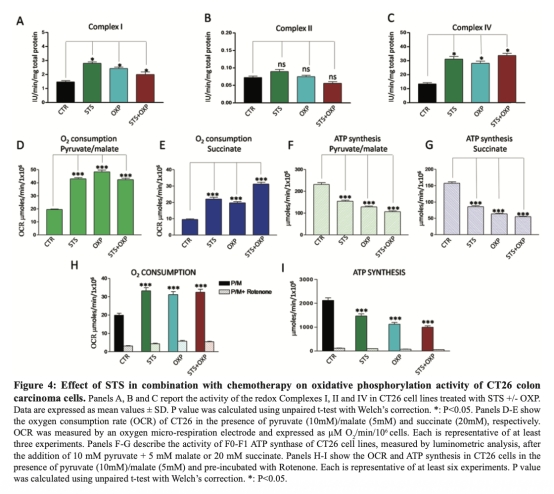
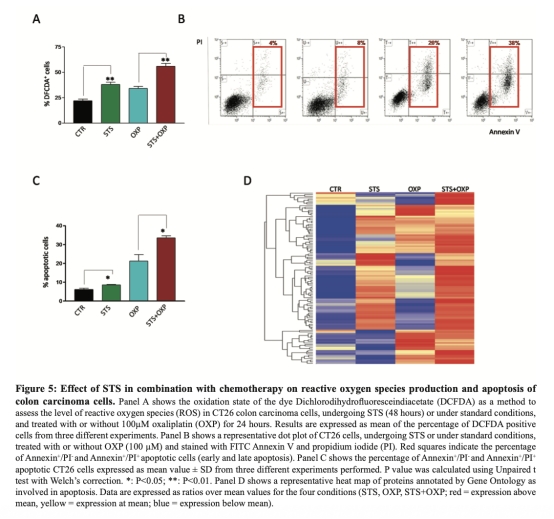
5. 活性氧(ROS)和凋亡數據:通過DCFDA染色和Annexin V/PI流式細胞術測量,顯示STS和OXP增加ROS產生和凋亡,研究意義是 linking代謝變化到細胞死亡機制,數據來自圖5。
結論
研究結論是短期饑餓(STS)通過誘導抗瓦伯格效應,使結腸癌細胞從糖酵解轉向氧化磷酸化,但導致呼吸鏈解偶聯,增加氧消耗和ROS產生,同時減少ATP合成,從而促進氧化應激和凋亡。STS與化療聯合可增強這種效應,顯著抑制腫瘤生長,為STS作為化療增敏劑提供了代謝機制基礎。
使用丹麥Unisense電極測量數據的研究意義:
使用丹麥Unisense電極測量的數據是氧消耗速率(OCR),通過微呼吸測定系統在封閉腔中進行。這些數據的研究意義在于直接量化了STS對線粒體呼吸功能的影響。測量顯示STS處理后OCR增加,但ATP合成減少,表明呼吸鏈存在解偶聯現象,即電子傳遞未有效耦合到ATP生產,導致能量浪費和電子泄漏產生活性氧。這證實了STS通過促進無效呼吸誘導代謝危機,從而增強癌細胞對化療的敏感性,為理解STS的化療增敏機制提供了關鍵實驗證據。