熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Adenosine A2a receptor stimulation prevents proteinuria in diabetic rats by promoting an anti-inflammatory phenotype without affecting oxidative stress
腺苷A2a受體刺激通過促進抗炎表型而不影響氧化應激來預防糖尿病大鼠的蛋白尿
來源:Acta Physiologica, Volume 214, 2015, Pages 311-318
《生理學報》第214卷,2015年,頁碼311-318
摘要
摘要闡述了本研究的主要發現:在胰島素缺乏的糖尿病大鼠模型中,慢性腺苷A2a受體(A2aAR)激動劑CGS21680治療能夠完全預防糖尿病引起的蛋白尿和腎小球損傷。這種保護作用是通過抗炎機制實現的,具體表現為降低了促炎因子TNF-α的排泄、增加了抗炎因子IL-10的水平、減少了巨噬細胞浸潤和腎小球損傷,但并不影響腎臟的氧化應激狀態和缺氧狀況。腎小球濾過率、腎血流量等基礎腎功能參數也未受A2aAR刺激的影響。
研究目的
本研究旨在探討慢性刺激腺苷A2a受體(A2aAR)是否能保護糖尿病大鼠的腎功能,并進一步闡明這種保護作用是否通過調節炎癥通路或腎臟氧合狀態來實現。目前尚無有效保護糖尿病患者腎功能的臨床治療方法,因此本研究旨在尋找新的治療靶點。
研究思路
研究采用鏈脲佐菌素(STZ)誘導的糖尿病大鼠模型。在誘導糖尿病的同時,通過皮下植入的微型滲透泵,對糖尿病大鼠和對照組大鼠持續輸注A2aAR特異性激動劑CGS21680或載體,持續整個4周的糖尿病病程。實驗結束時,通過急性實驗測量大鼠的腎臟血流動力學參數(如平均動脈壓、腎血流量、腎小球濾過率)和使用丹麥Unisense微電極測量腎臟皮質和髓質的氧分壓。同時,收集尿液和血漿樣本,用于分析蛋白排泄、氧化應激標志物(TBARS)和炎癥細胞因子(TNF-α, IL-10, IL-4, IL-6)水平。最后,對腎臟組織進行組織學和超微結構分析,評估腎小球損傷、巨噬細胞浸潤、基底膜厚度和腎小管間質損傷。
測量的數據及研究意義
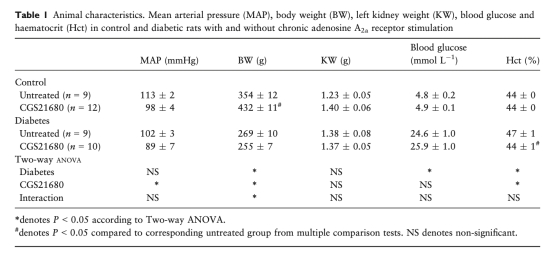
1. 動物基本特征和血糖(來自表1):數據顯示糖尿病大鼠體重增長減緩、血糖顯著升高。A2aAR刺激降低了對照組和糖尿病組的平均動脈壓,但對血糖無影響。這些數據表明實驗成功建立了糖尿病模型,且A2aAR刺激的效應并非通過改善血糖實現。
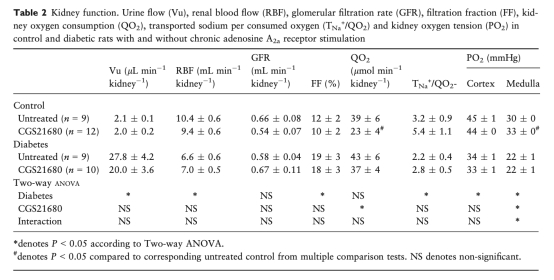
2. 腎臟功能參數(來自表2):糖尿病大鼠表現為多尿、腎血流量降低、濾過分數增加以及腎臟皮質和髓質嚴重缺氧。A2aAR刺激并未顯著改變這些參數(除在對照組中輕微增加髓質氧分壓外)。這表明A2aAR的保護作用不依賴于改善腎臟血流動力學或緩解腎臟整體缺氧。
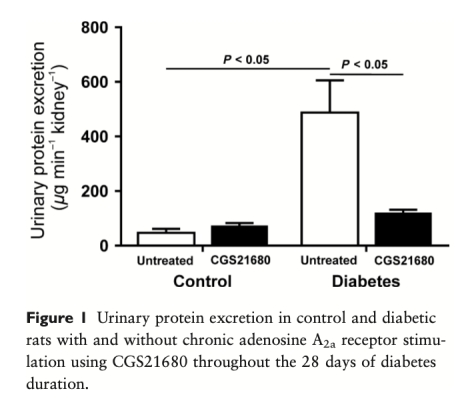
3. 蛋白尿和氧化應激標志物(來自圖1和表3):糖尿病大鼠尿蛋白排泄量顯著增加10倍,氧化應激標志物TBARS在血漿和尿液中均升高。A2aAR刺激完全預防了糖尿病引起的蛋白尿,但卻進一步加劇了糖尿病大鼠的尿液TBARS排泄。這說明A2aAR的腎臟保護作用與氧化應激水平無關,甚至可能在糖尿病背景下加劇氧化應激。
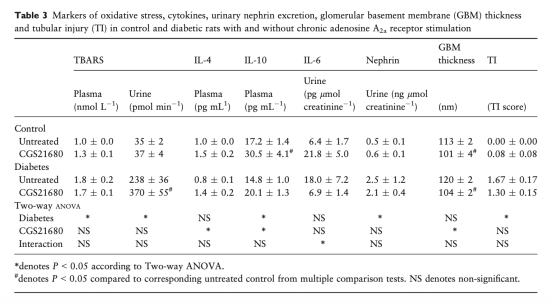
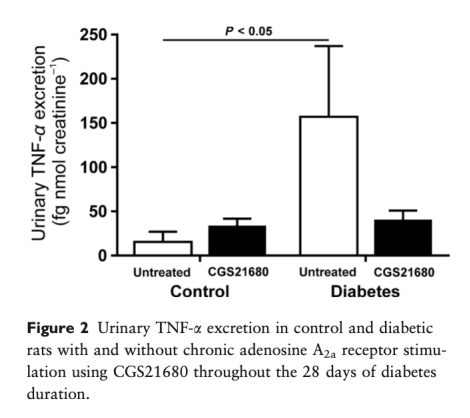
4. 炎癥標志物(來自圖2和表3):糖尿病大鼠尿液TNF-α排泄顯著增加10倍,血漿抗炎因子IL-10水平降低。A2aAR刺激完全阻止了TNF-α排泄的增加,并提高了血漿IL-10和IL-4的水平。這表明A2aAR刺激發揮了強大的抗炎作用。
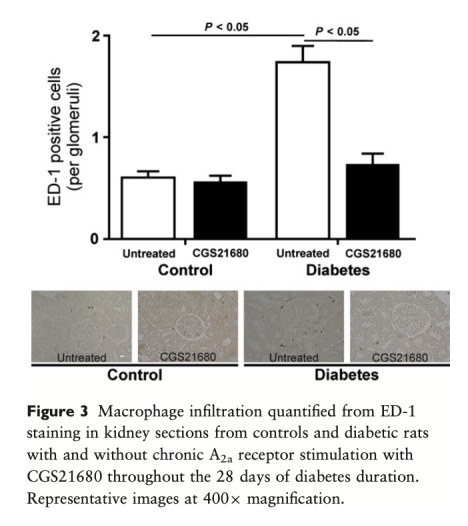
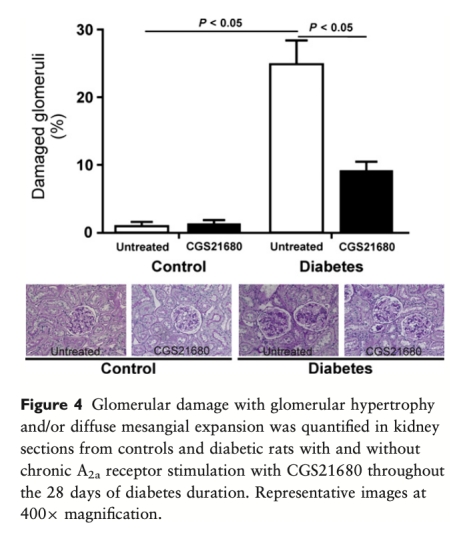
5. 組織學結果(來自圖3、圖4和表3):糖尿病大鼠腎臟中巨噬細胞浸潤增加、腎小球損傷(肥大和系膜擴張)比例升高、腎小球基底膜增厚。A2aAR刺激顯著減少了巨噬細胞浸潤、降低了腎小球損傷比例和基底膜厚度。這些形態學數據直接證實了A2aAR刺激對腎臟結構的保護作用,并與抗炎效應相吻合。
結論
本研究得出結論:慢性A2aAR刺激通過抗炎機制(減少巨噬細胞浸潤、降低TNF-α、提升IL-10)有效預防了糖尿病大鼠的蛋白尿和腎小球損傷。這一保護作用獨立于腎臟氧化應激和組織缺氧的改善,凸顯了炎癥在糖尿病腎病腎小球損傷中的關鍵作用,而缺氧則可能是獨立導致腎小管損傷的機制。A2aAR激動劑有望成為治療糖尿病腎病的新策略。
使用丹麥Unisense電極測量數據的研究意義
使用丹麥Unisense公司生產的Clark型微電極直接測量腎臟組織氧分壓(PO2)在本研究中具有重要的研究意義。首先,這種方法提供了直接、實時的局部組織氧合數據,能夠精確區分皮質和髓質這兩個氧分壓截然不同的區域。本研究結果顯示糖尿病大鼠皮質和髓質均出現顯著缺氧,這為“糖尿病腎病中存在腎組織缺氧”的假說提供了直接證據。其次,通過結合腎血流量和動靜脈氧含量差計算的整體腎臟耗氧量(QO2)未發生改變,但鈉轉運效率(TNa+/QO2)下降,這提示缺氧的原因更可能是由于氧消耗增加(源于低效的鈉重吸收)而非氧供應不足。最關鍵的是,當發現A2aAR激動劑能產生腎臟保護作用時,Unisense電極測量的數據明確顯示這種保護作用并非通過緩解腎臟缺氧來實現,因為治療組的腎組織PO2并未改善。這一發現成功地將A2aAR的保護機制與缺氧通路分離開來,將研究重點導向了炎癥機制。因此,該技術的應用使得研究者能夠得出一個強有力的結論:A2aAR激動劑的益處是抗炎作用所致,而非改善腎臟氧合。