熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Optimized Real-Time Monitoring of Glutathione Redox Status in Single Pyramidal Neurons in Organotypic Hippocampal Slices during Oxygen-Glucose Deprivation and Reperfusion
優(yōu)化實時監(jiān)測器官型海馬切片中單個錐體神經(jīng)元在氧糖剝奪和再灌注期間的谷胱甘肽氧化還原狀態(tài)
來源:ACS Chemical Neuroscience, 2015, 6, 11, 1838–1848
《ACS化學(xué)神經(jīng)科學(xué)》,2015年,第6卷第11期,第1838–1848頁
摘要
本研究通過將氧化還原敏感的Grx1-roGFP2融合蛋白轉(zhuǎn)染到器官型海馬切片培養(yǎng)物(OHSCs)CA1區(qū)的單個錐體神經(jīng)元中,優(yōu)化了實時監(jiān)測谷胱甘肽(GSH)系統(tǒng)在氧糖剝奪和再灌注(OGD/RP)期間的變化。開發(fā)了優(yōu)化的灌注系統(tǒng),確保組織內(nèi)pO2快速可控變化,模擬急性中風(fēng)條件。使用共轉(zhuǎn)染的tdTomato作為內(nèi)標,提高Grx1-roGFP2氧化還原狀態(tài)定量測量的準確性。結(jié)果表明,在OGD期間,線粒體中GSH還原電位(EGSH)變得更還原,而在RP期間變得更氧化,而細胞質(zhì)中的變化不顯著。
研究目的
本研究旨在開發(fā)一種優(yōu)化方法,用于實時監(jiān)測OHSCs中單個錐體神經(jīng)元在OGD/RP期間的GSH氧化還原狀態(tài),以模擬中風(fēng)等缺血性損傷的體外模型。通過改進灌注系統(tǒng)和傳感器校準,提高測量的時空分辨率,區(qū)分線粒體和細胞質(zhì)中的氧化還原動態(tài)。
研究思路
研究采用器官型海馬切片培養(yǎng)物(OHSCs)作為模型,通過基因槍或單細胞電穿孔將Grx1-roGFP2傳感器轉(zhuǎn)染到CA1區(qū)錐體神經(jīng)元的細胞質(zhì)或線粒體中。優(yōu)化灌注系統(tǒng)(如[O+V]系統(tǒng)),使用在線氧合器和真空抽吸,實現(xiàn)快速溶液交換和控制pO2。使用丹麥Unisense氧微電極測量組織深度相關(guān)的pO2變化。在OGD/RP協(xié)議(10分鐘對照、20分鐘OGD、30分鐘RP)中,通過比率熒光成像監(jiān)測Grx1-roGFP2信號,并利用tdTomato作為內(nèi)標校準傳感器氧化度(OxDroGFP2)和EGSH。通過比較不同灌注系統(tǒng)和組織深度,驗證模型的體內(nèi)相關(guān)性。
測量的數(shù)據(jù)及研究意義
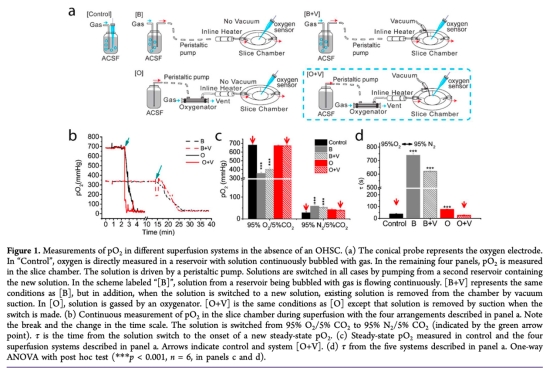
1. pO2在灌注系統(tǒng)中的變化:數(shù)據(jù)來自Figure 1。測量顯示,優(yōu)化系統(tǒng)[O+V]能快速(τ<30秒)實現(xiàn)pO2穩(wěn)態(tài)變化,而傳統(tǒng)系統(tǒng)響應(yīng)慢。研究意義:確保OGD/RP期間pO2變化時間尺度與體內(nèi)中風(fēng)模型一致,提高實驗的生理相關(guān)性,為實時監(jiān)測氧化還原動態(tài)提供可靠環(huán)境。
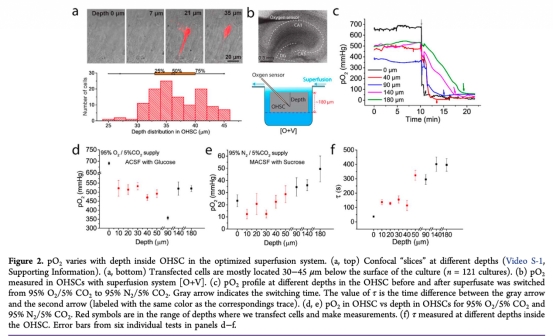
2. pO2隨組織深度的分布:數(shù)據(jù)來自Figure 2。在OHSCs中,pO2從表面(約691 mmHg)到中間(最低358 mmHg)變化,轉(zhuǎn)染細胞位于30-45μm深度,該范圍內(nèi)pO2變化一致且快速(τ約2分鐘)。研究意義:證實轉(zhuǎn)染區(qū)域pO2可控,確保氧化還原測量在均勻缺氧條件下進行,減少深度異質(zhì)性帶來的偏差。
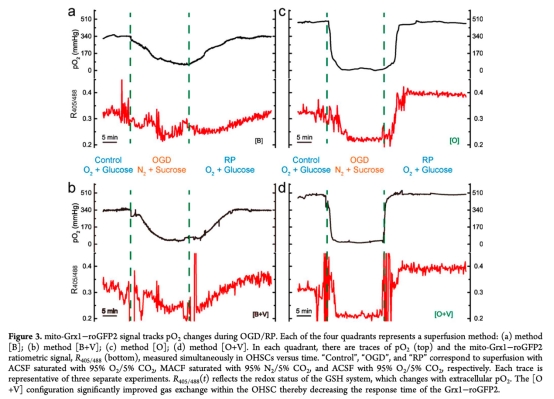
3. Grx1-roGFP2信號與pO2的同步變化:數(shù)據(jù)來自Figure 3。在OGD/RP期間,Grx1-roGFP2比率信號(R405/488)與pO2變化時間尺度一致,優(yōu)化系統(tǒng)[O+V]響應(yīng)最快。研究意義:驗證傳感器能實時反映氧化還原動態(tài),且系統(tǒng)優(yōu)化確保信號變化與生理過程同步,為研究GSH系統(tǒng)在缺血中的角色提供直接證據(jù)。
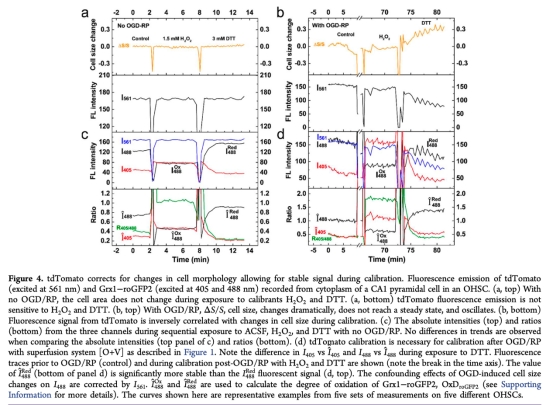
4. tdTomato內(nèi)標校準細胞形態(tài)變化:數(shù)據(jù)來自Figure 4。OGD/RP后校準期間,細胞大小變化顯著,tdTomato信號作為內(nèi)標校正Grx1-roGFP2絕對強度,使OxDroGFP2計算穩(wěn)定。研究意義:解決應(yīng)激條件下細胞體積變化對熒光信號的干擾,提高氧化還原參數(shù)定量的準確性,確保EGSH推導(dǎo)可靠。
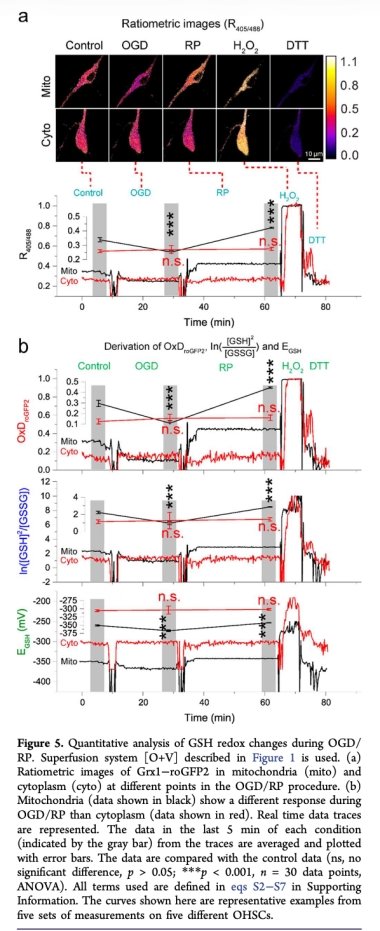
5. 線粒體和細胞質(zhì)GSH氧化還原變化:數(shù)據(jù)來自Figure 5。在線粒體中,OGD期間OxDroGFP2從0.30降至0.10(更還原),RP期間升至0.45(更氧化);細胞質(zhì)中無顯著變化。EGSH在線粒體OGD期間更負(-351 mV),RP期間更正。研究意義:揭示線粒體GSH系統(tǒng)在缺血應(yīng)激中動態(tài)變化更敏感,提示還原等效物供應(yīng)(如NADPH)可能主導(dǎo)氧化還原狀態(tài),而非ROS,為中風(fēng)機制提供新見解。
結(jié)論
優(yōu)化方法成功實現(xiàn)了OHSCs中單個錐體神經(jīng)元GSH氧化還原狀態(tài)的實時監(jiān)測。線粒體GSH系統(tǒng)在OGD期間迅速還原,RP期間氧化,而細胞質(zhì)系統(tǒng)保持穩(wěn)定,表明線粒體是缺血應(yīng)激的關(guān)鍵響應(yīng)區(qū)。該模型為研究中風(fēng)等疾病的氧化還原機制提供了高時空分辨率工具,并提示還原動力可能主導(dǎo)GSH狀態(tài)變化。
使用丹麥Unisense電極測量數(shù)據(jù)的研究意義
使用丹麥Unisense氧微電極測量組織pO2具有關(guān)鍵研究意義。該電極具有高靈敏度(檢測限低至2 nM)和快速響應(yīng)時間(<2秒),能精確監(jiān)測OHSCs不同深度的氧氣梯度變化。通過測量pO2隨深度分布(Figure 2),驗證了轉(zhuǎn)染細胞區(qū)域(30-45μm)的pO2可控且變化時間尺度(τ約2分鐘)與體內(nèi)中風(fēng)模型一致,確保OGD/RP實驗的生理相關(guān)性。電極數(shù)據(jù)還用于優(yōu)化灌注系統(tǒng)(如Figure 1顯示[O+V]系統(tǒng)響應(yīng)最快),減少擴散延遲,使氧化還原傳感器信號能真實反映急性缺氧事件。此外,pO2與Grx1-roGFP2信號同步變化(Figure 3),證實了氧化還原動態(tài)與氧合狀態(tài)的直接關(guān)聯(lián),為理解GSH系統(tǒng)在缺血中的調(diào)控提供了可靠環(huán)境參數(shù)。總之,Unisense電極的應(yīng)用增強了模型的整體可靠性,使體外研究更能模擬體內(nèi)條件。