熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Early adenosine release contributes to hypoxia-induced disruption of stimulus-induced sharp wave-ripple complexes in rat hippocampal area CA3
早期腺苷釋放促進缺氧誘導的大鼠海馬CA3區刺激誘發尖波漣漪復合體的破壞
來源: European Journal of Neuroscience,Volume42, Issue2, July 2015, Pages 1808-1817
《歐洲神經科學雜志》,第42卷第2期,2015年7月,第1808-1817頁
摘要
本研究探討了缺氧對大鼠海馬切片中尖波漣漪復合體(SPW-Rs)和反復發作樣放電(REDs)的影響及其阻斷機制。通過使用Clark型氧傳感器微電極測量氧含量,發現SPW-Rs活動期間的耗氧量可忽略不計,而REDs則消耗更多氧氣。當氧含量降至20%或更低并持續3分鐘時,這些網絡活動可被逆性阻斷。腺苷A1受體拮抗劑DPCPX可增加SPW-Rs的發生率和振幅,而激動劑則快速抑制SPW-Rs。缺氧可降低CA3錐體細胞微小興奮性突觸后電流的頻率,該效應可被DPCPX逆轉。結果表明缺氧早期腺苷釋放通過減少突觸前谷氨酸釋放,促使CA3區SPW-Rs的短暫阻斷。
研究目的
本研究旨在闡明缺氧對海馬SPW-Rs和REDs的抑制機制,重點探究腺苷在缺氧早期對突觸前谷氨酸釋放的調節作用,以及不同網絡活動對缺氧的敏感性差異。
研究思路
研究采用成年大鼠海馬切片,通過高頻刺激誘導SPW-Rs,并使用GABAA受體拮抗劑比枯枯堿將其轉化為REDs。利用丹麥Unisense氧微電極測量組織氧分壓(pO2),并結合細胞外場電位記錄、全細胞膜片鉗技術記錄mEPSCs和mIPSCs。通過施加不同缺氧程度(60%至0% O2)及腺苷A1受體調節劑(DPCPX激動劑/拮抗劑),分析缺氧對網絡活動和突觸傳遞的影響,并通過pO2深度剖面評估耗氧量。
測量的數據及研究意義
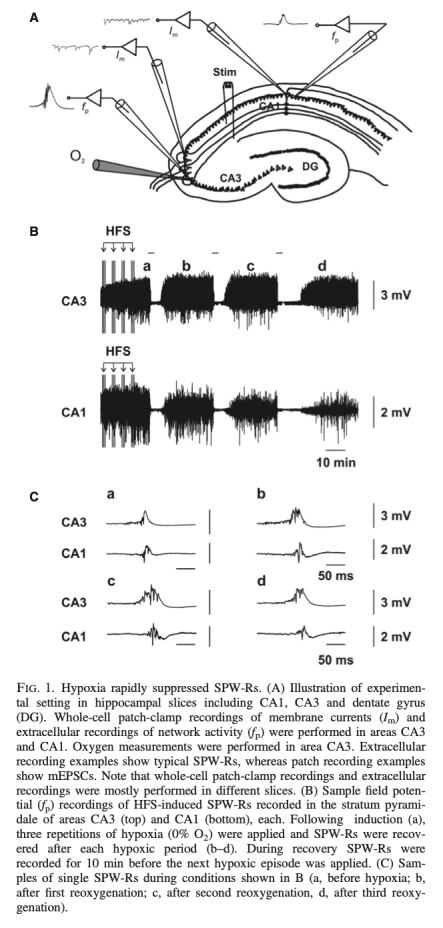
1 SPW-Rs和REDs的缺氧敏感性數據:來自圖1、圖2。數據顯示SPW-Rs在20% O2時被可逆抑制,而REDs在0% O2下仍能恢復。SPW-Rs在6分鐘嚴重缺氧后出現不可逆阻斷。研究意義:揭示SPW-Rs對缺氧更敏感,REDs耐受性更強,表明抑制性神經傳遞的缺失增強了網絡對缺氧的抵抗力。
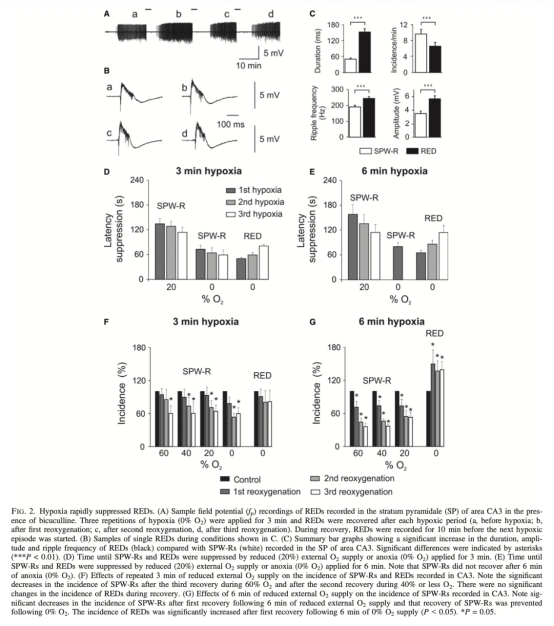
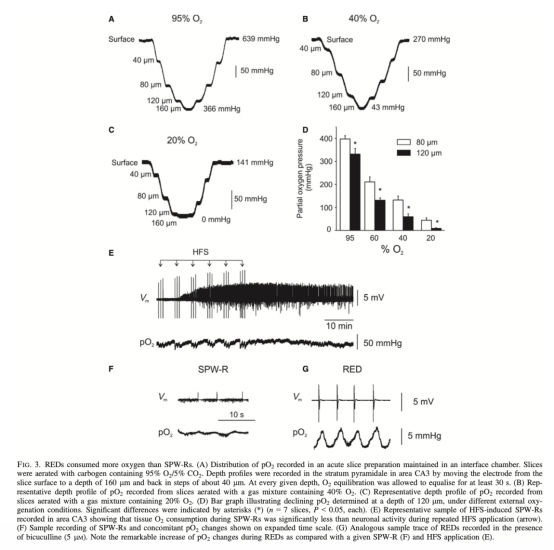
2 氧分壓深度剖面和耗氧量數據:來自圖3。pO2深度剖面顯示在160μm深度處氧分壓降至43 mmHg(40% O2條件)。單個SPW-R僅引起0.46 mmHg pO2下降,而REDs導致9.3 mmHg下降。研究意義:定量表明REDs耗氧量是SPW-Rs的20倍,證實癲癇樣活動的高代謝需求,并驗證了界面培養系統中氧梯度分布的可靠性。
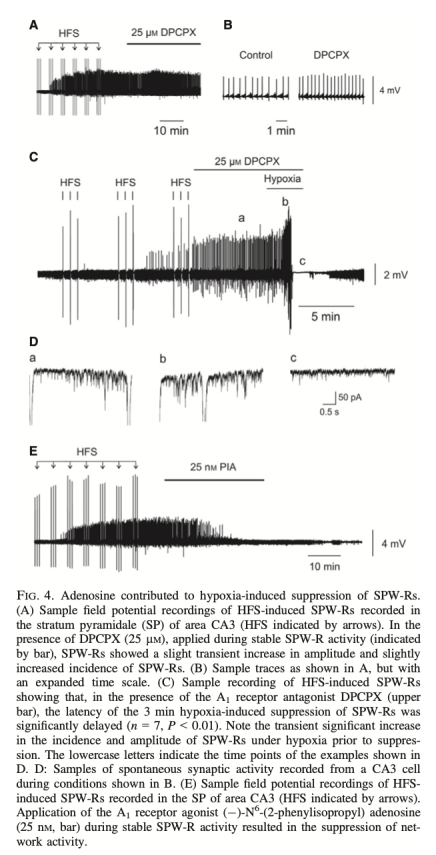
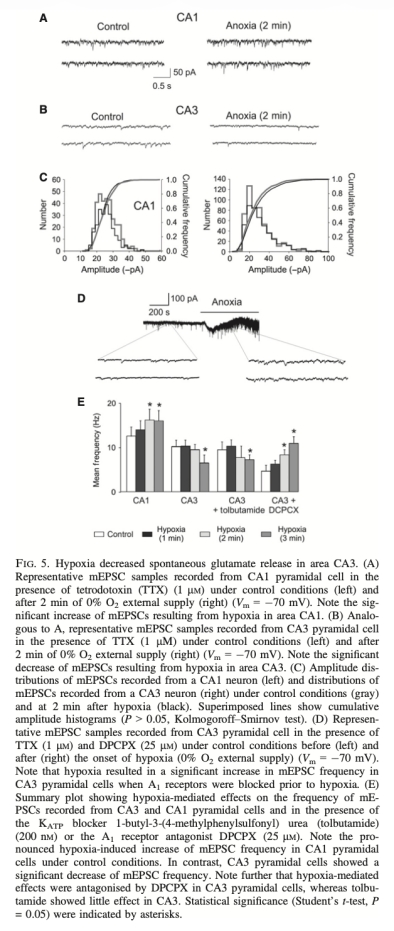
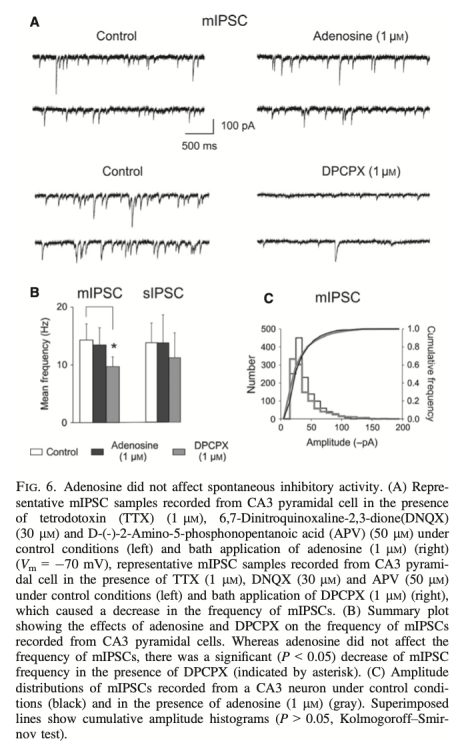
3 腺苷對突觸傳遞的調節數據:來自圖4、圖5、圖6。DPCPX(A1受體拮抗劑)延遲了缺氧對SPW-Rs的抑制,并逆轉了缺氧引起的CA3區mEPSC頻率降低。缺氧在CA1區增加mEPSC頻率,而在CA3區降低之。研究意義:表明腺苷通過A1受體介導的突觸前機制抑制谷氨酸釋放,且CA1與CA3區對缺氧的反應相反,提示區域特異性調節機制。
結論
1 缺氧通過早期腺苷釋放激活A1受體,抑制CA3區突觸前谷氨酸釋放,從而導致SPW-Rs的快速阻斷。
2 SPW-Rs的耗氧量遠低于REDs,表明生理性網絡活動能耗較低,而癲癇樣活動代謝需求顯著增加。
3 CA3與CA1區對缺氧的反應不同:缺氧降低CA3區谷氨酸釋放,卻增加CA1區釋放,這種差異可能與腺苷信號通路的區域特異性有關。
使用丹麥Unisense電極測量數據的研究意義
使用丹麥Unisense氧微電極(Clark型,尖端直徑10μm)測量海馬切片CA3區氧分壓具有關鍵研究意義。該電極提供高空間分辨率(40μm步進深度剖面)和實時pO2動態數據,精度達毫米汞柱級別。研究通過深度剖面(圖3A-C)量化了切片內的氧梯度,證實即使在高氧灌注(95% O2)條件下,組織深部(160μm)氧分壓可降至43 mmHg,模擬了體內生理范圍(30-80 mmHg)。電極數據直接揭示了SPW-Rs與REDs的耗氧差異:SPW-Rs僅引起微小pO2波動(0.46 mmHg),而REDs耗氧量顯著更高(9.3 mmHg),表明癲癇樣活動代謝需求激增。這些測量排除了缺氧本身對實驗結果的干擾,因為即使在嚴重缺氧(20% O2)時,電極記錄顯示組織pO2仍高于臨界缺氧閾值(7.5 mmHg)。此外,電極數據與場電位記錄的同步性(圖3E-G)證實了耗氧與電活動的直接關聯,為腺苷的代謝調節作用提供了可靠的環境參數。該技術的高靈敏度使研究人員能夠區分不同網絡活動的能量成本,為理解缺氧條件下神經回路功能的代謝基礎提供了直接證據。