熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
Cobaloxime-Based Artificial Hydrogenases
人工氫化酶在中性水溶液中的應(yīng)用
來源:Inorg. Chem. 2014, 53, 8071?8082
1. 論文摘要內(nèi)容
摘要指出,鈷肟是流行的產(chǎn)氫分子催化劑,但此前主要研究其在非水條件下的性能。本研究證明,它們也可用于設(shè)計在中性水溶液中應(yīng)用的人工氫化酶。研究者報告了通過將兩種鈷肟基團({Co(dmgH)?} 和 {Co(dmgBF?)?})結(jié)合到脫輔基鯨肌紅蛋白上,制備了兩種明確的生物雜化材料。所有光譜數(shù)據(jù)均證實鈷肟基團被插入到肌紅蛋白的結(jié)合口袋內(nèi),并通過軸向位置與組氨酸殘基配位,形成了熱力學(xué)穩(wěn)定的配合物。量子化學(xué)/分子力學(xué)對接計算表明,與口袋內(nèi)的另一個組氨酸殘基相比,其更傾向于與His93配位。有趣的是,鈷中心的氧化還原活性在這兩種生物雜化體中都得以保留,這使得它們在中性水溶液條件下具有催化產(chǎn)氫的活性。
2. 研究目的
本研究的主要目的是將鈷肟分子催化劑整合到蛋白質(zhì)(脫輔基鯨肌紅蛋白)支架中,構(gòu)建穩(wěn)定且功能明確的人工氫化酶,以解決鈷基分子催化劑在中性水溶液中穩(wěn)定性差、活性低的問題。研究旨在驗證這種生物雜化策略能否保護(hù)催化劑,并使其在生理pH的水環(huán)境中保持催化質(zhì)子還原產(chǎn)氫的能力。
3. 研究思路
設(shè)計并合成生物雜化體:選擇兩種鈷肟配合物 [Co(dmgBF?)?(H?O)?] 和 [Co(dmgH)?(H?O)?] 作為活性中心,以鯨肌紅蛋白 作為宿主蛋白。將脫輔基肌紅蛋白與鈷肟配合物反應(yīng),通過尺寸排阻色譜純化,得到兩種生物雜化體 SwMb·1 和 SwMb·2。
全面的結(jié)構(gòu)與性質(zhì)表征:利用多種光譜和波譜技術(shù)(紫外-可見吸收光譜、圓二色光譜、電子順磁共振、X射線吸收近邊結(jié)構(gòu)/擴展X射線吸收精細(xì)結(jié)構(gòu))詳細(xì)表征生物雜化體的形成,確認(rèn)鈷肟是否插入蛋白質(zhì)口袋并與組氨酸配位,并分析鈷的氧化態(tài)和局部幾何結(jié)構(gòu)。
理論計算模擬:進(jìn)行量子化學(xué)/分子力學(xué)對接計算,模擬鈷肟在蛋白質(zhì)口袋內(nèi)的結(jié)合模式,預(yù)測其最穩(wěn)定的配位構(gòu)型(如與His93還是His64結(jié)合),并與實驗結(jié)構(gòu)數(shù)據(jù)對比。
電化學(xué)性質(zhì)研究:將生物雜化體吸附到多壁碳納米管修飾電極上,通過循環(huán)伏安法測量其氧化還原電位,評估蛋白質(zhì)環(huán)境對鈷中心(Co(II)/Co(I) 電對)電勢的影響。
催化性能評估:在pH 7.0的中性水溶液中,測試生物雜化體的產(chǎn)氫催化活性。使用兩種體系:(i) 化學(xué)還原體系:以[Eu(EGTA)(H?O)]2? 為還原劑;(ii) 光催化體系:以[Ru(bpy)?]2? 或脫氮黃素 為光敏劑。使用Unisense氫氣微傳感器實時、定量監(jiān)測產(chǎn)生的氫氣。
4. 測量方面、數(shù)據(jù)來源及研究意義
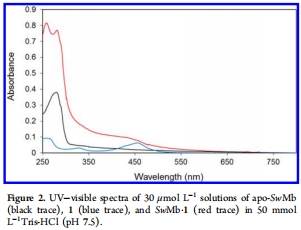
紫外-可見吸收光譜:記錄了生物雜化體及其組分的光譜。意義:SwMb·1的光譜顯示了鈷(II)中心的d-d躍遷特征峰,但與自由配合物相比發(fā)生藍(lán)移和展寬,表明蛋白質(zhì)環(huán)境和組氨酸配位改變了鈷的電子結(jié)構(gòu)。SwMb·2的光譜則類似鈷(III)物種。數(shù)據(jù)來自圖2、圖S1。
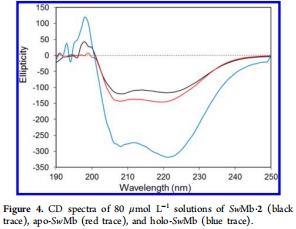
圓二色光譜:在遠(yuǎn)紫外區(qū)測定了蛋白質(zhì)的CD譜。意義:SwMb·1和SwMb·2的CD譜在190-200 nm區(qū)域出現(xiàn)了與holo-SwMb類似的信號,該信號與His93配位引起的局部蛋白質(zhì)折疊有關(guān),從而支持鈷肟與His93配位的結(jié)論。數(shù)據(jù)來自圖4。
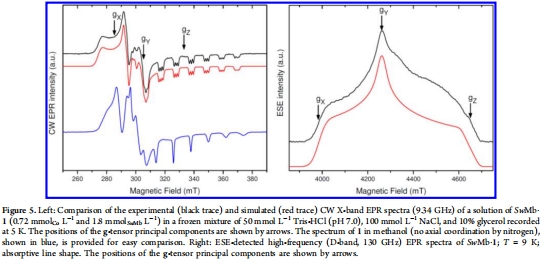
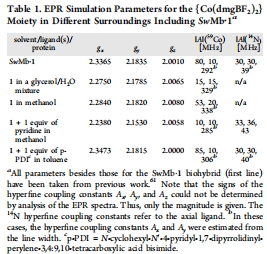
電子順磁共振譜:測量了SwMb·1的X波段和D波段EPR譜。意義:譜圖顯示出低自旋鈷(II)的特征及與1?N的超精細(xì)耦合,直接證明了軸向有一個氮原子(來自組氨酸)與鈷配位。g值和超精細(xì)耦合常數(shù)的分析表明鈷肟處于疏水環(huán)境中。數(shù)據(jù)來自圖5、表1。
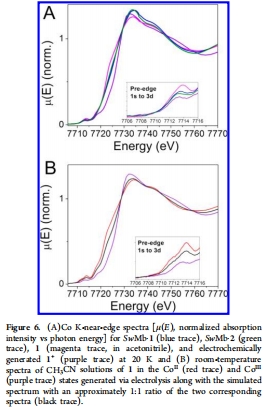
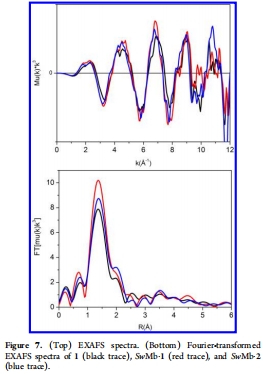
X射線吸收譜:測量了Co K-edge的XANES和EXAFS譜。意義:XANES邊前能量和形狀表明生物雜化體中存在Co(II)和Co(III)的混合。EXAFS譜顯示生物雜化體中鈷的第一配位殼層信號強度增加,表明配位數(shù)增加或鍵長更均一,這與理論計算中鈷與His93及水分子形成六配位結(jié)構(gòu)相符。數(shù)據(jù)來自圖6、圖7。
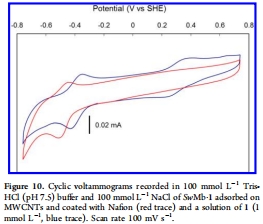
電化學(xué)數(shù)據(jù):通過循環(huán)伏安法測量了修飾電極上生物雜化體的氧化還原電位。意義:SwMb·1的Co(II)/Co(I)電對相對于自由配合物1負(fù)移了100 mV,表明蛋白質(zhì)環(huán)境顯著調(diào)控了鈷中心的還原電勢。SwMb·2的循環(huán)伏安圖在-0.6 V (vs. SHE) 左右出現(xiàn)催化電流,提示其具有產(chǎn)氫催化活性。數(shù)據(jù)來自圖10、圖S6、S7。
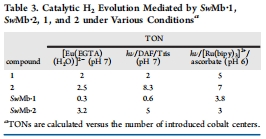
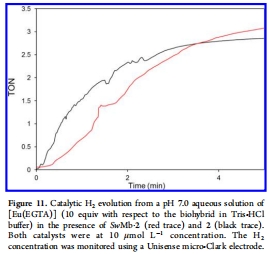
催化產(chǎn)氫活性:使用Unisense氫氣微傳感器定量測定了在不同催化體系下的氫氣產(chǎn)量,并計算轉(zhuǎn)換數(shù)。意義:直接證明兩種生物雜化體在中性水條件下具有催化產(chǎn)氫活性。SwMb·2在化學(xué)還原和光催化條件下均表現(xiàn)出活性,而SwMb·1在更酸性的條件(pH 6)下活性更高。數(shù)據(jù)匯總于表3,動力學(xué)示例見圖11。
5. 研究結(jié)論
成功構(gòu)建穩(wěn)定的人工氫化酶:成功將兩種鈷肟配合物通過軸向配位插入鯨肌紅蛋白的亞鐵血紅素結(jié)合口袋,主要與His93配位,形成了熱力學(xué)穩(wěn)定、結(jié)構(gòu)明確的生物雜化體SwMb·1和SwMb·2。
蛋白質(zhì)環(huán)境調(diào)控催化劑性質(zhì):光譜和電化學(xué)數(shù)據(jù)證實,蛋白質(zhì)的疏水口袋和特異的組氨酸配位顯著改變了鈷肟的電子結(jié)構(gòu)、氧化還原電勢及其穩(wěn)定性,使其更適應(yīng)水環(huán)境。
保留催化活性:兩種生物雜化體均能在中性或近中性水溶液中催化質(zhì)子還原產(chǎn)生氫氣,盡管轉(zhuǎn)換數(shù)(3-5)相較于部分自由配合物有所降低。這證明了“人工酶”策略用于穩(wěn)定水相分子催化劑的可行性。
結(jié)構(gòu)與活性關(guān)系:SwMb·2(質(zhì)子橋聯(lián)型鈷肟)在中性pH下活性優(yōu)于SwMb·1(二氟硼橋聯(lián)型)。SwMb·1需要更酸的pH以提升活性,這與自由配合物的性質(zhì)趨勢一致,表明蛋白質(zhì)環(huán)境并未改變其本質(zhì)的pH依賴性。
催化機制限制:由于催化劑被隔離在蛋白質(zhì)口袋內(nèi),雙分子反應(yīng)路徑被阻斷,催化可能嚴(yán)格遵循單分子機理(如Co(I)-H中間體質(zhì)子化),這可能是其轉(zhuǎn)換數(shù)受限的原因之一。
6. 詳細(xì)解讀使用丹麥Unisense電極測量出來的數(shù)據(jù)有什么研究意義
在本研究中,使用丹麥Unisense公司的微克拉克氫電極 所進(jìn)行的測量,是定量評估人工氫化酶催化性能的核心和關(guān)鍵,其研究意義至關(guān)重要:
實現(xiàn)高靈敏度、實時、定量的氫氣檢測:催化產(chǎn)氫的轉(zhuǎn)換數(shù)是衡量人工氫化酶性能的黃金標(biāo)準(zhǔn)。Unisense氫氣微傳感器具有極高的靈敏度和選擇性,能夠?qū)崟r監(jiān)測密閉微型呼吸室內(nèi)溶解氫氣的濃度變化。這使得研究者可以精確繪制產(chǎn)氫動力學(xué)曲線,如圖11所示,從而準(zhǔn)確計算出催化反應(yīng)的初始速率和總轉(zhuǎn)換數(shù)。這對于比較不同生物雜化體之間、以及與自由配合物之間的活性差異至關(guān)重要。
適用于微量反應(yīng)體系:本研究使用Unisense的400 μL微型呼吸室進(jìn)行催化測試。該傳感器非常適合這種微量液上氣相分析,能夠在不干擾反應(yīng)體系的情況下,對微量氣體產(chǎn)物進(jìn)行原位、連續(xù)監(jiān)測。這避免了傳統(tǒng)氣相色譜等方法需要取樣、可能導(dǎo)致空氣混入或壓力變化的缺點,特別適合對氧氣敏感的反應(yīng)體系。
為催化效率與機理提供直接證據(jù):通過實時產(chǎn)氫數(shù)據(jù),研究者可以清晰地觀察到反應(yīng)的誘導(dǎo)期、線性產(chǎn)氫階段以及催化劑可能失活的平臺期。例如,圖11 顯示SwMb·2的產(chǎn)氫在約5分鐘內(nèi)完成,對應(yīng)還原劑消耗完畢。這些動態(tài)信息有助于分析催化反應(yīng)的效率。此外,通過多輪添加還原劑的實驗,可以測試催化劑的穩(wěn)定性,這些結(jié)論都依賴于Unisense電極提供的連續(xù)、可靠的氫氣濃度-時間曲線。
支撐不同催化體系的性能比較:研究測試了化學(xué)還原和兩種不同的光催化體系。Unisense電極提供的標(biāo)準(zhǔn)化、可重復(fù)的定量產(chǎn)氫數(shù)據(jù),使得研究者能夠?qū)⒉煌?qū)動條件下的催化轉(zhuǎn)換數(shù)(表3)進(jìn)行公平比較。例如,數(shù)據(jù)表明在相同pH下,SwMb·2的活性普遍高于SwMb·1;而在pH 6的光催化體系中,兩者活性都有所提升。這些比較是得出“蛋白質(zhì)環(huán)境調(diào)控活性”和“催化活性具有pH依賴性”等結(jié)論的基礎(chǔ)。
驗證催化與電化學(xué)數(shù)據(jù)的關(guān)聯(lián):循環(huán)伏安法表明SwMb·2具有較低的產(chǎn)氫過電位(~200 mV)。Unisense電極在溶液測試中證實了該生物雜化體在溫和還原劑(驅(qū)動力量約220-280 mV)存在下確實能催化產(chǎn)氫。這種電化學(xué)預(yù)測與溶液催化實驗的相互印證,極大地增強了整個研究的說服力和完整性。
總結(jié):Unisense氫氣微傳感器在本研究中扮演了“催化性能的精準(zhǔn)秤”角色。它將“人工氫化酶能否工作”這一定性問題,轉(zhuǎn)化為“能工作多好、多快、持續(xù)多久”的定量科學(xué)描述。其提供的高時間分辨率、定量的產(chǎn)氫動力學(xué)數(shù)據(jù),是所有催化活性比較、機理推斷和最終性能評估的基石。沒有這種精確的氫氣檢測手段,關(guān)于鈷肟-肌紅蛋白雜化體作為有效人工氫化酶的結(jié)論將缺乏最直接的證據(jù)。