熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
在腦機接口領域,傳統(tǒng)技術長期面臨三大瓶頸:侵入性創(chuàng)傷、信號衰減和功能單一性。美國精準神經科學公司最新研發(fā)的皮層薄膜微電極陣列系統(tǒng),通過400-900μm微切口實現(xiàn)無開顱植入,標志著神經接口技術進入微創(chuàng)時代。這項發(fā)表于《自然生物醫(yī)學工程》的研究,不僅將電極密度提升至1024通道,更實現(xiàn)了神經記錄與刺激的雙向交互,為癱瘓康復、癲癇診療等領域帶來突破性進展。
傳統(tǒng)開顱植入技術存在顯著缺陷。常規(guī)手術需切除10-15cm骨瓣,電極長期植入后易出現(xiàn)信號漂移,運動解碼準確率隨時間呈指數(shù)衰減。更致命的是其功能局限性——多數(shù)設備僅能執(zhí)行單一任務。這種技術困局在新型薄膜電極系統(tǒng)中被徹底打破:通過380μm厚的柔性基底承載50μm微電極,配合特制導針實現(xiàn)亞毫米級精準部署,動物實驗顯示皮層軟膜完整率維持在98%以上。
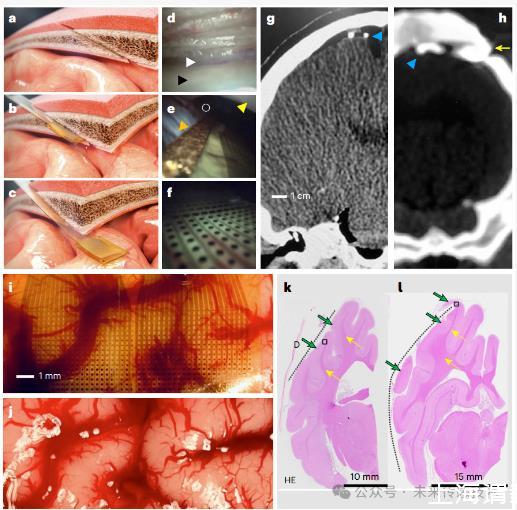
微創(chuàng)植入技術的實現(xiàn)依賴精密的機械設計。研究團隊開發(fā)了獨特的顱微切口插入系統(tǒng),通過聚酰亞胺口袋固定導針,使電極陣列在硬膜下空間展開時保持與皮層表面平行。CT影像顯示,植入后陣列邊緣與顱骨切口的間距可精確控制在50μm內。這種設計在豬模型實驗中展現(xiàn)出優(yōu)異的可逆性:移除陣列后皮層表面完整性達到100%,組織學分析證實與傳統(tǒng)硬膜下電極無系統(tǒng)性差異。
高密度記錄能力是該系統(tǒng)的另一突破。1024通道陣列在20kHz采樣率下,可捕捉到皮層表面300μm分辨率的電活動。實驗數(shù)據(jù)顯示,觸覺刺激位置解碼準確率超過90%,顯著優(yōu)于傳統(tǒng)4通道電極。更值得注意的是其動態(tài)適應性:通過CRNN神經網(wǎng)絡架構,系統(tǒng)能實時提取低頻和高伽瑪頻段特征,在不同麻醉深度下保持穩(wěn)定解碼性能。這為臨床應用提供了關鍵保障,特別是在癲癇灶定位等需要區(qū)分清醒與麻醉狀態(tài)的場景中。
雙向交互功能拓展了神經調控邊界。同一電極既可記錄皮層活動,又能實施亞毫米級刺激,這種設計在視覺重建實驗中展現(xiàn)獨特優(yōu)勢。通過左半球感覺運動皮層的電極陣列,研究團隊成功誘導出灰度感知,證明了皮層表面電刺激的空間特異性。在運動控制方面,自由行走的迷你豬實驗顯示,脛神經電刺激可誘發(fā)特征性相位反轉,這種精確的時空分辨率使步態(tài)解碼成為可能。
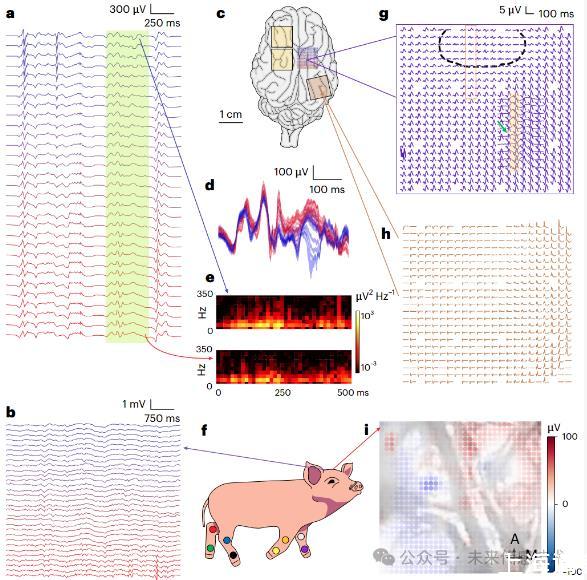
臨床轉化驗證了技術可行性。在5名神經外科患者的試點研究中,1024通道電極在清醒語言映射期間表現(xiàn)出99%的產率。術中記錄顯示,言語開始解碼準確率達87%,接近自然語言的識別水平。特別值得關注的是其與現(xiàn)有手術流程的兼容性:系統(tǒng)可無縫集成在癲癇或腫瘤切除手術中,無需額外增加開顱步驟,這極大降低了臨床轉化門檻。
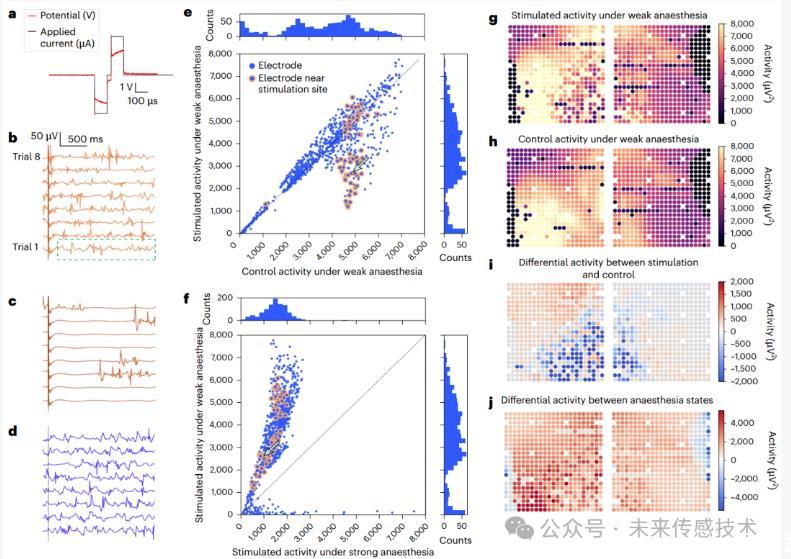
技術安全性經多維度驗證。42天慢性植入實驗顯示,薄膜電極組與傳統(tǒng)電極組的組織反應無顯著差異。運動皮層陣列移除后,軟膜再生完整度達100%。刺激安全性測試表明,100μA電流波形可誘發(fā)局部神經調制而不產生極化電位,這種精準調控能力在麻醉深度調節(jié)等應用中具有重要價值。
該技術的產業(yè)化前景值得期待。模塊化設計允許電極數(shù)量按需擴展,從529通道到2000+通道的靈活配置滿足不同臨床需求。在工業(yè)檢測領域,實時腦疲勞監(jiān)測系統(tǒng)已進入原型開發(fā)階段。對于癱瘓患者,意念控制外骨骼的90%+準確率預示著生活自理能力的重大提升。而在視覺重建方面,灰度感知的實現(xiàn)為全色視覺恢復提供了理論基礎。
這項研究標志著神經接口技術的范式轉變。通過微創(chuàng)植入和高密度記錄,研究團隊突破了傳統(tǒng)技術的生理和功能限制。未來研究需解決長期穩(wěn)定性問題,特別是慢性炎癥對信號質量的影響。同時,如何將亞毫米級刺激精度應用于更復雜的神經調控任務,仍需深入探索。但不可否認,這項技術已為腦機接口領域開辟了全新發(fā)展路徑。
 相關新聞
相關新聞