熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
對于上肢截肢者而言,能夠像控制原生肢體一樣自如地控制假肢,是夢寐以求的目標。近年來,靶向肌肉神經移植術(Targeted Muscle Reinnervation,TMR)已成為一項革命性技術。通過將殘端神經重新導向至鄰近的“閑置”肌肉(如胸肌),這些肌肉便成為了截肢者運動意圖的“生物放大器”,其表面肌電信號可用于控制假肢。
然而,傳統TMR面臨一個核心挑戰:控制上肢的神經(如正中神經、尺神經)是多功能、多束的“信息高速公路”,內含指揮手部各種精細動作的不同指令。當整條神經被轉移至一塊肌肉時,所有指令都匯聚于一點,導致肌電信號相互重疊、難以區分,限制了假肢的自由度控制。
為解決這一問題,再生周圍神經接口(RPNI)技術應運而生。它通過精細的外科手術將神經分離成獨立的束組,并分別植入小的肌肉移植物中,旨在創造多個獨立的信號源。但RPNI亦存在局限:神經分離帶有盲目性,可能損傷神經;可創建的信號源數量有限;且小肌肉移植物的信號穩定性難以保障。
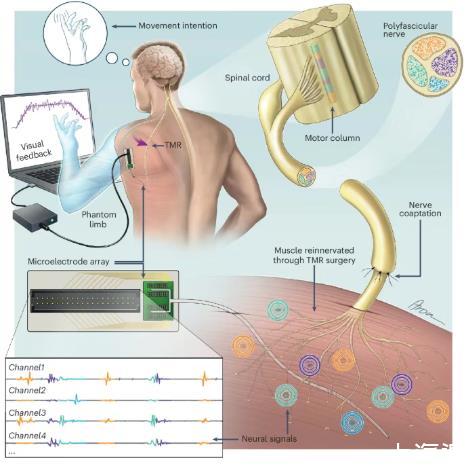
那么,能否在不進行風險較高的神經分離手術的前提下,仍能從單塊再生的肌肉中提取出多個清晰的控制命令呢?一項發表于《自然-生物醫學工程》的最新研究給出了肯定的答案。由帝國理工學院Dario Farina教授和維也納醫科大學Oskar C.Aszmann教授共同領導的研究團隊證明,結合高密度植入式微電極陣列和先進的數學解碼算法,能夠從一個再支配肌肉的單個記錄位點,成功分離出來自多束神經的不同功能信號。這項突破性研究為發展更強大、更精確的神經機器接口開辟了全新路徑。
帝國理工團隊提出了一項創新假設:即使多束功能不同的神經共同支配同一塊再生肌肉,只要使用足夠高空間分辨率的記錄手段,再輔以先進的信號處理方法,就能夠在數學層面“功能性地”分離這些混合的神經驅動信號。
為驗證這一設想,研究團隊在三名經肱骨或肩關節水平截肢的男性受試者身上開展了實驗。這些患者均在7至12年前接受了TMR手術,部分用于緩解神經瘤疼痛,部分旨在改善假肢控制能力。研究人員在其四塊經過神經再支配的再生肌肉中植入了40通道的高密度微電極陣列,實現了對局部肌電信號的精細采集。
成功解碼111個運動單元,揭示神經控制的生理機制
通過盲源分離技術,研究團隊首次在人類TMR肌肉中成功分解出共計111個信噪比超過30dB的單個運動單元(motor unit)活動。這些運動單元的動作電位形態多樣,部分伴有衛星電位,放電頻率分布在12–18脈沖/秒之間,變異系數合理,整體處于正常生理范圍。
更重要的是,研究發現:
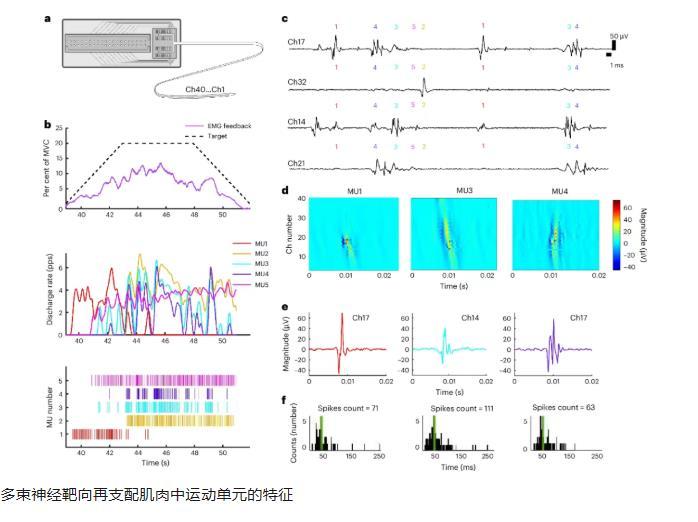
運動單元呈現出任務特異性激活模式,即某些單元僅在執行特定幻肢動作(如小指屈曲、三指捏握)時被募集;
即使在同一肌肉中,不同任務對應的神經驅動具有高度正交性(余弦相似度低至0.05–0.12),表明大腦能獨立調控不同動作;
通過非負矩陣分解(NNMF)等降維方法,研究人員識別出隱藏在高維運動單元活動背后的“神經流形”——一個低維潛在空間,能夠高效表征多種運動意圖。
例如,在兩塊肌肉(TMR1和TMR2)中,神經流形的維度恰好等于任務數量(6和5),說明每個任務都有獨特的神經編碼模式;而在另兩塊肌肉中,盡管任務更多,五維流形已足以區分絕大多數動作,體現了神經系統模塊化控制的效率。
信號穩定且可追蹤,具備臨床應用潛力
研究還評估了系統的長期穩定性。通過對同一任務在實驗開始與結束時重復執行,并追蹤相同運動單元的波形特征,結果表明大多數運動單元可在數小時內穩定重現,即使微電極發生輕微位移也能準確匹配。這證明該系統具備良好的魯棒性和可重復性,是邁向長期植入應用的重要一步。
此外,相關性分析顯示,約35%–66%的運動單元接收共同突觸輸入,且這種協同激活同時存在于特異性與共享單元中,符合現代運動控制理論中的“運動協同”(motor synergy)模型。
未來展望與挑戰
這項研究標志著仿生假肢控制領域的一個范式轉變。它表明,通過結合先進的植入式電極和智能解碼算法,TMR技術有望釋放出比先前認知更大的控制潛能,甚至可能超越RPNI在信號數量上的理論限制。研究者展望,未來或可通過將多條多束神經轉移至同一塊肌肉,創建“超再支配”肌肉,從而復制整個缺失肢體的全部神經信息,實現極其自然和直觀的假肢控制。
當然,將這項技術從實驗室推向臨床應用仍面臨挑戰。包括開發更安全、更耐用、無線化的長期植入式電極系統,以及實現解碼算法的實時化和自適應化,以應對日常生活中信號的自然波動。
參考文獻
Ferrante,L.,Boesendorfer,A.,Barsakcioglu,D.Y.et al.Implanted microelectrode arrays in reinnervated muscles allow separation of neural drives from transferred polyfunctional nerves.Nat.Biomed.Eng(2025).