熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
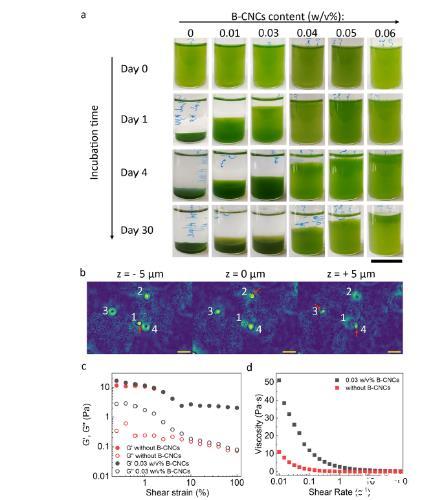
圖2、細菌纖維素納米晶體(B-CNC)對微藻溶液穩定性的影響。(a) 微藻懸浮沉積物在瓶底靜靜孵育 1 天后未添加 B-CNC,而 B-CNC 的加入則防止了微藻沉降(尺度條=2 厘米)。(b) 含有 0.03 w/v% B-CNC 的微藻懸浮液全息圖 Z 疊加。紅色箭頭表示各自框架中聚焦的微藻細胞,標記為 1、2、3 和 4,它們的焦點位置在 z 堆棧中顯示的不同高度:單元 1 位于 z = ?5 微米,單元 2 在 z=0 微米, 以及 3 和 4 單元,z=+5 微米。每個微藻細胞周圍可見數控中心簇(所有圖像中比例尺=20 微米)。(c) 在 10 rad/s 微藻懸浮液下,振蕩幅度從 0.1%掃蕩至 100%,無論是否使用 0.03 w/v% B-CNC,均為 4 天培養。通過穩態流動實驗評估微藻懸浮液的粘性行為,剪切速率范圍從 0.01 到 100 /s。(d) 含有 0 和 0.03 w/v% B-CNC 的懸浮液隨剪切速率變化的粘度剖面。
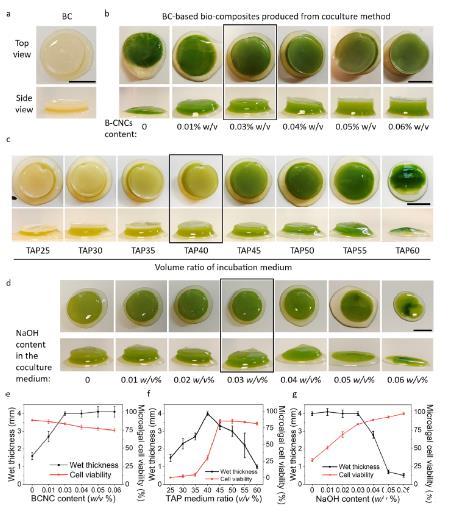
圖3、細菌和微藻共培養配方的優化。(a)從 4 天齡的 K. hansenii 靜態培養中采集的純細菌纖維素(BC)濕膜圖像,BC 膜形成于空氣-液體界面。(b)從 4 天齡的 K. hansenii/C. reinhardtii 靜態共培養中采集的 BC 基生物復合材料的頂視圖和側面圖像,含不同細菌纖維素納米晶體(B-CNC)(中等體積比為 TAP:HS = 40:60,NaOH 含量 0.03 w/v%)。(c) 來自共培養(B-CNCs 含量為 0.03 w/v%,無 NaOH 含量)的 BC 基生物復合材料的頂視圖和側視圖像(TAP25-HS 培養基的體積比 TAP25-TAP60)。(d) 從 4 天齡細菌和微藻靜態共培養中采集的 BC 基生物復合材料的頂視圖和側面圖像,含不同 NaOH 含量(中等體積比為 TAP:HS = 40:60(TAP40),B-CNCs 含量為 0.03 w/v%)。(e)B-CNC 含量、(f)培養基體積比和(g)NaOH 含量對 BC 基生物復合材料的濕厚和微藻細胞存活性的影響。(比例桿=1 厘米)。
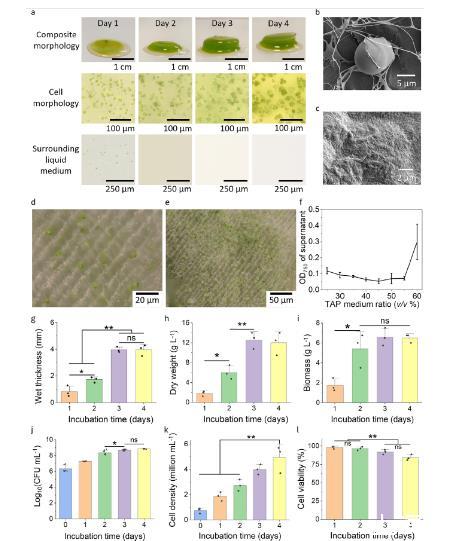
圖4、對基于 BC 的生物復合材料中的材料形態和生物活性的表征。(a) 從靜態 K. hansenii/C. reinhardtii 共培養(TAP:HS = 40:60;0.03 w/v% NaOH;0.03 w/v% B-CNC)采集的基于 BC 的生物復合物側面圖像,以及第 1、2、3、4 天記錄的光學顯微鏡圖像,顯示被困 C. reinhardtii 的形態及周圍液體培養基的外觀,記錄在第 1、2、3、4 天。(b)俯視掃描電子顯微鏡(SEM)圖像,顯示 C. reinhardtii 微藻纏繞在 BC 纖維網絡中。c,俯視 SEM 圖像,顯示被 BC 纖維和 K. hansenii 菌覆蓋的 C. reinhardtii 細胞。(d,e)BC 基生物復合材料的光微鏡圖像,展示了微藻細胞成功嵌入 BC 分層結構中的過程。(f) 周圍液體培養基在不同 TAP:HS 培養體積比下靜態孵育 4 天后的光學密度(OD750)。OD 值越低,表示微生物復合材料的微藻泄漏減少。(g–l)BC 基生物復合材料中生物活性的表征:(g)共培養樣品在培養過程中的濕厚、(h)干重和(i)生物量值。j, K. hansenii 細菌在共培養過程中的存活性。(k,l)共培養過程中微藻細胞密度(k)和細胞存活率(l)。(ns,不顯著;**p < 0.01;*p % 3C 0.05,基于事后圖基 HSD 的單因子(單因子)方差分析確定)。條形圖表示平均值(n = 3),誤差條表示標準差。 單獨的數據點疊加以顯示各組內的分布情況。
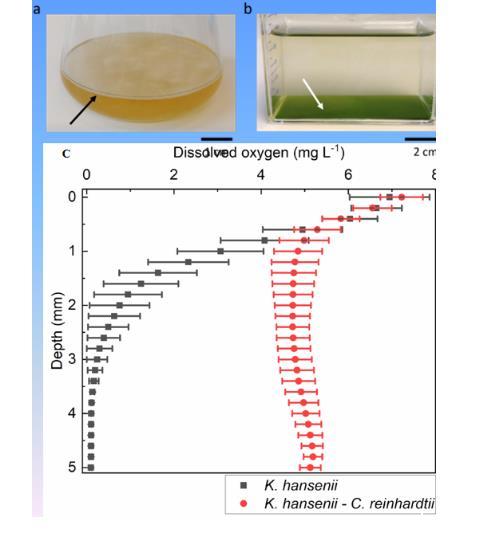
圖5、靜態培養 4 天后,細菌(K. hansenii)和微藻(C. reinhardtii)的液體培養物的照片。a. 在氣液界面處形成了一層固體的細菌纖維素(BC)膜(黑色箭頭)。b. 微藻細胞(白色箭頭)沉淀在培養瓶的底部。c. 在含有細菌(哈森氏菌)和微藻(雷納德氏藻)的培養體積內,溶解氧濃度的深度分布情況。
結論與展望
微生物之間的共生關系是全球生態系統功能的關鍵。在這里,我們通過創造通常在自然界中不協同生長的物種間人工共生關系,將這一概念推廣到生物材料制造。研究人員結合了生產纖維素的和綠色微藻實現細菌纖維素的整體生長。通常細菌纖維素以浮動的薄膜形式在培養基的空氣-液體界面產生,因為游離氧與培養基中的養分是細菌合成纖維素纖維所需的。在共培養中,細菌纖維素的生產可以大批量實現,超越空氣-液體界面的空間限制,因為具有光合作用活動的運動微藻在培養基中作為氧氣生成點。作為交換,纖維素提供的高度多孔且機械堅固的支架,使藻類-細菌群落能夠形成厚度達數厘米的生物復合結構。本研究直接證明了這種共生生長平臺允許在靜態培養條件下同時生產大批量細菌纖維素,采用任意但可調節的三維形狀,取決于培養容器的幾何形狀。
本研究提出了一種低干預、生物驅動的簡易方法,解決了BC材料在大體積、三維成型生產中的長期瓶頸,為未來可擴展的可持續功能材料生產奠定了基礎。Unisense微電極在本研究中主要用于直接測量靜態培養體系中的溶解氧濃度剖面,為了證實共培養體系中微藻(C. reinhardtii)能作為培養基內部的分布式氧氣源,研究過程中使用了Unisense微電極對培養液不同深度的溶解氧濃度進行了直接測量,從實驗上驗證了本研究的核心創新點——光合微藻能夠有效緩解氧氣擴散限制。證明了微藻在靜態培養中確實起到了“移動制氧站”的作用,為細菌在全液體體積內合成纖維素提供了必需的氧氣,從而突破了傳統BC生產只能發生在氣液界面的瓶頸。
 相關新聞
相關新聞