熱線(xiàn):021-66110810,66110819
手機(jī):13564362870


熱線(xiàn):021-66110810,66110819
手機(jī):13564362870
摘要: 鈷肟是流行的析氫分子催化劑,但迄今為止主要在非水條件下進(jìn)行研究。我們?cè)诖吮砻鳎鼈儗?duì)于設(shè)計(jì)用于中性水溶液的人工氫化酶也具有價(jià)值,并報(bào)告了通過(guò)將兩個(gè)鈷肟部分,{Co(dmgH)2} 和 {Co(dmgBF2)2}(dmgH2 = 二甲基乙二肟),結(jié)合到脫輔基抹香鯨肌紅蛋白(SwMb)上,制備兩種明確的生物雜交物種。所有光譜數(shù)據(jù)都證實(shí)鈷肟部分被插入到 SwMb 蛋白的結(jié)合口袋內(nèi),并與鈷復(fù)合物的軸向位置上的一個(gè)組氨酸殘基配位,從而形成熱力學(xué)穩(wěn)定的復(fù)合物。量子化學(xué)/分子力學(xué)對(duì)接計(jì)算表明,與附近存在的另一個(gè)組氨酸殘基(His64)相比,對(duì) His93 有配位偏好。有趣的是,鈷中心的氧化還原活性在這兩種生物雜交物中都得以保留,這使它們具有在近中性水條件下析氫的催化活性。
引言
氫化酶催化質(zhì)子可逆還原為分子氫。它們?cè)跓崃W(xué)平衡下發(fā)揮作用,并顯示出非常高的轉(zhuǎn)換頻率,從而使它們作為獨(dú)特的有效分子催化劑在與鉑金屬競(jìng)爭(zhēng) H2/H+ 相互轉(zhuǎn)換方面具有競(jìng)爭(zhēng)力。由于它們的活性位點(diǎn)僅包含地球儲(chǔ)量豐富的第一行過(guò)渡金屬,例如鐵和鎳,在過(guò)去二十年中已經(jīng)報(bào)道了許多用于析氫的仿生和生物啟發(fā)合成催化劑。特別是,鈷肟和二亞胺-二肟鈷配合物已被證明是非水介質(zhì)中最活躍的析氫催化劑之一。
很少有研究探討這類(lèi)催化劑在完全水相條件下的活性。總的來(lái)說(shuō),分子鈷基催化劑如鈷肟或二亞胺-二肟鈷配合物在 pH 7 時(shí)似乎不是很活躍,我們最近表明,它們?cè)?pH 7 的磷酸鹽水性緩沖液中周轉(zhuǎn)過(guò)程中會(huì)轉(zhuǎn)化為鈷基納米顆粒。穩(wěn)定這些催化劑以用于中性水介質(zhì)的一種可能途徑是通過(guò)更好地控制活性中心的直接環(huán)境。最近,所謂的“人工酶”形式中的金屬蛋白帶來(lái)了靈感。事實(shí)上,在金屬酶中,多肽框架控制溶劑的接近性,并為活性位點(diǎn)提供低介電常數(shù)和極性的周?chē)h(huán)境,從而既調(diào)節(jié)其催化活性,又保護(hù)其免受不希望的分解反應(yīng)。人工酶,其中一個(gè)分子合成催化劑被嵌入一個(gè)精心選擇的肽或蛋白質(zhì)中,最近被證明在水中具有催化活性。有趣的是,[Co(dmgH)2(py)Cl](dmgH2 = 二甲基乙二肟)與光系統(tǒng) I 的疏水自組裝產(chǎn)生了一種能夠光驅(qū)動(dòng) H2 生產(chǎn)的雜化復(fù)合物。
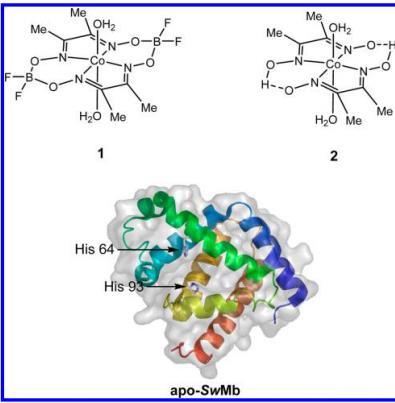
圖 1. 用于本研究的鈷肟配合物和抹香鯨肌紅蛋白(SwMb)的表示。蛋白質(zhì)的帶狀圖(PDB ID: 1UPD)顯示了血紅素結(jié)合口袋中的兩個(gè)組氨酸殘基(His64 和 His93)。
這些有希望的結(jié)果促使我們構(gòu)建基于鈷肟的人工氫化酶,即二氟硼烷橋連的鈷肟 [Co(dmgBF2)2(H2O)2](1)和質(zhì)子橋連的鈷肟 [Co(dmgH)2(H2O)2](2)。選擇抹香鯨肌紅蛋白(SwMb)作為宿主蛋白,因?yàn)樗軌蛲ㄟ^(guò)金屬離子在軸向位置上與位于其疏水腔中的適當(dāng)組氨酸殘基(His93)配位來(lái)結(jié)合幾種平面正方形配合物(包括其天然輔因子,血紅素)。我們?cè)诖藞?bào)告兩種能夠催化析氫的鈷肟-SwMb 生物雜交物 SwMb·1 和 SwMb-2 的制備以及生化和光譜表征。
實(shí)驗(yàn)部分
材料
血紅素、EuCl2、(乙二醇)雙(2-氨基乙基醚)-N,N,N',N'-四乙酸(EGTA)和 Nafion 溶液(5% 乙醇溶液)購(gòu)自 Sigma-Aldrich。[Co(dmgH)2(H2O)2] 和脫氮黃素(DAF)根據(jù)報(bào)道的程序制備。商業(yè)級(jí) C100 多壁碳納米管(MWCNTs;>95%)購(gòu)自 Nanocyl。S-(2,2,5,5-四甲基-2,5-二氫-1H-吡咯-3-基)甲基甲磺硫代酸鹽自 Reanal Private Ltd.(布達(dá)佩斯,匈牙利)購(gòu)買(mǎi)。
重組抹香鯨肌紅蛋白(SwMb)在大腸桿菌中的生產(chǎn)和純化根據(jù)報(bào)道的程序進(jìn)行,并作了一些修改。在該程序中,脫輔基-SwMb 通過(guò)將包涵體重溶于 0.1% 三氟乙酸水溶液中,然后依次對(duì) 20 mmol L-1 Tris-醋酸鹽(pH 5.0)和 50 mmol L-1 Tris-HCl(pH 7.5)溶液進(jìn)行兩次透析獲得(每一步通過(guò)離心去除沉淀的蛋白質(zhì))。進(jìn)一步的純化通過(guò)使用用 50 mmol L-1 Tris-HCl(pH 8.0)和 20 mmol L-1 NaCl 緩沖液平衡的 Superdex 75 Hiload 16/60 Prepgrade 柱進(jìn)行凝膠過(guò)濾(尺寸排阻色譜)。紫外-可見(jiàn)光監(jiān)測(cè)的滴定證實(shí)純化的蛋白質(zhì)完全用 1 當(dāng)量的血紅素重建。
物理測(cè)量
紫外-可見(jiàn)光譜使用 Shimadzu UV-1800 分光光度計(jì)在石英或塑料比色皿(1 cm 光程)中記錄。圓二色性(CD)測(cè)量使用 Jasco J-810 光譜儀進(jìn)行。電感耦合等離子體質(zhì)譜(ICP-MS)鈷滴定在格勒諾布爾大學(xué)醫(yī)院中心生物化學(xué)、毒理學(xué)和藥理學(xué)系進(jìn)行。電感耦合等離子體原子發(fā)射光譜(ICP-AES)鈷滴定在阿貢國(guó)家實(shí)驗(yàn)室使用 Thermo Scientific iCAP 600 光譜儀進(jìn)行,誤差在 5% 以?xún)?nèi)。蛋白質(zhì)濃度通過(guò)玫瑰紅滴定法確定(使用牛血清白蛋白作為標(biāo)準(zhǔn))。
連續(xù)波(CW)X 波段(9 GHz)電子順磁共振(EPR)實(shí)驗(yàn)使用兩臺(tái)不同的儀器獲得:(i)配備 Oxford ESR 910 低溫恒溫器的 Bruker EMX 光譜儀用于低溫研究(微波頻率用頻率計(jì)數(shù)器測(cè)量,磁場(chǎng)用 NMR 高斯計(jì)測(cè)量);(ii)Bruker ELEXSYS E580 EPR 光譜儀(Bruker Biospin,萊茵斯特滕,德國(guó)),配備 TE102 矩形 EPR 共振腔(Bruker ER 4102st)和氦氣流低溫恒溫器(Air Product,阿倫敦,賓夕法尼亞州)。溫度由 Lakeshore 低溫溫度控制器(韋斯特維爾,俄亥俄州)控制,大約為 5 或 80 K。CW 實(shí)驗(yàn)中使用的場(chǎng)調(diào)制導(dǎo)致導(dǎo)數(shù)型線(xiàn)形。高頻 EPR 測(cè)量在阿貢國(guó)家實(shí)驗(yàn)室使用自制的 D 波段(130 GHz)光譜儀進(jìn)行,配備單模 TE011 圓柱形腔。樣品的高頻 EPR 光譜以脈沖模式記錄,以消除由于快速通過(guò)效應(yīng)引起的微波相位失真。通過(guò)監(jiān)測(cè)雙微波脈沖序列的電子自旋回波(ESE)強(qiáng)度隨磁場(chǎng)變化的函數(shù)來(lái)記錄 EPR 光譜的吸收線(xiàn)形。微波脈沖的持續(xù)時(shí)間分別為 50 和 70 ns,微波脈沖之間的典型間隔時(shí)間為 150-300 ns。
數(shù)據(jù)處理
使用 Xepr(Bruker BioSpin)和 Matlab 7.11.1(MathWorks)環(huán)境進(jìn)行。磁性參數(shù)從 EPR 光譜的理論模擬中獲得。模擬使用 EasySpin 軟件包(版本 4.0.0)進(jìn)行。確定多頻 EPR 光譜組的電子 g 張量的精度估計(jì)為 ±0.001(相對(duì)值)。請(qǐng)注意,取決于樣品位置磁場(chǎng)校準(zhǔn)的絕對(duì)誤差更大。
用于 EPR 測(cè)量的生物雜交物溶液在 50 mmol L-1 Tris-HCl(pH 7.0)中制備,加入 100 mmol L-1 NaCl 和 10% 甘油,并在手套箱中引入 4-mm 外徑石英管中。自旋定量通過(guò)比較在非飽和條件下記錄的光譜的積分強(qiáng)度與在非飽和條件下記錄的 MTSL 自旋標(biāo)記溶液的光譜的積分強(qiáng)度來(lái)進(jìn)行。
 相關(guān)新聞
相關(guān)新聞