熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
研究簡介:在再生醫學中,有效管理外科皮瓣的組織缺血至關重要,但也充滿挑戰,主要是因為血液灌注不足常導致遠端皮瓣尖端壞死。本研究旨在探討嵌入在明膠甲基丙烯酰胺(GelMA)水凝膠中的過氧化氫酶涂覆的氧氣生成微粒(cOMP-GelMA水凝膠)的治療潛力,以建立有利于組織再生的優化微環境。通過使用大型(3 × 9 cm2)大鼠隨機皮瓣模型,評估了四組實驗對象的皮瓣存活與再生情況:對照組、純GelMA水凝膠組,以及含有兩種cOMP濃度(0.2% 和 0.5% w/v)的cOMP-GelMA水凝膠組。研究結果顯示,與含有0.5% cOMP的cOMP-GelMA相比,含有0.2% OMP的cOMP-GelMA能顯著增強血管生成、動脈生成、線粒體生物合成和抗氧化能力。此外,較低cOMP濃度(0.2%)比較高濃度(0.5%)更能顯著減輕炎癥反應。這些結果證明,通過適度的氧氣輸送所實現的輕度缺氧,通過過氧化物酶體增殖物激活受體γ共激活因子1-α和缺氧誘導因子1-α依賴的信號通路,有利于組織修復與再生。本研究突出了使用大型模型探索輕度缺氧治療益處的創新性,并表明cOMPs控制的氧氣輸送可以改善缺血組織的長期功能恢復。
Unisense微電極測定系統的應用
unisense氧氣微電極用于實時、原位監測皮瓣組織內的氧分壓(pO?)變化,從而客觀評估cOMP-GelMA水凝膠對局部氧微環境的調控效果。研究人員在大鼠皮瓣模型的特定位置(例如皮瓣遠端缺血區域)植入Unisense氧微電極,以直接測量組織內部的氧氣濃度。這種測量通常在術后不同時間點(如植入水凝膠后數小時至數天)進行,以動態追蹤氧分壓的時空變化。
實驗結論
研究證實了cOMP-GelMA水凝膠作為一種局部氧氣輸送平臺,在增強缺血組織修復方面具有顯著的治療潛力。其核心機制在于,通過可控的氧氣釋放,在植入部位創造了一個輕度缺氧的微環境。這種優化的微環境能夠有效促進血管生成和動脈生成,同時減輕炎癥反應并降低氧化應激。這些有益效果主要是通過激活缺氧誘導因子1-α(HIF-1α) 和過氧化物酶體增殖物激活受體γ共激活因子1-α(PGC-1α) 依賴的關鍵信號通路來實現的。該水凝膠具有良好的生物相容性、可擴展性,并且其皮下植入的策略使其能夠與皮下血管叢直接相互作用,克服了組織氧擴散的限制。這些發現為推進氧生成生物材料的臨床應用奠定了堅實基礎,不僅為解決重建外科中的關鍵挑戰提供了方案,也為治療糖尿病慢性潰瘍、心肌缺血等多種缺血性疾病指明了新的、可定制的治療方向。
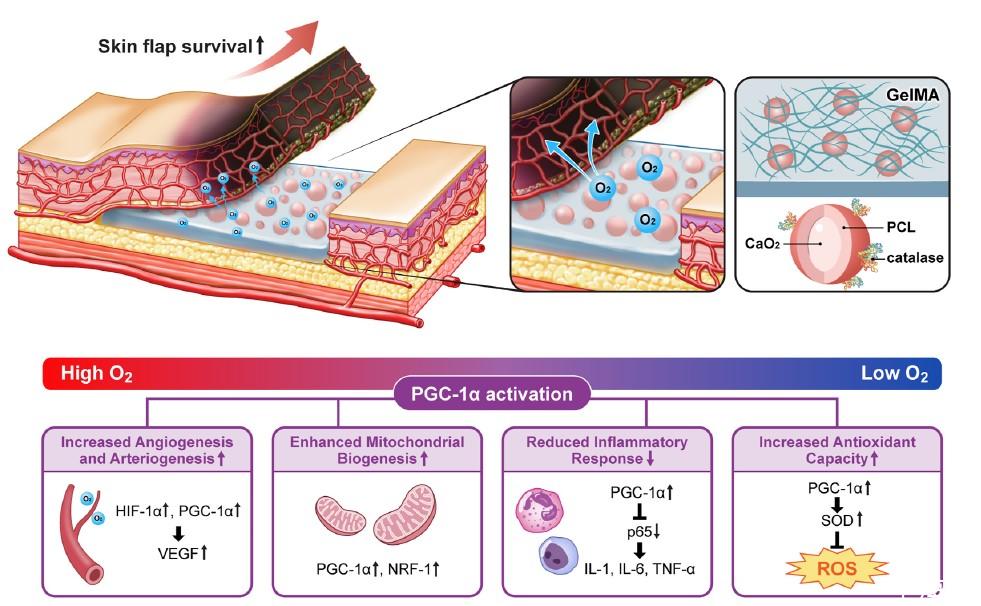
圖1、COMP-GelMA 水凝膠片植入后向缺血區域局部輸送氧氣的總體示意圖,以及通過提高 HIF-1α 水平和 PGC-1α 激活來增強皮瓣存活的可能機制。PGC-1α,過氧化物酶體增殖物激活受體γ共激活因子 1-α;HIF-1α,缺氧誘導因子 1-α。
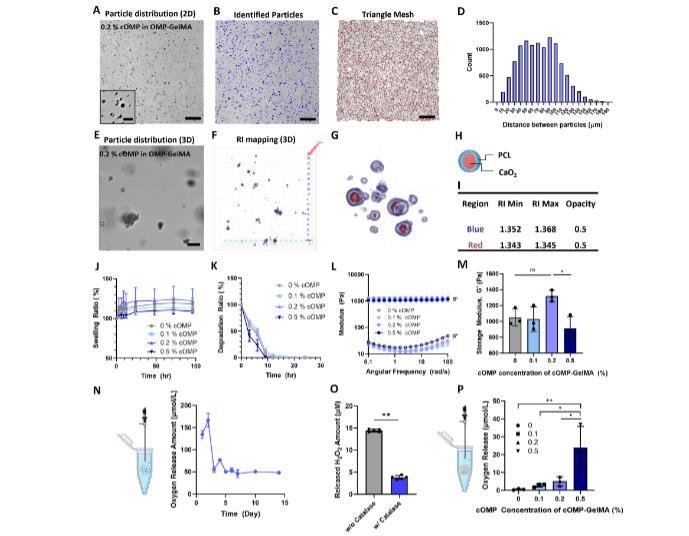
圖2、OMP-GelMA 的特性分析。(A)二維圖像展示了 OMP(0.2%)在 cOMP-GelMA 中的分布情況(比例尺為 500 微米,圖中插圖比例尺為 50 微米)。(B)通過使用 MATLAB 處理圖像來識別顆粒(藍色:OMP)。(C)顯示 cOMPs 之間三角形網格的圖像。(D)cOMPs 的距離分布圖。(E)包含 0.2% OMP 的 cOMP-GelMA 的三維斷層圖像(比例尺為 20 微米)。(F)折射率映射圖形結果顯示 OMP 的分布情況以及(G)其高幅度圖像。藍色:PCL,紅色:CaO2。(H)OMP 的示意圖。(I)藍色和紅色區域之間的折射率差異。(J)在 37℃下,不同 OMP 濃度的 cOMP-GelMA 在 PBS 中隨時間的膨脹率圖。
(K)在 37℃下,不同 OMP 濃度的 cOMP-GelMA 在 PBS 中加入 2μg/mL 膠原酶后隨時間的降解率圖。(L)cOMP-GelMA 的儲存和損耗模量隨角頻率的變化情況。(M)1 弦/秒時的 cOMP-GelMA 的儲存模量(*p < 0.01)。(N)從 1 毫升無氧 PBS 中 0.2% OMP 中隨時間測量的氧氣量示意圖以及 0.2% OMP 在 1 毫升無氧 PBS 中隨時間的氧氣釋放曲線。(O)純 OMPs 和 cOMP 釋放的 H2O2 量。(P)cOMP-GelMA 中氧含量的示意圖以及在室溫下無氧 PBS 中孵育 1 天后不同 OMPs 濃度下 cOMP-GelMA 釋放的氧量。