熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
細胞-電極界面的等效電路模擬
使用Multisim 14.3軟件模擬了細胞-電極界面,然后根據先前的研究構建了無源電路。本文設計了符合細胞-電極界面的等效電路。該等效電路由典型的細胞-電極界面元件和記錄元件組成,包括非連接膜電阻Rnj和電容Cnj、連接膜電阻Rj和電容Cj、封接電阻Rseal、金電極電阻Re和電容Ce、放大電阻Rin以及雜散電容Cstray。在模擬中,將標準方法獲得的動作電位用作原始動作電位。Rnj、Cnj、Rseal和Cstray的設置近似于文獻結果。Cj和Rj在微電穿孔后顯著降低,其值在微電穿孔前后分別近似為800pF和1.5GΩ,以及80pF和0.1GΩ。Re和Ce分別為3kΩ和4.37nF。
電生理記錄
心肌細胞在37°C和5% CO2下維持,并從細胞同步搏動的第三天開始采集電信號。使用32通道電生理信號采集系統記錄培養在微電極上的原代大鼠心肌細胞。該系統由連接細胞的微電極陣列、自制數據采集器、信號放大器和用于數據可視化的圖形用戶界面(即計算機軟件)組成。通過32通道微電極陣列記錄的數據使用LabVIEW軟件編寫的數據采集和可視化界面存儲和顯示。電生理信號以15kHz的采樣率進行1Hz至7.5kHz的帶通記錄。對于微電穿孔,向器件施加2500個周期的3V、200微秒方波電脈沖,總時間為1秒。微電穿孔是在與金微電極相同位置進行的。記錄系統在電穿孔期間持續采集信號。由于放大器飽和,在微電穿孔后恢復電生理記錄。
信號處理和統計分析
使用自定義MATLAB腳本分析信號采集系統收集的原始數據。該腳本程序具有多通道數據顯示、去噪、特征點提取和信號分離功能。首先可視化數據并手動選擇有效信號,然后對信號進行均值濾波以降低噪聲。為了進一步分離細胞外場電位和細胞內動作電位的同步信號,分別在兩個窗口中提取具有峰值點的數據段。本研究采用一種算法來提取電信號的峰值電位、基線電位和半最大電位,并通過時間序列分析確定信噪比、搏動頻率和50%動作電位持續時間。
此外,我們根據電信號的峰峰值手動計算了細胞內動作電位與細胞外場電位的比值。另外,通過手動識別電穿孔的開始和特征性細胞外電信號的出現,我們通過計算這兩個時間點之間的差異來估計電穿孔過程的持續時間。分析了從10個微電極記錄的數據,以評估以下參數,包括動作電位的峰峰值、細胞內動作電位峰峰值/場電位峰峰值、動作電位信噪比、場電位信噪比、動作電位持續時間、微電穿孔前后心肌細胞的搏動頻率以及50%動作電位持續時間。分析了來自4個實驗組的數據,每組包含從25-32個微電極記錄的數據,以評估單細胞動作電位信號比例和動作電位產率。在統計分析中,所有結果均以均值±標準誤差表示。使用Origin 2021軟件通過普通單因素方差分析對數據進行分析。,p<0.05;,p<0.01;,p<0.001;,p<0.0001;NS,無統計學意義。
結果
微電極陣列的制備和微電學表征
如圖1a所示,為了在相同芯片和同一批心肌細胞上探索微電極尺寸對使用微電穿孔記錄細胞內動作電位的影響,在同一芯片上設計了不同尺寸的微電極,尺寸分別為20、50、100、200和400微米。為了減少電信號泄漏并增強檢測靈敏度,非電極區域的金屬層覆蓋了一層2微米厚的SU-8絕緣材料。在培養階段,心肌細胞生長并附著在各種尺寸的微電極表面(圖1b)。在檢測期間,向微電極表面施加3V、200微秒的單相脈沖(1秒內2500個脈沖),使細胞膜形成納米孔,以進行細胞內動作電位的短期記錄(圖1c)。這些微電極可以以約0.2至1毫伏的幅度捕獲高質量的細胞內動作電位(圖1d)。
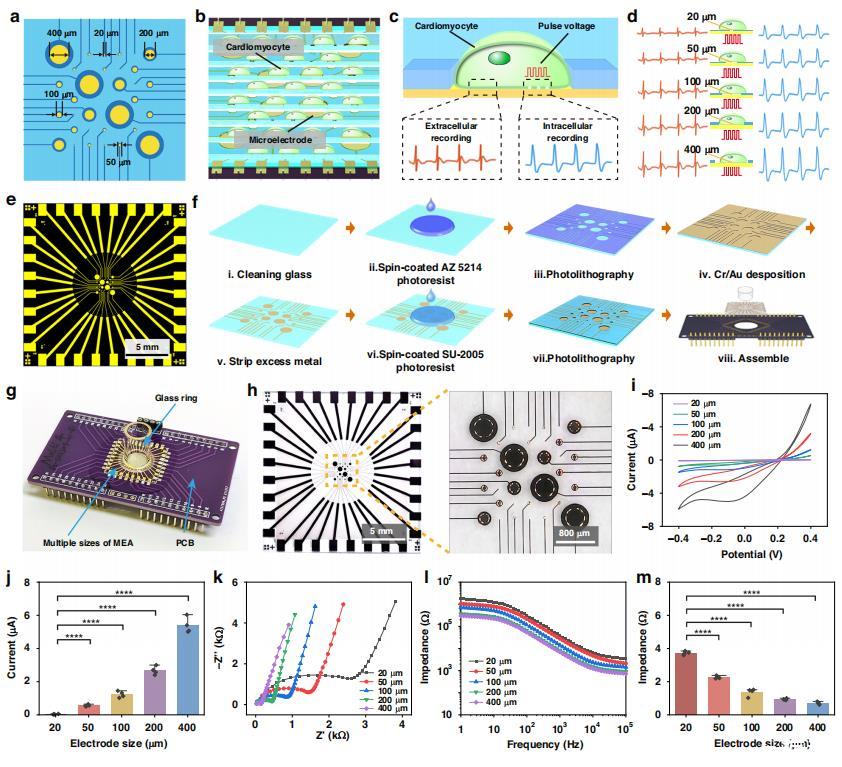
圖1. 用于記錄細胞內動作電位的多尺寸微電極陣列的設計、制造和電學表征。
a 多尺寸微電極陣列的布局示意圖,包含五種尺寸的微電極。
b 心肌細胞在多尺寸微電極陣列表面的培養示意圖。
c 通過微電穿孔記錄細胞內動作電位的示意圖。
d 通過微電穿孔記錄的心肌細胞典型細胞內動作電位波形。
e 用于制造多尺寸微電極陣列的掩模圖案CAD設計。
f 多尺寸微電極陣列的制造工藝流程。
g 組裝好的多尺寸微電極陣列器件照片。
h 從單個4英寸晶圓切割得到的25個獨立多尺寸微電極陣列芯片。
i 不同尺寸微電極在5 mM K3[Fe(CN)6]/K4[Fe(CN)6]溶液中的循環伏安曲線。
j 不同尺寸微電極的峰值電流統計圖。
k 不同尺寸微電極的電子轉移電阻統計圖。
l 不同尺寸微電極的電化學阻抗譜波特圖。
m 在1 kHz頻率下不同尺寸微電極的阻抗統計圖。統計圖每組分析n=4個數據,以均值±sem表示。顯著性差異通過單因素方差分析,,p<0.05;,p<0.01;,p<0.001;,p<0.0001。
制備多尺寸微電極陣列的過程始于使用CAD軟件創建掩模圖案(圖1e),隨后通過光刻技術制造器件。制造過程如圖1f所示,其中石英玻璃用作器件的基底,通過第一次光刻定義了微電極、導線和焊盤的輪廓。然后濺射鉻/金涂層,并使用丙酮剝離多余的金屬。接下來,通過二次光刻在金屬層上形成2微米厚的SU-8絕緣層,以隔離導線并暴露微電極的活性區域。在組裝階段,使用聚二甲基硅氧烷將多尺寸微電極陣列固定到定制的印刷電路板上,并使用導電銀膠將陣列連接到印刷電路板的相應焊盤上。隨后,使用聚二甲基硅氧烷將玻璃環粘附到微電極陣列的中心作為細胞培養區。
最后,將引腳排焊接到印刷電路板上以連接到記錄設備。圖1g展示了一個用于記錄心肌細胞內動作電位的完整微電極陣列器件。為了提高微電極陣列的生產率,設計了包含5x5微電極陣列陣列的光掩模用于微納制造,將其切割成25個獨立的微電極陣列芯片(圖1h)。
為了評估不同尺寸微電極的電性能,分別研究了不同尺寸微電極的電流響應和阻抗特性。如圖1i的循環伏安曲線所示,氧化還原峰的電流值隨著微電極尺寸的增加而逐漸增加。在20微米微電極中沒有觀察到明顯的[Fe(CN)6]3-/4-氧化還原峰,而在400微米微電極中,峰值電流達到5.01微安。如圖1j的統計數據所示,400微米微電極的峰值電流比20微米微電極高約142.63倍,這一結果表明較大尺寸的微電極具有更強的電荷轉移能力。
在圖1k中,微電極表面的電子轉移電阻隨著微電極尺寸的增加呈現出類似的增加趨勢,這與電流響應表征的結果一致。這種現象可歸因于較大尺寸的微電極擁有更多的活性位點。在阻抗分析方面,圖1l顯示了五種尺寸微電極在[Fe(CN)6]3-/4-溶液中的典型波特圖。結果表明,在相同掃描頻率下,微電極尺寸的增加導致微電極阻抗逐漸降低。具體來說,如圖1m所示,在1千赫茲頻率下,400微米微電極的阻抗(Z = 710.46歐姆,n=4)比20微米微電極( Z= 3721.84歐姆,n=4)低約5.24倍。這表明較大的微電極尺寸有利于電流的均勻分布并降低局部電流密度的波動,從而降低了局部阻抗。這一特性對于精確檢測各種低幅度生物電活動至關重要。
 相關新聞
相關新聞