熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
2.5. N2O 測量
使用配備電子捕獲檢測器和 Porapak Q 柱的氣相色譜儀,以 30 mL min-1 高純 N2 作為載氣,測量尾氣中的 N2O 濃度。
2.6. 微電極測量
使用 NH4+、NO2-、pH、DO 和 N2O 微電極進行微環境測量。前四種微電極是自制的,其性能先前已證明是穩定的。根據 de Beer 等人的方法,在測量前進行制造和校準。N2O 微電極購自 Unisense,丹麥。每次測量前進行三點校準(純水、50% N2O 溶液和飽和 N2O 溶液)。
從 PN 反應器中取出污泥絮體,輕輕地放置在流動池中尼龍網的正上方。微電極在沉降條件下穿透污泥聚集體。為了獲得穩態剖面,在開始剖面測量前將污泥聚集體靜置 30 分鐘,并且每種微電極測量至少進行三次。由于絮體具有對稱結構,微電極只需穿透絮體深度的一半即可反映整個底物分布。
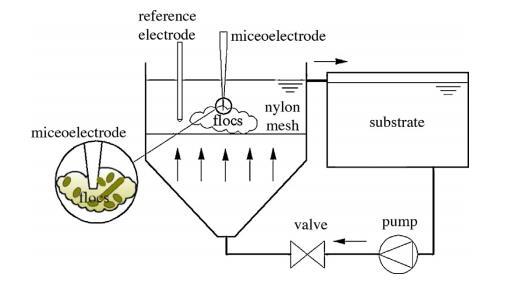
圖1:用于微電極測量的流動池設置示意圖
用于微剖面測量的流動池中的培養基由 NH4Cl (4.2 mg N L-1)、NaNO2 (4.2 mg N L-1) 和 NaHCO3 (37.8 mg L-1) 組成,并通過添加 HCl (0.5 mol L-1) 和 NaOH (0.5 mol L-1) 來控制不同的 pH 值。為了提供氧限制條件,通過吹入 N2 將該培養基的 DO 濃度維持在 1 mg L-1 以下。由于 PN 反應器的 pH 在 6.8-8.5 范圍內變化,因此選擇了四個不同的 pH 值 (7.0, 7.5, 8.0 和 8.5) 進行微剖面測量。
2.7. 凈體積速率計算
根據物質傳遞方程計算凈體積速率:
?C(z, t)/?t = Ds \* ?^2 C(z, t)/?z^2 - Q(z) + P(z)
其中 C(z, t) 分別是時間 t 和深度 z 處的底物濃度。Q 和 P 分別是消耗和產生速率。Ds 是有效擴散系數;在 25°C 時,計算 NH4+、NO2- 和 N2O 時分別使用了 1.38×10^-9、1.25×10^-9 和 2.10×10^-9 m^2 s^-1 的 Ds 值。
當達到穩態時,左邊表達式為零。方程 (1) 可簡化為:
Ds \* ?^2 C(z)/?z^2 = Q(z) - P(z)
定義 R(z) = Q(z) - P(z) 為凈體積速率。使用歐拉公式進行數值積分,可以得到以下方程:
?C/?z\_(n+1) = ?C/?z\_n + h \* R\_n / Ds
其中 h 是步長。根據濃度梯度,可以得到以下方程:
C\_(n+1) = C\_n + h \* ?C/?z\_n
將 ?C/?z\_n 代入方程 (3),可以計算為:
R\_(n-1) = Ds [ (C\_(n+1) - C\_n) / h - ?C/?z\_(n-1) ] / h。
3. 結果
3.1. pH 對 PN 性能的影響
在每個 pH 值下,反應器至少運行一周。在初始 pH 范圍 7.5-8.5 內,pH 的變化對部分亞硝化幾乎沒有影響。進水 NH4+ 濃度為 598±12 mg N L-1,SBR 將大約一半的 NH4+-N 轉化為 NO2--N。出水中 NH4+ 和 NO2- 的濃度分別為 283±16 和 297±22 mg N L-1。出水中 NO2- 與 NH4+ 的摩爾比為 1.05±0.12,這適合作為厭氧氨氧化過程的進水。出水中的 NO3- 濃度為 28.40±2.46 mg N L-1,表明亞硝酸鹽氧化細菌的活性較低。
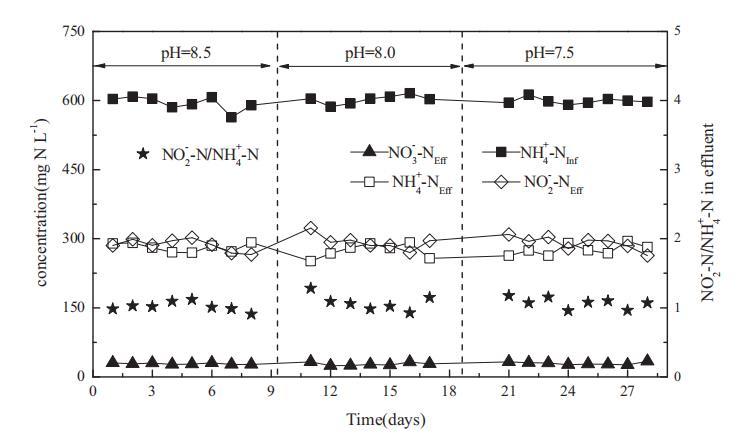
圖2:不同初始pH下部分亞硝化反應器的性能
3.2. 微生物群落結構
在第 25 天,使用 PCR 和 DGGE 分析研究了微生物群落。檢測到了已知的 AOB——亞硝化單胞菌屬,這與其他部分亞硝化系統的觀察結果一致。雖然未向反應器投加有機物,但也檢測到了已知具有反硝化功能的異養菌——叢毛單胞菌屬、黃桿菌屬和食酸菌屬。有機化合物可能來自生物質的衰亡。值得注意的是,盡管在反應器中觀察到了硝化作用,但未檢測到 NOB。未檢測到 NOB 意味著它們占細菌種群的 <9%。
3.3. 單個周期中 pH 對 N2O 排放的影響
初始 pH 對單個周期中氮轉化的影響如圖3所示。對于所有 pH 值,DO 濃度下降并維持在 0.3 mg L-1 左右。pH 隨著部分亞硝化過程的進行而降低,但在初始 pH 值為 8.0 和 7.5 時,在初始處理時間 40 分鐘內觀察到 pH 略有增加,這是由于 CO2 的吹脫。
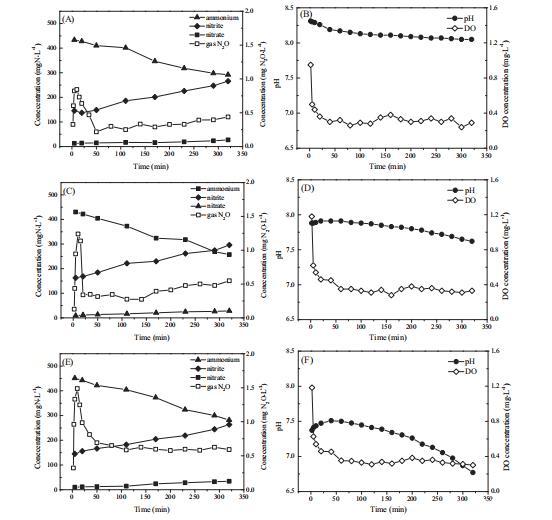
圖3. 不同pH水平下部分亞硝化循環過程中氮和工藝參數的變化(A和B對應初始pH為8.5,C和D對應初始pH為8.0,E和F對應初始pH為7.5)
NH4+ 的濃度幾乎呈線性下降,而 NO2- 的濃度幾乎呈線性增加,在曝氣過程結束時,NO2- 與 NH4+ 離子的摩爾比接近 1:1。AOR 顯示,隨著 pH 從 8.5 降低到 8.0 和 7.5,它們從 0.144 增加到 0.158 和 0.176 mg NH4+-N min-1 g-1 MLSS,表明 AOB 的活性隨著初始 pH 的降低而增加。這與 Hulle 等人的發現一致,他們發現當 pH 升高超過 7.23 時,AOB 活性降低。NO3- 離子的濃度從大約 10 mg N L-1 緩慢增加到 30 mg N L-1。
在曝氣時間的最初 50 分鐘內,在曝氣 10 分鐘后觀察到一個 N2O 排放峰。對于初始 pH 值 7.5、8.0 和 8.5,獲得的最大 N2O 濃度分別為 1.43、1.24 和 0.84 mg L-1。從運行時間 50 分鐘起,尾氣中 N2O 排放的趨勢發生了變化。在初始 pH 值 8.5 和 8.0 時,N2O 濃度分別從 0.22 緩慢增加到 0.44 mg L-1 和從 0.31 增加到 0.55 mg L-1,而在 pH 7.5 時,N2O 濃度維持在 0.6 mg L-1 左右。在 pH 7.5、8.0 和 8.5 時,一個周期內分別獲得 63.74、40.59 和 34.72 mg 的 N2O 排放量。這表明在氧限制條件下,隨著初始 pH 從 7.5 增加到 8.5,N2O 排放量減少。
 相關新聞
相關新聞