熱線:021-66110810,66110819
手機:13564362870


熱線:021-66110810,66110819
手機:13564362870
作為替代方法,我們預(yù)期mIm表面配體具有足夠的親核性以打開環(huán)氧環(huán)并與ZIF表面形成β-羥烷基共價鍵。基于這一推理,我們用甲氧基聚乙二醇環(huán)氧(mPEG;Mn = 750 g mol?1)與ZIF-8納米晶體反應(yīng)。通過質(zhì)譜確認(rèn)了開環(huán)環(huán)氧與mIm之間預(yù)期共價鍵的形成,NMR消化實驗表明約10%的mIm表面配體被mPEG功能化。值得注意的是,這種接枝密度(0.8配體每nm2)足以穩(wěn)定水中高達8.3 vol%(7.0 wt%)的ZIF-8膠體溶液,在至少5天內(nèi)沉淀或聚集最小。與用PEG非共價功能化的ZIF-8納米晶體相比,濃度函數(shù)的溶液密度與含有空氣填充孔的多孔液體預(yù)期一致,測量的O?容量為理論量的96%±7%。因此,用低分子量配體進行共價表面修飾可以在保持永久微孔性和高氣體吸收容量的同時賦予疏水MOF在水中的膠體分散性。
這里報告的多孔液體的高氣體容量為體外或體內(nèi)O?輸送等提出了有趣的可能性。自然界經(jīng)過數(shù)億年進化出復(fù)雜且嚴(yán)格調(diào)控的系統(tǒng)來在水中輸送O?,當(dāng)這些系統(tǒng)缺失或失效時,輸送足夠的O?以防止缺氧是具有挑戰(zhàn)性的。
已經(jīng)探索了多種天然和合成氣體載體——包括無細胞血紅蛋白、血紅素模擬物、全氟碳乳液和脂質(zhì)涂層或聚合物涂層微泡——以從水性流體輸送O?,但克服包括有限的氣體攜帶容量、對釋放動力學(xué)的控制差、缺乏可逆性、大顆粒尺寸、劑量限制性毒性和長期穩(wěn)定性等問題仍然是一個未解決的挑戰(zhàn)。因此,目前美國食品藥品監(jiān)督管理局沒有批準(zhǔn)可注射的O?來源或人工血液替代品,盡管經(jīng)過數(shù)十年的研究。在1 bar和25°C下氧化時,血液的O?攜帶容量約為24 ml dl?1(假設(shè)15 g Hb dl?1),比純水中可溶解的2.9 ml dl?1大一個數(shù)量級。
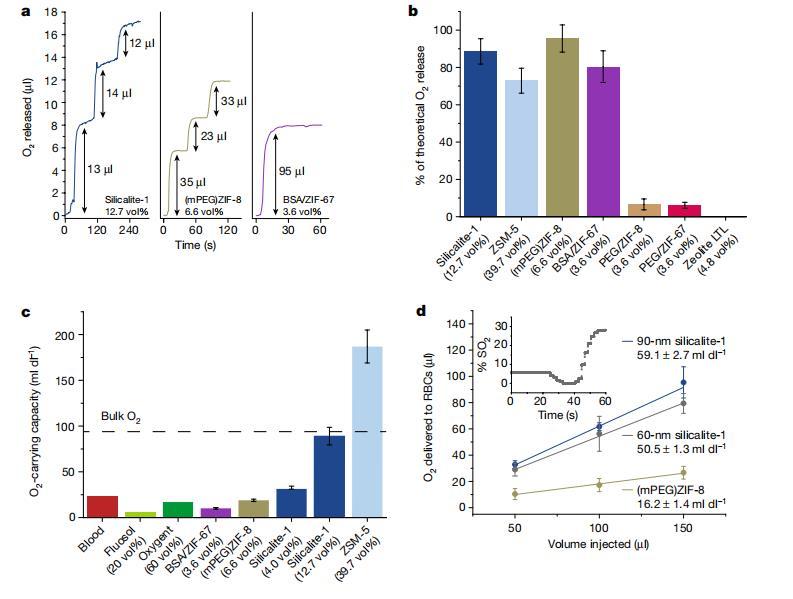
圖4 | 水與血液中的O2釋放測量結(jié)果。a、將氧合硅沸石-1、(mPEG)ZIF-8及BSA/ZIF-67納米晶體溶液注入脫氧水后的O2釋放動力學(xué)。所有溶液均注入1.2 ml氣密瓶中,注射體積標(biāo)注于箭頭旁。b、疏水性沸石與 MOF 納米晶體氧合水溶液釋放的O2量相對于理論值的對比(理論值基于完全干燥孔隙且氣體容量與固態(tài)測量值相當(dāng)?shù)募僭O(shè))。c、疏水性沸石與 MOF 納米晶體水溶液的O2載量與血液(15 g Hb/dl?1)及兩種代表性全氟化碳乳劑(Fluosol與Oxygent)的O2載量比較。所有數(shù)據(jù)均基于常溫下1 bar O2平衡條件下的溶液。d、(mPEG)ZIF-8(6.7 vol%)及硅沸石-1納米晶體溶液(60 nm與90 nm納米晶體體積分?jǐn)?shù)分別為9.1 vol%與11.0 vol%)對脫氧濃縮紅細胞(RBCs)的O2釋放量隨注射體積變化關(guān)系。各溶液的O2載量通過數(shù)據(jù)線性擬合斜率計算得出。需注意所有溶液均在常溫1 bar O2條件下平衡,并含5%葡萄糖。插圖:單次注射100 μl 60 nm硅沸石-1納米晶體溶液(9.1 vol%)的典型O2釋放動力學(xué)曲線。基線數(shù)據(jù)采集需在注射前至少持續(xù)4分鐘,以確保氧傳感器穩(wěn)定。圖b-d中的誤差條表示每個數(shù)據(jù)點至少三次獨立測量所對應(yīng)的標(biāo)準(zhǔn)差。
在非共價O?載體中,脂質(zhì)涂層微泡分散體(90 vol%)已被證明具有接近O?氣相密度(91 ml dl?1)的不可逆O?容量,而濃縮的全氟碳乳液(60 vol%)已達到高達17 ml dl?1的可逆O?容量。多孔液體提供了遠遠超過這些值的可逆O?容量的途徑,這將允許從較小體積的水性流體輸送更大量的O?。特別是,由于silicalite-1和ZIF-8納米晶體在固態(tài)下分別吸附731 ml dl?1和241 ml dl?1的O?,低濃度水性溶液應(yīng)能夠儲存和輸送異常高密度的O?。事實上,6.6 vol%的(mPEG)ZIF-8納米晶體溶液的測量O?攜帶容量與許多全氟碳乳液相似,后者的濃度至少為20 vol%。
此外,在僅4.0 vol%的濃度下,我們90 nm silicalite-1納米晶體的水性溶液具有31.3±0.1 ml dl?1的測量可逆O?容量,超過血液。在12.7 vol%的濃度下,這種O?攜帶容量增加到89±10 ml dl?1,與體相O?氣體的密度相當(dāng)。盡管較高濃度的silicalite-1溶液傾向于凝膠化,但我們發(fā)現(xiàn)ZSM-5納米晶體——silicalite-1的同結(jié)構(gòu)鋁硅酸鹽類似物——比silicalite-1納米晶體具有更親水的外表面(ZSM-5和silicalite-1的zeta電位分別為-49.1 mV和-38.7 mV)。
因此,我們能夠在水中形成高達40 vol%濃度的ZSM-5納米晶體穩(wěn)定膠體溶液,即使在較高濃度下也具有相對較低的粘度。此外,密度測量證實,在這種高Si/Al比下,微孔足夠疏水以防止水侵入并形成多孔溶液。這導(dǎo)致極高的測量O?攜帶容量187±18 ml dl?1,據(jù)我們所知,這超過了任何其他天然或合成水性O(shè)?載體。
作為對這些多孔液體的高O?攜帶容量是否可以轉(zhuǎn)化為比純水更具生物醫(yī)學(xué)相關(guān)性的環(huán)境的初步探索,我們進行了離體實驗,以測試向脫氧捐獻人血輸送O?。
值得注意的是,密度測量證實,silicalite-1和(mPEG)ZIF-8納米晶體的永久微孔性在5%葡萄糖溶液中得以保持,該溶液與紅細胞等滲。這些溶液的O?攜帶容量是通過測量將不同體積的氧化溶液添加到脫氧紅細胞時氧合血紅蛋白濃度的變化來提取的。值得注意的是,90 nm silicalite-1納米晶體(11.0 vol%)、60 nm silicalite-1納米晶體(9.1 vol%)和(mPEG)ZIF-8(6.6 vol%)在5%葡萄糖中的氧化溶液在注入紅細胞后迅速釋放O?,釋放的O?量以劑量依賴性方式線性增加。
提取的O?攜帶容量與從吸附測量和純水中O?釋放實驗預(yù)測的值非常一致。此外,更濃縮的silicalite-1膠體溶液能夠向紅細胞輸送110 ml dl?1的O?。這些原理驗證實驗證明了水性多孔液體用于體內(nèi)或體外O?輸送的潛力,但我們注意到,在設(shè)計滿足特定生物醫(yī)學(xué)要求的流體時,需要考慮除氣體攜帶容量之外的許多其他因素——包括循環(huán)性、生物相容性、長期穩(wěn)定性和成本。
總的來說,我們的結(jié)果表明如何應(yīng)用熱力學(xué)原理將微孔固體的高表面積和氣體容量帶到水性流體中。這種方法對生物醫(yī)學(xué)和能源技術(shù)具有顯著影響,其中許多技術(shù)受限于氣體分子通過水性環(huán)境的傳輸。例如,微孔水概念可以導(dǎo)致新的電解質(zhì),補充或替代電催化反應(yīng)中的氣體擴散電極,或通過允許更高密度的氣體分子局部化在電極表面來克服使用稀釋氣體流的燃料電池中的質(zhì)量傳輸限制——有效地充當(dāng)氣體緩沖器。
除了催化和能源儲存,水性多孔液體還可以作為酸性氣體分離的綠色溶劑,因為這些流體提供了比現(xiàn)有物理吸附過程中使用的有機溶劑系統(tǒng)更高的氣體溶解度、更低的成本和更少的有害環(huán)境影響的機會。在生物醫(yī)學(xué)方面,微孔水可以實現(xiàn)減壓病的治療,或作為人工血液替代品的O?來源、創(chuàng)傷誘導(dǎo)缺氧的橋接療法或器官和組織保存介質(zhì)。盡管除了氣體攜帶容量之外,還需要考慮許多因素才能將這些系統(tǒng)轉(zhuǎn)化為可行的技術(shù),但設(shè)計具有不同晶體結(jié)構(gòu)、納米晶體尺寸和形狀以及外表面官能團的疏水沸石和MOF有無數(shù)的可能性,以創(chuàng)建具有高氣體容量和針對特定應(yīng)用定制特性的微孔水。
方法
材料合成
90 nm silicalite-1納米晶體的合成
90 nm silicalite-1納米晶體的合成遵循先前報道的程序。在代表性合成中,將四丙基氫氧化銨水溶液(TPAOH;31.51 ml,40 wt%)、H?O(40.52 ml)和四乙氧基硅烷(TEOS;38.36 ml)在250 ml玻璃瓶中混合。最初的雙相混合物攪拌18小時,使TEOS在堿性環(huán)境中水解并將乙醇(EtOH)釋放到溶液中。水解后,該溶液的摩爾比為9 TPAOH : 25 SiO? : 480 H?O : 100 EtOH。將均相溶液裝入23 ml和45 ml Parr酸消化容器中,每個容器填充約50%的溶液。密封后加熱至90°C 48小時。冷卻容器后,產(chǎn)物用納米純水稀釋約十倍,并以7,830 rpm(7,197 rcf)離心80分鐘。然后去除上清液,用納米純水洗滌六次。最終洗滌后,樣品在60°C下在離心管中干燥過夜。收集干燥的樣品并 finely 研磨成粉末。將約3 g粉末倒入氧化鋁坩堝中,裝入管式爐。粉末在流動的N?下通過加熱至200°C 1小時并在此溫度下保持2小時來干燥。然后通過在流動的空氣下加熱至550°C 1小時并在此溫度下保持10小時來煅燒粉末。然后將樣品冷卻至環(huán)境溫度并收集。
60 nm silicalite-1納米晶體的合成
在代表性合成中,將TPAOH水溶液(53.35 ml,40 wt%)和TEOS(64.46 ml)在250 ml玻璃瓶中混合。雙相混合物攪拌68小時,以使TEOS完全水解并使溶液老化。所得溶液的摩爾比為9 TPAOH : 25 SiO? : 380 H?O : 100 EtOH。老化完成后,打開溶液并將其放入110°C的油浴中以蒸發(fā)TEOS水解過程中產(chǎn)生的EtOH。在2小時內(nèi),油浴溫度升至120°C。加熱后,重新稱重溶液并添加H?O以替換加熱過程中蒸發(fā)的水,并將溶液的摩爾比調(diào)整為9 TPAOH : 25 SiO? : 280 H?O。將所得均相溶液裝入23 ml Parr酸消化容器中,每個容器填充約50%的溶液。密封后加熱至80°C 48小時。冷卻容器后,產(chǎn)物用納米純水稀釋約十倍,并以7,830 rpm(7,197 rcf)離心180分鐘,去除上清液,用納米純水洗滌六次。最終洗滌后,樣品在60°C下在離心管中干燥過夜。收集干燥的樣品,finely 研磨成粉末,并按照上述90 nm silicalite-1納米顆粒描述的相同程序進行煅燒。
 相關(guān)新聞
相關(guān)新聞